甲醇脱氢可制取甲醛,反应原理为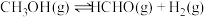 ,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是

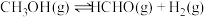 ,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
A.脱氢反应的 |
B.600K时,Y点: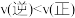 |
| C.要实现从Y点到Z点的变化可通过增大压强的方法 |
D.在 时,该反应的平衡常数为8.1 时,该反应的平衡常数为8.1 |
更新时间:2022/02/27 12:29:05
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应A(g)+B(g) 2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
 2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是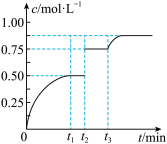
| A.若t1=2min,则v(D)=0.125mol/(L·min) |
| B.t2时刻改变的条件是增加等物质的量的A和B |
| C.t1时刻后向体系中再充入A、B、C各1mol,则v正>v逆 |
| D.若t3时刻改变的条件是升温,则该反应是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氨的催化氧化是硝酸工业中的重要反应: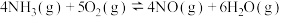
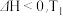 时,将
时,将 和
和 的混合气体充入
的混合气体充入 恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
下列说法正确的是
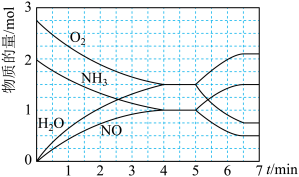
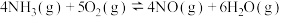
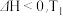 时,将
时,将 和
和 的混合气体充入
的混合气体充入 恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:下列说法正确的是

A. , ,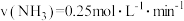 |
| B.加催化剂或缩小容积均可降低反应的活化能,提高反应速率 |
C. 时, 时,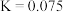 |
D. 时,改变的条件可能为降低温度 时,改变的条件可能为降低温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】对于可逆反应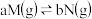
 ,同时符合如图各曲线,则下列判断正确的是
,同时符合如图各曲线,则下列判断正确的是

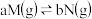
 ,同时符合如图各曲线,则下列判断正确的是
,同时符合如图各曲线,则下列判断正确的是
A. , , , , | B. , , , , |
C. , , , , | D. , , , , |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是 ( )
| A.密闭容器中有一定量红棕色的NO2,加压(缩小体积)后颜色先变深后变浅 |
| B.高压条件比常压条件有利于SO2和O2合成SO3 |
| C.由H2(g)、I2(g)、HI(g)组成的平衡体系加压(缩小体积)后颜色变深 |
| D.实验室用排饱和食盐水的方法收集氯气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知反应:3M(g)+N(g)⇌P(s)+4Q(g)ΔH<0。图中a、b曲线表示在密闭容器中不同条件下,M的转化率随时间的变化情况。若使曲线b变为曲线a,可采取的措施是
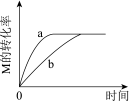

| A.增大压强 | B.增加N的浓度 | C.加少量固体P | D.升高温度 |
您最近一年使用:0次
【推荐1】已知: ,
, 均难溶于水,
均难溶于水, ,离子浓度
,离子浓度 时认为其沉淀完全。
时认为其沉淀完全。 时,
时, ,
, 的沉淀溶解平衡曲线如图所示,其中
的沉淀溶解平衡曲线如图所示,其中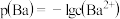 ,
,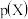
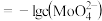 或
或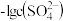 。下列叙述正确的是
。下列叙述正确的是

 ,
, 均难溶于水,
均难溶于水, ,离子浓度
,离子浓度 时认为其沉淀完全。
时认为其沉淀完全。 时,
时, ,
, 的沉淀溶解平衡曲线如图所示,其中
的沉淀溶解平衡曲线如图所示,其中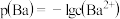 ,
,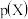
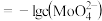 或
或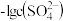 。下列叙述正确的是
。下列叙述正确的是
A. 时, 时,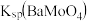 的数量级为 的数量级为 |
B. 时, 时, 点对应为 点对应为 的饱和溶液 的饱和溶液 |
C. 时, 时,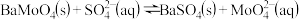 的平衡常数 的平衡常数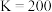 |
D. 时,向浓度均为 时,向浓度均为 的 的 和 和 的混合溶液中加入 的混合溶液中加入 溶液,当 溶液,当 恰好完全沉淀时,溶液中 恰好完全沉淀时,溶液中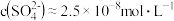 |
您最近一年使用:0次
【推荐2】一定量的 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: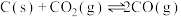 。平衡时,体系中气体体积分数与温度的关系如下图所示:
。平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(p分)=气体总压(p总)×体积分数
下列说法正确的是
 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: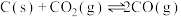 。平衡时,体系中气体体积分数与温度的关系如下图所示:
。平衡时,体系中气体体积分数与温度的关系如下图所示:
已知:气体分压(p分)=气体总压(p总)×体积分数
下列说法正确的是
A. 时,若充入惰性气体,v正,v逆均减小,平衡不移动 时,若充入惰性气体,v正,v逆均减小,平衡不移动 |
B. 时,反应达平衡后 时,反应达平衡后 的转化率为 的转化率为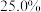 |
C. 时,若充入等体积的 时,若充入等体积的 和 和 ,平衡向逆反应方向移动 ,平衡向逆反应方向移动 |
D.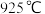 时,化学平衡常数 时,化学平衡常数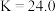 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在甲、乙两个体积均为IL的恒容密闭容器中分别加入1molQ(g),发生反应2Q(g) M(g)+N(g),其中Q的物质的量随时间的变化如表:
M(g)+N(g),其中Q的物质的量随时间的变化如表:
下列说法中正确的是
 M(g)+N(g),其中Q的物质的量随时间的变化如表:
M(g)+N(g),其中Q的物质的量随时间的变化如表:| 时间/s | t | 2t | 3t | 4t | 5t | 6t | 7t | |
| Q/mol | 甲 | 0.60 | 0.30 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| 乙 | 0.72 | 0.51 | 0.36 | 0.25 | 0.22 | 0.20 | 0.20 | |
| A.反应的温度:甲容器高于乙容器 |
| B.甲容器中一定加入了催化剂,乙容器中一定未加入催化剂 |
C.用M表示甲容器中从起始到平衡的反应速率一定是: mol•L-1•s-1 mol•L-1•s-1 |
| D.两个容器中反应的平衡常数都是4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定条件下进行反应:COCl2(g) Cl2(g)+CO(g)。向2.0L恒容密闭容器中充入1.0molCOCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见表:
Cl2(g)+CO(g)。向2.0L恒容密闭容器中充入1.0molCOCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见表:
下列说法正确的是
 Cl2(g)+CO(g)。向2.0L恒容密闭容器中充入1.0molCOCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见表:
Cl2(g)+CO(g)。向2.0L恒容密闭容器中充入1.0molCOCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见表:| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A.保持其他条件不变,升高温度,平衡时c(Cl2)=0.22mol·L-1,则反应的△H<0 |
| B.若在2L恒容绝热(与外界没有热量变换)密闭容器进行该反应,化学平衡常数不变 |
| C.保持其他条件不变,起始向容器中充入1.20molCOCl2、0.60molCl2和0.60molCO,反应达到平衡前的速率:v(正)<v(逆) |
| D.2s时,用CO表示的化学反应速率为0.75mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,向三个容积不等的恒容密闭容器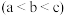 中分别投入
中分别投入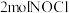 ,发生反应:
,发生反应: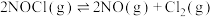 。
。 后,三个容器中
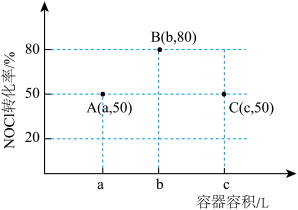
后,三个容器中 的转化率如图中A、B、C三点。下列叙述正确的是
的转化率如图中A、B、C三点。下列叙述正确的是
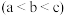 中分别投入
中分别投入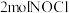 ,发生反应:
,发生反应: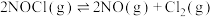 。
。 后,三个容器中
后,三个容器中 的转化率如图中A、B、C三点。下列叙述正确的是
的转化率如图中A、B、C三点。下列叙述正确的是
A.A点延长反应时间,可以提高 的转化率 的转化率 |
| B.A、B两点的压强之比为25∶28 |
| C.容积为cL的容器NOCl的平衡转化率等于80% |
D.容积为aL的容器达到平衡后再投入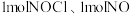 ,平衡不移动 ,平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知: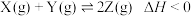 ,400℃时该反应的化学平衡常数K=1。一定条件下,分别在甲、乙、丙3个恒容密闭容器中加入X和Y,反应体系中相关数据如下表:
,400℃时该反应的化学平衡常数K=1。一定条件下,分别在甲、乙、丙3个恒容密闭容器中加入X和Y,反应体系中相关数据如下表:
下列说法正确的是
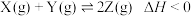 ,400℃时该反应的化学平衡常数K=1。一定条件下,分别在甲、乙、丙3个恒容密闭容器中加入X和Y,反应体系中相关数据如下表:
,400℃时该反应的化学平衡常数K=1。一定条件下,分别在甲、乙、丙3个恒容密闭容器中加入X和Y,反应体系中相关数据如下表:容器 | 温度/℃ | 起始时物质的浓度/ | 10分钟时物质的浓度/ | |
c(X) | c(Y) | c(Z) | ||
甲 | 400 | 1 | 1 | 0.5 |
乙 | T1 | 1 | 1 | 0.4 |
丙 | 400 | 1 | 2 | a |
A.甲中,10分钟时 |
| B.乙中,可能T1<400 |
| C.丙中,a<0.5 |
| D.丙中,达平衡后,保持温度不变,再充入1molX和2molY,X的转化率提高 |
您最近一年使用:0次

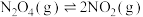
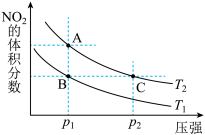
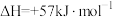 ,在温度为
,在温度为 、
、 时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是