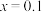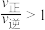氨的催化氧化是硝酸工业中的重要反应: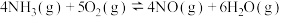
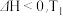 时,将
时,将 和
和 的混合气体充入
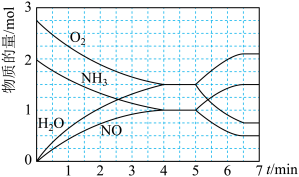
的混合气体充入 恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
下列说法正确的是
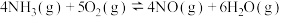
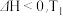 时,将
时,将 和
和 的混合气体充入
的混合气体充入 恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:
恒容密闭容器中发生上述反应,各物质的物质的量随时间变化关系如图所示:下列说法正确的是

A. , ,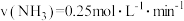 |
| B.加催化剂或缩小容积均可降低反应的活化能,提高反应速率 |
C. 时, 时,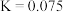 |
D. 时,改变的条件可能为降低温度 时,改变的条件可能为降低温度 |
更新时间:2020-01-24 15:30:42
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某温度下,将2mol X和2mol Y充入2L密闭容器中发生如下反应: 。2min后达到平衡,测得Q的浓度为0.4mol/L,含0.8mol Z。下列叙述
。2min后达到平衡,测得Q的浓度为0.4mol/L,含0.8mol Z。下列叙述不正确 的是
 。2min后达到平衡,测得Q的浓度为0.4mol/L,含0.8mol Z。下列叙述
。2min后达到平衡,测得Q的浓度为0.4mol/L,含0.8mol Z。下列叙述| A.a的值为2 |
| B.在0~2min内,X表示的速率为0.2mol/(L·min) |
| C.Y的转化率为60% |
D.该温度下,化学平衡常数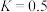 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在2L恒容密闭容器中,通入1mol X、0.6mol Y,发生反应: ,2min末,测得Z、W的浓度分别为
,2min末,测得Z、W的浓度分别为 、
、 ,则下列说法错误的是
,则下列说法错误的是
 ,2min末,测得Z、W的浓度分别为
,2min末,测得Z、W的浓度分别为 、
、 ,则下列说法错误的是
,则下列说法错误的是A. | B.反应过程中混合气体的平均相对分子质量不变 |
C.0~2min内,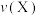 为 为 | D.2min末,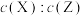 等于8∶3 等于8∶3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】 与稀盐酸反应生成
与稀盐酸反应生成 的量与反应时间的关系如图所示。下列说法错误的是
的量与反应时间的关系如图所示。下列说法错误的是
 与稀盐酸反应生成
与稀盐酸反应生成 的量与反应时间的关系如图所示。下列说法错误的是
的量与反应时间的关系如图所示。下列说法错误的是
A.用HCl和 表示的化学反应速率数值不相同,但所表示的意义相同 表示的化学反应速率数值不相同,但所表示的意义相同 |
B.反应在2~4min内生成 的平均反应速率为0.1 的平均反应速率为0.1  |
C.4min后,反应速率减小的主要原因是 减小 减小 |
| D.反应开始后前4min内温度比浓度对反应速率的影响大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】反应mA(s)+nB(g) pC(g) △H<0,在一定温度下,平衡时B的体积分数与压强变化的关系如图所示,则下列叙述正确的是
pC(g) △H<0,在一定温度下,平衡时B的体积分数与压强变化的关系如图所示,则下列叙述正确的是

①m+n<p ②x点的状态是v正>v逆 ③n>p ④x点比y点的反应速度慢 ⑤若升高温度,该反应的平衡常数增大
 pC(g) △H<0,在一定温度下,平衡时B的体积分数与压强变化的关系如图所示,则下列叙述正确的是
pC(g) △H<0,在一定温度下,平衡时B的体积分数与压强变化的关系如图所示,则下列叙述正确的是
①m+n<p ②x点的状态是v正>v逆 ③n>p ④x点比y点的反应速度慢 ⑤若升高温度,该反应的平衡常数增大
| A.①②④ | B.②④ |
| C.③⑤ | D.①③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在体积可变的密闭容器中投入0.5molCO和0.75mol ,不同条件下发生反应:
,不同条件下发生反应: 。实验测得平衡时
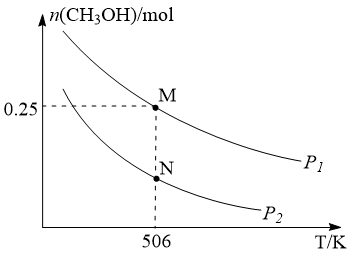
。实验测得平衡时 的物质的量随温度、压强的变化如图所示。下列说法错误的是
的物质的量随温度、压强的变化如图所示。下列说法错误的是
 ,不同条件下发生反应:
,不同条件下发生反应: 。实验测得平衡时
。实验测得平衡时 的物质的量随温度、压强的变化如图所示。下列说法错误的是
的物质的量随温度、压强的变化如图所示。下列说法错误的是
| A.M点CO的转化率为50% |
B.平衡后再加入0.5molCO和0.75mol 重新到达平衡,CO的转化率增大 重新到达平衡,CO的转化率增大 |
C.反应:  |
| D.506K时,若混合气体的总物质的量不再改变,说明反应达到化学平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取10mL 0.lmol/LNa2S2O3溶液和5mL 0. lmol/L Na2S2O3溶液、5mL蒸馏水于两支试管中,然后同时加入10mL 0.1mol/LH2SO4溶液 | 前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 在容积不变的密闭容器中发生反应:N2(g) +3H2(g) 2NH3(g) 向其中通入氩气,反应速率不变 2NH3(g) 向其中通入氩气,反应速率不变 | 化学反应速率不受压强影响 |
| C | 探究温度对化学反应速率的影响 | 将装有NO2和N2O4混合气体的连同球分别浸泡在冰水和热水中2NO2(g)(红棕色) N2O4(g)(无色),△H< 0 N2O4(g)(无色),△H< 0 | 热水中气体颜色浅,冰水中颜色深 |
| D | 探究KI与FeCl3反应的限度 | 取1mL.0.1mol/LKI溶液于试管中,加入5mL0.1mol/L FeCl3溶液,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI与FeCl3的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
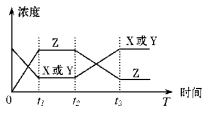
【推荐2】今有反应X(g)+Y(g) 2Z(g) △H<0,若反应开始经t1后达到平衡,又经t2后由于反应条件的改变使平衡破坏,到t3时又达平衡(如图所示),t2~t3曲线变化的原因是
2Z(g) △H<0,若反应开始经t1后达到平衡,又经t2后由于反应条件的改变使平衡破坏,到t3时又达平衡(如图所示),t2~t3曲线变化的原因是
 2Z(g) △H<0,若反应开始经t1后达到平衡,又经t2后由于反应条件的改变使平衡破坏,到t3时又达平衡(如图所示),t2~t3曲线变化的原因是
2Z(g) △H<0,若反应开始经t1后达到平衡,又经t2后由于反应条件的改变使平衡破坏,到t3时又达平衡(如图所示),t2~t3曲线变化的原因是
| A.增大了X或Y的浓度 |
| B.使用了催化剂 |
| C.增加了反应体系的压强 |
| D.升高了反应的温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向10.0mL浓度均为0.1mol/L的 和
和 混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3。
混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3。
① ;
;
②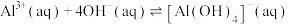 ,298K,
,298K,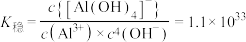 。
。
下列叙述错误的是
 和
和 混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3。
混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3。
①
 ;
;②
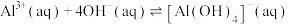 ,298K,
,298K,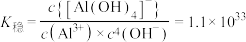 。
。下列叙述错误的是
A.曲线Ⅰ代表 |
B.常温下, |
C.c点铁铝元素主要存在形式为 和 和 |
D.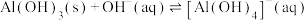 的平衡常数K为 的平衡常数K为 数量级 数量级 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一定温度下,一定体积的密闭容器中有如下平衡:H2(g)+I2(g) 2HI(g)。已知H2和I2的起始浓度均为0.10 mol/L,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均变为0.20 mol/L时,则平衡时H2的浓度(mol/L)是
2HI(g)。已知H2和I2的起始浓度均为0.10 mol/L,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均变为0.20 mol/L时,则平衡时H2的浓度(mol/L)是
 2HI(g)。已知H2和I2的起始浓度均为0.10 mol/L,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均变为0.20 mol/L时,则平衡时H2的浓度(mol/L)是
2HI(g)。已知H2和I2的起始浓度均为0.10 mol/L,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均变为0.20 mol/L时,则平衡时H2的浓度(mol/L)是| A.0.16 | B.0.08 | C.0.06 | D.0.04 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知 A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:
830℃时,向一个2L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4s内A的平均反应速率v(A)=0.005mol/(L·s)。下列说法正确的是( )
温度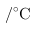 | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| A.4s时c(B)为0.76 mol/L |
| B.830℃达平衡时,A的转化率为80% |
| C.反应达平衡后,升高温度,平衡正向移动 |
| D.1200℃时反应C(g)+D(g)⇌A(g)+B(g)的平衡常数的值为0.4 |
您最近一年使用:0次

 CH3OH(g)
CH3OH(g)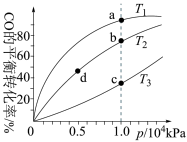
 与
与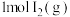 ,发生反应
,发生反应
 (
( 绝对值很小,以下简称“该反应”),体系的自由能G(由体系的焓、熵与温度共同决定:
绝对值很小,以下简称“该反应”),体系的自由能G(由体系的焓、熵与温度共同决定: )随体系中氢气的体积分数
)随体系中氢气的体积分数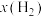 变化的示意图如图2所示,其中P点为曲线最低点。则下列说法中
变化的示意图如图2所示,其中P点为曲线最低点。则下列说法中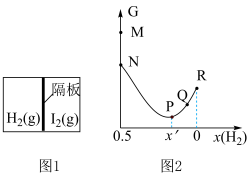
 与
与 混合造成的
混合造成的