1 . 若反应:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-373.4 kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,改变条件,下列说法
N2(g)+2CO2(g) ΔH=-373.4 kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,改变条件,下列说法不正确 的是
 N2(g)+2CO2(g) ΔH=-373.4 kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,改变条件,下列说法
N2(g)+2CO2(g) ΔH=-373.4 kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,改变条件,下列说法| A.分离出CO2,使Q减小,Q<K,因此平衡正向移动 |
| B.分离出N2,使Q减小,Q<K,因此平衡正向移动 |
| C.降低温度,使Q减小,Q<K,因此平衡正向移动 |
| D.加入催化剂可以同等程度增大正、逆反应速率,平衡不移动 |
您最近一年使用:0次
名校
解题方法
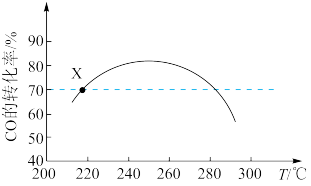
2 . 工业上利用CO和H2合成二甲醚:3CO(g)+3H2(g)  CH3OCH3(g)+CO2(g) ΔH<0;其它条件不变时,相同时间内CO的转化率随温度T的变化情况如图所示。下列说法
CH3OCH3(g)+CO2(g) ΔH<0;其它条件不变时,相同时间内CO的转化率随温度T的变化情况如图所示。下列说法不正确 的是
 CH3OCH3(g)+CO2(g) ΔH<0;其它条件不变时,相同时间内CO的转化率随温度T的变化情况如图所示。下列说法
CH3OCH3(g)+CO2(g) ΔH<0;其它条件不变时,相同时间内CO的转化率随温度T的变化情况如图所示。下列说法
| A.状态X时,v消耗(CO)=v生成(CO) |
| B.一定压强下,升高温度,CO的平衡转化率降低 |
| C.相同温度时,增大压强,可以提高CO的转化率 |
| D.状态X时,选择合适催化剂,可以提高相同时间内CO的转化率 |
您最近一年使用:0次
2022-09-24更新
|
774次组卷
|
8卷引用:北京市顺义区杨镇第一中学2021-2022学年高二上学期期中考试化学试题
北京市顺义区杨镇第一中学2021-2022学年高二上学期期中考试化学试题 贵州省黔西南州金成实验学校2022-2023学年高二上学期9月月考化学试题(已下线)北京市第四中学2022-2023高二上学期期中考试化学试题安徽省舒城晓天中学2022-2023学年高二上学期期中考试化学试题(已下线)第06讲 化学反应速率与化学平衡的图像-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)山东省泰安第一中学2023-2024学年高二上学期10月月考化学试题广东省松湖莞中、深大附中两校2023-2024学年高二上学期10月联考化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二上学期11月期中检测化学试题
名校
3 . 25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,说法错误的是
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
| A.反应达到平衡时,X的转化率为50% |
| B.方程式为X+3Y⇌2Z,平衡常数为1600 |
| C.增大压强使平衡正向方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
您最近一年使用:0次
2021-12-29更新
|
223次组卷
|
11卷引用:河南省济源市第五中学2020-2021学年高二下学期6月月考化学试题
河南省济源市第五中学2020-2021学年高二下学期6月月考化学试题(已下线)第二章 第三节化学平衡(第3课时 化学平衡常数)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)安徽省六安市新安中学2021-2022学年高二上学期期中考试化学试题内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题安徽省六安市新安中学2021-2022学年高二上学期12月月考化学试题河南省范县第一中学等学校2021-2022学年高二上学期联考检测化学试题 广西玉林市市直六所普通高中2021-2022学年高二上学期期中考试理科综合化学试题河南省安阳市滑县实验学校2020-2021学年高二上学期期中考试化学试题(普通班)内蒙古集宁新世纪中学2020-2021学年高二上学期期中考试化学试题(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)四川省泸县第四中学2022-2023学年高二上学期期中考试化学试题
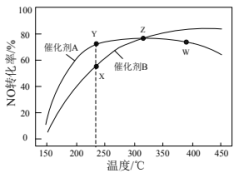
4 . 燃煤电厂锅炉尾气中含有氮氧化物(主要成分NO),可通过主反应4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H=-1627.7kJ·mol-1除去。温度高于300℃时会发生副反应:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-904.7kJ·mol-1。在恒压、反应物起始物质的量之比一定的条件下,反应相同时间,NO的转化率在不同催化剂作用下随温度变化的曲线如图所示。下列有关说法一定正确的是

| A.N2(g)+O2(g)=2NO(g) △H=-180.7kJ·mol-1 |
| B.图中X点所示条件下,反应时间足够长,NO的转化率能达到Y点的值 |
| C.关于X、Y、Z三点,KX=KY,Z点反应达到化学平衡状态 |
| D.图中Z点到W点NO的转化率降低的原因是主反应的平衡逆向移动 |
您最近一年使用:0次
5 . 反应 在密闭容器中进行并达到平衡状态,下列说法或结论正确的是
在密闭容器中进行并达到平衡状态,下列说法或结论正确的是
 在密闭容器中进行并达到平衡状态,下列说法或结论正确的是
在密闭容器中进行并达到平衡状态,下列说法或结论正确的是| A.其他条件不变时,将容器的体积缩小一半,化学平衡不移动 |
| B.保持体积不变,充入少量He,体系压强增大,反应速率增大,化学平衡移动 |
C.反应达到平衡状态时, 正(CO)= 正(CO)= 逆(H2O) 逆(H2O) |
| D.其他条件不变时,适当增加c(S)的质量,化学平衡正向移动 |
您最近一年使用:0次
6 . 已知反应: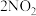 (红棕色)
(红棕色)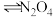 (无色)
(无色)  。将一定量的
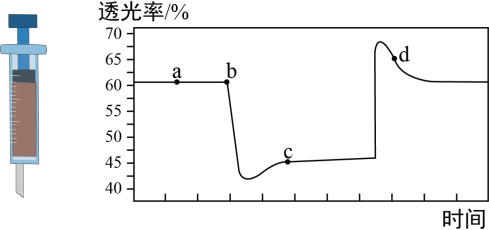
。将一定量的 充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,则透光率越小)。下列说法,正确的是
充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,则透光率越小)。下列说法,正确的是
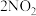 (红棕色)
(红棕色)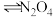 (无色)
(无色)  。将一定量的
。将一定量的 充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,则透光率越小)。下列说法,正确的是
充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,则透光率越小)。下列说法,正确的是
A.a点: (正) (正) (逆) d点: (逆) d点: (正) (正)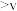 (逆) (逆) |
| B.b点对应的时刻改变的条件是将注射器压缩 |
C.c点与a点相比,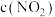 增大, 增大,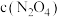 减小 减小 |
| D.若在c点将体系降低温度,其透光率将减小 |
您最近一年使用:0次
2022-08-28更新
|
152次组卷
|
3卷引用:河南省信阳市2021-2022学年高二上学期期中考试化学试题
21-22高三上·江苏·期中
7 . N2O4与NO2能相互转化,N2O4易与水反应生成硝酸和亚硝酸混合物[25°C,Ka(HNO2)=4.6×10-4]。工业上制取四氧化二氮的方法是氨的催化氧化。下列有关说法正确的是
A.四氧化二氮与水反应的离子方程式为:N2O4+H2O=2H+ + + + |
B.恒温恒容条件下,2NO2(g) N2O4(g)平衡体系中再加入少量N2O4, N2O4(g)平衡体系中再加入少量N2O4,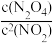 的值不变 的值不变 |
C.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-904kJ·mol-1选用高效催化剂,可降低该反应的ΔH 4NO(g)+6H2O(g) △H=-904kJ·mol-1选用高效催化剂,可降低该反应的ΔH |
D.2NO2(g) N2O4(g),加压一定不能促进N2O4生成 N2O4(g),加压一定不能促进N2O4生成 |
您最近一年使用:0次
名校
8 . 对于平衡体系:mA(g)+nB(g) pC(g)+qD(g) △H<0,下列说法错误的是
pC(g)+qD(g) △H<0,下列说法错误的是
 pC(g)+qD(g) △H<0,下列说法错误的是
pC(g)+qD(g) △H<0,下列说法错误的是| A.若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.58倍,则m+n>p+q |
| B.若反应从正反应开始,达平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| C.若m+n=p+q,则当容器内温度升高时,平衡逆向移动,容器中气体的压强不变 |
| D.若平衡体系中共有气体a mol,再向其中加入b mol B,当重新达到平衡时,气体的总物质的量等于(a+b) mol,则m+n=p+q |
您最近一年使用:0次
2020-09-15更新
|
94次组卷
|
3卷引用:黑龙江省双鸭山市第一中学2021-2022学年高二上学期第一次月考化学试题
名校
9 . 甲醇是一种绿色能源。工业上用 和CO合成
和CO合成 的反应为
的反应为 。将2 mol
。将2 mol  和1 mol CO充入1 L密闭容器中,在恒温恒压条件下,充分反应一段时间后达到平衡状态1。下列说法不正确的是
和1 mol CO充入1 L密闭容器中,在恒温恒压条件下,充分反应一段时间后达到平衡状态1。下列说法不正确的是
 和CO合成
和CO合成 的反应为
的反应为 。将2 mol
。将2 mol  和1 mol CO充入1 L密闭容器中,在恒温恒压条件下,充分反应一段时间后达到平衡状态1。下列说法不正确的是
和1 mol CO充入1 L密闭容器中,在恒温恒压条件下,充分反应一段时间后达到平衡状态1。下列说法不正确的是| A.若反应在恒温恒容条件下进行,平衡时CO的转化率小于平衡状态1的 |
B.容器中CO和 的体积分数之比保持不变不能说明反应达到平衡状态 的体积分数之比保持不变不能说明反应达到平衡状态 |
C.若平衡状态1中再充入a mol  ,达到新平衡时, ,达到新平衡时, 的体积分数比原平衡状态的小 的体积分数比原平衡状态的小 |
D.若平衡状态1中通入 ,达到新平衡时, ,达到新平衡时, 的平衡浓度减小 的平衡浓度减小 |
您最近一年使用:0次
10 . 2021年6月17日,搭载神舟十二号载人飞船的长征二号F遥十二运载火箭成功发射,并顺利完成与天和核心舱对接。火箭采用偏二甲肼(C2H8N2)/N2O4发动机,核心舱电源系统由锂离子蓄电池组以及三结砷化镓(GaAs)太阳电池翼组成。氮化硼(BN)陶瓷基复合材料应用于核心舱电推进系统,碳化硅(SiC)颗粒增强铝基复合材料应用于太阳电池翼伸展机构关键部件,表面处理后镁合金部件应用在核心舱医学样本分析与高微重力科学实验柜中。偏二甲肼(C2H8N2)/N2O4发动机中使用的N2O4存在着N2O4(g)  2NO2(g)平衡。下列说法不正确的是
2NO2(g)平衡。下列说法不正确的是
 2NO2(g)平衡。下列说法不正确的是
2NO2(g)平衡。下列说法不正确的是| A.恒温恒容条件下,若混合气体的颜色保持不变,则该反应达到平衡状态 |
| B.当v (N2O4)正=2 v (NO2)正时,该反应达到平衡状态 |
| C.恒温恒容条件下,达平衡状态后,再充入一定量的N2O4,N2O4转化率将减小 |
| D.该反应在一定条件下能自发进行的原因是∆H>0,∆S>0 |
您最近一年使用:0次



