解题方法
1 . CO2可用于制备CH4、合成气(CO、H2),是CO2资源化利用的重要途径。
(1)CO2甲烷化过程可能发生反应:
i.
ii.
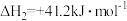
iii.
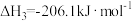
①
___________  。
。
②利用不同催化剂,在一定温度和反应时间条件下,测得产物的生成速率与催化剂的关系如图1.可知有利于制甲烷的催化剂是___________ 。
③压强一定时,按照 投料,发生上述反应,
投料,发生上述反应, 的平衡转化率与温度的关系如图2。
的平衡转化率与温度的关系如图2。
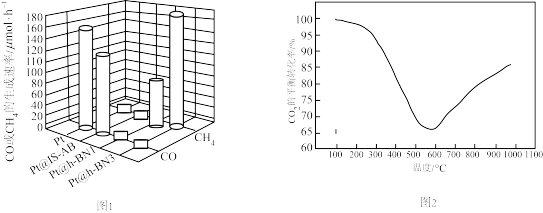
请解释温度高于600℃之后,随着温度升高 转化率增大的原因
转化率增大的原因___________ 。
(2)利用CO、 合成甲醇的反应为
合成甲醇的反应为
 ,向密闭容器中充入1molCO和
,向密闭容器中充入1molCO和 ,发生反应,测得CO的平衡转化率数据与温度、压强的对应关系如下表所示:
,发生反应,测得CO的平衡转化率数据与温度、压强的对应关系如下表所示:
①由此可知,P1_____ P2(填“大于”或“小于”)。有利于提高CO平衡转化率的措施是______ 。
②P2kPa、250℃条件下,反应5min达到平衡,此时H2的物质的量为_____ ,该反应的压强平衡常数Kp=_______ (kPa)2(用分压代替浓度,分压=总压×该组分物质的量分数,用P2的式子表示)。
(1)CO2甲烷化过程可能发生反应:
i.

ii.

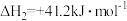
iii.

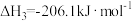
①

 。
。②利用不同催化剂,在一定温度和反应时间条件下,测得产物的生成速率与催化剂的关系如图1.可知有利于制甲烷的催化剂是
③压强一定时,按照
 投料,发生上述反应,
投料,发生上述反应, 的平衡转化率与温度的关系如图2。
的平衡转化率与温度的关系如图2。
请解释温度高于600℃之后,随着温度升高
 转化率增大的原因
转化率增大的原因(2)利用CO、
 合成甲醇的反应为
合成甲醇的反应为
 ,向密闭容器中充入1molCO和
,向密闭容器中充入1molCO和 ,发生反应,测得CO的平衡转化率数据与温度、压强的对应关系如下表所示:
,发生反应,测得CO的平衡转化率数据与温度、压强的对应关系如下表所示:| 温度/℃ 转化率 压强/kPa | 50 | 100 | 150 | 200 | 250 | 300 |
| P1 | 0.82 | 0.70 | 0.34 | 0.12 | 0.04 | 0.02 |
| P2 | 0.90 | 0.86 | 0.76 | 0.48 | 0.20 | 0.10 |
②P2kPa、250℃条件下,反应5min达到平衡,此时H2的物质的量为
您最近一年使用:0次
名校
2 . CO2的资源化利用意义重大,其主要产品——甲醇可用于生产二甲醚,二甲醚在日用化工、制药、农药、染料、涂料等方面有广泛的用途。
该反应体系中涉及以下两个主要反应:
主反应: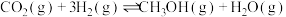
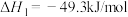
副反应:

(1)已知25℃和101kPa下, 、
、 的燃烧热
的燃烧热 分别为
分别为 、
、 ,
,
 ,则
,则
___________ kJ/mol。
(2)在CO2加氢制甲醇的体系中,下列说法错误的是___________ 。
a.增大初始投料比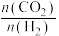 ,有利于提高CO2的转化率
,有利于提高CO2的转化率
b.当气体的平均摩尔质量保持不变时,说明反应体系已达平衡
c.平衡后,压缩容器体积,主反应平衡正向移动,副反应平衡不移动
d.选用合适的催化剂可提高CO2的平衡转化率
(3)不同条件下,相同的时间段内CH3OH的选择性和产率随温度的变化如图。
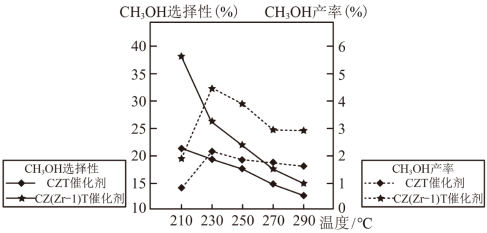
CH3OH选择性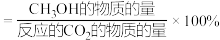
①由图可知,合成甲醇的适宜条件为___________ (填标号)。
A.C2T催化剂 B.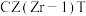 催化剂 C.230℃ D.290℃
催化剂 C.230℃ D.290℃
②在230℃以上,升高温度,CO2的平衡转化率增大,但甲醇的产率降低,原因是___________ 。
(4)在某密闭容器中充入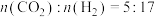 的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。
的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。
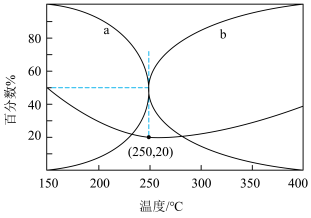
①表示平衡时CH3OH在含碳产物中物质的量百分数的曲线是___________ (填“a”或“b”)。
②250℃时副反应 的Kp=
的Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
该反应体系中涉及以下两个主要反应:
主反应:
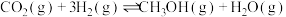
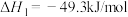
副反应:


(1)已知25℃和101kPa下,
 、
、 的燃烧热
的燃烧热 分别为
分别为 、
、 ,
,
 ,则
,则
(2)在CO2加氢制甲醇的体系中,下列说法错误的是
a.增大初始投料比
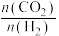 ,有利于提高CO2的转化率
,有利于提高CO2的转化率b.当气体的平均摩尔质量保持不变时,说明反应体系已达平衡
c.平衡后,压缩容器体积,主反应平衡正向移动,副反应平衡不移动
d.选用合适的催化剂可提高CO2的平衡转化率
(3)不同条件下,相同的时间段内CH3OH的选择性和产率随温度的变化如图。

CH3OH选择性
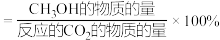
①由图可知,合成甲醇的适宜条件为
A.C2T催化剂 B.
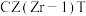 催化剂 C.230℃ D.290℃
催化剂 C.230℃ D.290℃②在230℃以上,升高温度,CO2的平衡转化率增大,但甲醇的产率降低,原因是
(4)在某密闭容器中充入
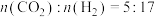 的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。
的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。
①表示平衡时CH3OH在含碳产物中物质的量百分数的曲线是
②250℃时副反应
 的Kp=
的Kp=
您最近一年使用:0次
名校
解题方法
3 . 金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石TiO2 转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H1=172kJ∙mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) △H2=-51kJ∙mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的H 为___________ kJ mol-1, Kp =___________ Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是___________ 。
③对于碳氯化反应:增大压强,平衡___________ 移动(填“向左”“向右”或“不”);温度升高,平衡转化率___________ (填“变大”“变小”或“不变”)。
(2)在1.0 105 Pa ,将TiO2、C、Cl2以物质的量比 1∶2.2∶2 进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
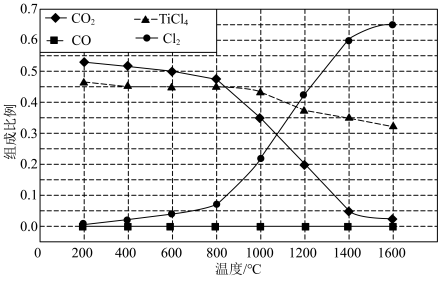
图中显示,在200℃平衡时TiO2 几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是___________ 。
(3)TiO2碳氯化是一个“气—固—固”反应,有利于TiO2 C “固—固”接触的措施是________ 。
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H1=172kJ∙mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) △H2=-51kJ∙mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的H 为
②碳氯化的反应趋势远大于直接氯化,其原因是
③对于碳氯化反应:增大压强,平衡
(2)在1.0 105 Pa ,将TiO2、C、Cl2以物质的量比 1∶2.2∶2 进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。

图中显示,在200℃平衡时TiO2 几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是
(3)TiO2碳氯化是一个“气—固—固”反应,有利于TiO2 C “固—固”接触的措施是
您最近一年使用:0次



