1 . 某化学科研小组研究在其他条件不变时,改变某一条件对反应[可用 表示]化学平衡的影响,得到如图所示图像(图中
表示]化学平衡的影响,得到如图所示图像(图中 表示压强,
表示压强, 表示温度,
表示温度, 表示物质的量,
表示物质的量, 表示平衡转化率,
表示平衡转化率, 表示平衡体积分数):
表示平衡体积分数):
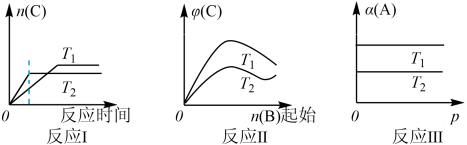
分析图像,回答下列问题:
(1)在反应I中,T1___________ (填“>”“<”或“=”)T2,该正反应为___________ (填“吸热”或“放热”)反应。
(2)在反应Ⅱ中,若此正反应为吸热反应,则T1___________ (填“>”“<”或“=”)T2。
(3)在反应Ⅲ中,a+b___________ c(填“>”“<”或“=”)。
 表示]化学平衡的影响,得到如图所示图像(图中
表示]化学平衡的影响,得到如图所示图像(图中 表示压强,
表示压强, 表示温度,
表示温度, 表示物质的量,
表示物质的量, 表示平衡转化率,
表示平衡转化率, 表示平衡体积分数):
表示平衡体积分数):
分析图像,回答下列问题:
(1)在反应I中,T1
(2)在反应Ⅱ中,若此正反应为吸热反应,则T1
(3)在反应Ⅲ中,a+b
您最近一年使用:0次
2 . 为探究外界条件对反应: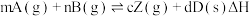 的影响,以A和B物质的量之比为
的影响,以A和B物质的量之比为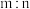 开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
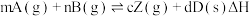 的影响,以A和B物质的量之比为
的影响,以A和B物质的量之比为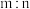 开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
| A.在恒温恒容条件下,向已达到平衡的体系中加入少量A,平衡正向移动,A的百分含量减小 |
B.降低温度, 比 比 减少更多 减少更多 |
| C.不断增加A的投料量,Z的体积分数可能减少 |
D.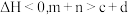 |
您最近一年使用:0次
名校
解题方法
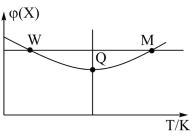
3 . 在2L恒容密闭容器中充入2mol X和1mol Y发生反应
 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是

 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
| A.Q点时,Y的转化率最大 |
| B.W点X的正反应速率等于M点X的正反应速率 |
| C.升高温度,平衡常数增大 |
| D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
您最近一年使用:0次
2023-10-22更新
|
388次组卷
|
3卷引用:福建省福州三中2023-2024学年高二上学期期中考试化学试题
名校
解题方法
4 . 甲醇制烯烃(MTO)是煤制烯烃工艺路线的核心技术。煤制烯烃主要包括煤的气化、液化、烯烃化三个阶段。
(1)煤的液化发生的主要反应之一为
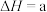 kJ⋅mol
kJ⋅mol ,在不同温度下,K(500°C)
,在不同温度下,K(500°C)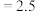 (mol⋅L
(mol⋅L ),K(700°C)
),K(700°C)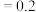 (mol⋅L
(mol⋅L )
)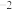 。
。
①
___________ 0(填“>”、“<”、“=”)。
②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内 、CO、
、CO、 物质的量分别为2 mol、1 mol、3 mol,则此时生成
物质的量分别为2 mol、1 mol、3 mol,则此时生成 的速率
的速率___________ 消耗 的速率(填“>”、“<”、“=”)。
的速率(填“>”、“<”、“=”)。
(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
Ⅰ.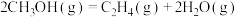
 kJ⋅mol
kJ⋅mol
Ⅱ.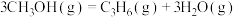
 kJ⋅mol
kJ⋅mol
Ⅲ.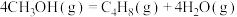
 kJ⋅mol
kJ⋅mol
① 转化为
转化为 的热化学方程式为Ⅳ:
的热化学方程式为Ⅳ: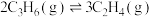
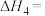
___________ 。
②加入 作为稀释剂,反应Ⅰ中
作为稀释剂,反应Ⅰ中 的产率将
的产率将___________ (填“增大”、“减小”或“不变”)。
(3)为研究不同条件对反应的影响,测得不同温度下平衡时 、
、 和
和 的物质的量分数变化,如图所示:
的物质的量分数变化,如图所示:
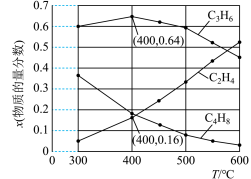
①随着温度的升高, 的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是
的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是___________ 。
②体系总压为0.1 MPa,400℃时反应Ⅳ的平衡常数
___________ 。
(1)煤的液化发生的主要反应之一为

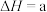 kJ⋅mol
kJ⋅mol ,在不同温度下,K(500°C)
,在不同温度下,K(500°C)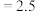 (mol⋅L
(mol⋅L ),K(700°C)
),K(700°C)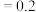 (mol⋅L
(mol⋅L )
)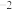 。
。①

②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内
 、CO、
、CO、 物质的量分别为2 mol、1 mol、3 mol,则此时生成
物质的量分别为2 mol、1 mol、3 mol,则此时生成 的速率
的速率 的速率(填“>”、“<”、“=”)。
的速率(填“>”、“<”、“=”)。(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
Ⅰ.
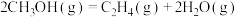
 kJ⋅mol
kJ⋅mol
Ⅱ.
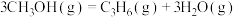
 kJ⋅mol
kJ⋅mol
Ⅲ.
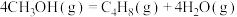
 kJ⋅mol
kJ⋅mol
①
 转化为
转化为 的热化学方程式为Ⅳ:
的热化学方程式为Ⅳ: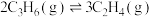
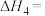
②加入
 作为稀释剂,反应Ⅰ中
作为稀释剂,反应Ⅰ中 的产率将
的产率将(3)为研究不同条件对反应的影响,测得不同温度下平衡时
 、
、 和
和 的物质的量分数变化,如图所示:
的物质的量分数变化,如图所示:
①随着温度的升高,
 的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是
的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是②体系总压为0.1 MPa,400℃时反应Ⅳ的平衡常数

您最近一年使用:0次
名校
解题方法
5 . 下列图示与对应的叙述相符的是
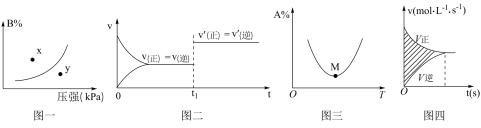

A.图一表示反应:  ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 |
B.图二是可逆反应  的速率时间图像,在 的速率时间图像,在 时刻改变条件一定是加入催化剂 时刻改变条件一定是加入催化剂 |
C.图三表示对于化学反应 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 |
D.图四所示图中的阴影部分面积的含义是( ) ) |
您最近一年使用:0次
2023-10-10更新
|
447次组卷
|
4卷引用:福建省南安市华侨中学2023-2024学年高二上学期10月月考化学试题
6 . 某化学研究小组探究外界条件对化学反应mA(g)+nB(g)⇌pC(g)(m+n≠p)的速率和平衡的影响,图象如图,下列判断正确的是

| A.图d中,曲线a一定增加了催化剂 |
| B.由图b可知,该反应m+n<p |
| C.图c是绝热条件下速率和时间的图象,由此说明该反应吸热 |
| D.由图a可知,T1>T2,该反应的逆反应为放热反应 |
您最近一年使用:0次
2023-08-26更新
|
919次组卷
|
7卷引用:福建省南平市高级中学2022-2023学年高二上学期期中考试化学(选考)试题
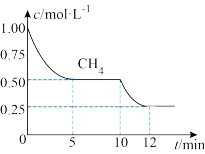
7 . 二甲醚是一种重要的清洁燃料,工业上可以通过 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。
Ⅰ. 分子间脱水制二甲醚
分子间脱水制二甲醚

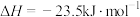 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
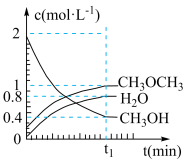
(1) 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡_____ (填“向右”、“向左”或“不发生”)移动,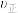 将
将_____ (填“增大”或“减小”)
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为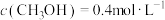 、
、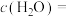
 、
、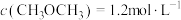 ,此时
,此时
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
Ⅱ.合成气制取二甲醚的原理如下:
反应1:
反应2:
(3)500K时,在2L密闭容器中充入4molCO和8mol ,4min达到平衡,平衡时CO的转化率为80%,且
,4min达到平衡,平衡时CO的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率
_____ ,反应1的平衡常数
_____ (结果需化成最简比)。
(4)由天然气获得合成气过程中可能发生以下反应:

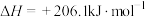
在一密闭容器中进行上述反应,测得 随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。Ⅰ.
 分子间脱水制二甲醚
分子间脱水制二甲醚
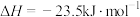 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。 
(1)
 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡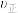 将
将(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为
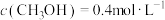 、
、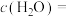
 、
、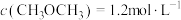 ,此时
,此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。Ⅱ.合成气制取二甲醚的原理如下:
反应1:

反应2:

(3)500K时,在2L密闭容器中充入4molCO和8mol
 ,4min达到平衡,平衡时CO的转化率为80%,且
,4min达到平衡,平衡时CO的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率

(4)由天然气获得合成气过程中可能发生以下反应:

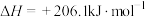
在一密闭容器中进行上述反应,测得
 随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
| A.压缩体积 | B.增大体积 | C.升高温度 | D.加入催化剂 |
您最近一年使用:0次
2023-08-20更新
|
303次组卷
|
2卷引用:福建省宁德市部分一级达标中学2022-2023学年高二上学期11月期中考试化学(C卷)试题
名校
8 . 为探究外界条件对反应: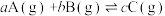 ΔH的影响,以A和B的物质的量之比为a:b开始反应,通过实验得到不同条件下反应达到平衡时A的物质的量分数随温度、压强的变化如图所示。下列判断正确的是
ΔH的影响,以A和B的物质的量之比为a:b开始反应,通过实验得到不同条件下反应达到平衡时A的物质的量分数随温度、压强的变化如图所示。下列判断正确的是

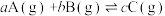 ΔH的影响,以A和B的物质的量之比为a:b开始反应,通过实验得到不同条件下反应达到平衡时A的物质的量分数随温度、压强的变化如图所示。下列判断正确的是
ΔH的影响,以A和B的物质的量之比为a:b开始反应,通过实验得到不同条件下反应达到平衡时A的物质的量分数随温度、压强的变化如图所示。下列判断正确的是
| A.a+b>c |
| B.平衡后增大容器体积,反应会放出热量 |
| C.升高温度,正,逆反应速率都增大,平衡常数也增大 |
| D.平衡后再充入amol A,平衡正向移动,再次达到平衡后,A的物质的量分数减小 |
您最近一年使用:0次
2022-11-14更新
|
175次组卷
|
4卷引用:福建省永泰县城关中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
9 . 在密闭容器中进行反应: ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是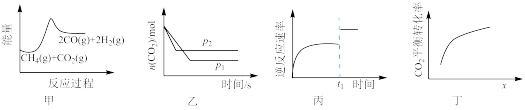
| A.由图甲可知,该反应为吸热反应 |
B.由图乙可知,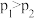 |
C.由图丙可知, 时刻改变的条件可能是加入了催化剂 时刻改变的条件可能是加入了催化剂 |
D.由图丁可知,横坐标 可能是指投料比 可能是指投料比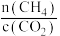 |
您最近一年使用:0次
2022-09-03更新
|
648次组卷
|
10卷引用:福建省泉州市2021-2022学年高二上学期期末教学质量监测化学试题
福建省泉州市2021-2022学年高二上学期期末教学质量监测化学试题福建省三明第一中学2022-2023学年高二上学期中考试化学试题福建省福州市外国语学校2022-2023学年高二上学期12月阶段性测试化学试题福建省厦门外国语学校石狮分校2022-2023学年高二上学期期中考试化学试题福建省福州第三中学2023-2024学年高二上学期1月期末考试化学试题福建省莆田五中2023-2024学年高二上学期第三次月考化学试卷 河南省中原名校2022-2023学年高二上学期第二次联考化学试题广东省惠州市第一中学2022-2023学年高二上学期第一次月考化学试题陕西省榆林市绥德中学2022-2023学年高二上学期第二次阶段性考试化学试题山东省济南市莱钢高级中学2022-2023学年高二上学期期中考试化学试题
名校
10 . 给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡: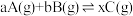 ,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
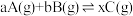 ,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指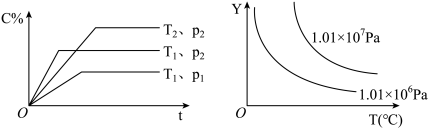
| A.反应物A的百分含量 | B.平衡混合气的总物质的量 | C.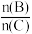 比值 比值 | D.反应物B的平衡转化率 |
您最近一年使用:0次
2022-09-13更新
|
678次组卷
|
4卷引用:福建省厦门第一中学2020-2021学年高二上学期期中考试化学试题



