解题方法
1 . 利用 可消除CO污染或定量测定CO,反应为:
可消除CO污染或定量测定CO,反应为:
完成下列填空:
(1)该反应的平衡常数表达式
___________ 。在2L恒容密闭容器中反应25min后,固体质量减少了6.4g,则0~25min  的平均反应速率为
的平均反应速率为___________ 。
(2)取一定量的 和CO于某密闭容器中,分别在80
和CO于某密闭容器中,分别在80 和100
和100 下进行实验,测得
下进行实验,测得 如下:
如下:
上表中
___________ ,理由是___________ 。根据上表数据可以得出的结论是___________ 。
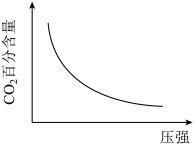
(3)如图所示,300 时
时 的百分含量随着压强的增大而减小,请解释其原因
的百分含量随着压强的增大而减小,请解释其原因___________ 。
(4) 可用高浓度NaOH溶液吸收。
可用高浓度NaOH溶液吸收。
①若4.48L (标准状况)和0.35mol NaOH溶液完全反应,生成的碳酸钠和碳酸氢钠的物质的量之比为
(标准状况)和0.35mol NaOH溶液完全反应,生成的碳酸钠和碳酸氢钠的物质的量之比为___________ 。
②继续通入二氧化碳至溶液中碳酸钠和碳酸氢钠(碳酸氢钠溶液呈碱性)的物质的量之比1∶1,则溶液中各离子浓度大小顺序为___________ 。
③若使碳酸氢钠溶液中 的比值变小,可加入的物质是
的比值变小,可加入的物质是___________ 。
a.通入HCl b.NaOH固体 c.通入 d.
d. 固体
固体
 可消除CO污染或定量测定CO,反应为:
可消除CO污染或定量测定CO,反应为:
完成下列填空:
(1)该反应的平衡常数表达式

 的平均反应速率为
的平均反应速率为(2)取一定量的
 和CO于某密闭容器中,分别在80
和CO于某密闭容器中,分别在80 和100
和100 下进行实验,测得
下进行实验,测得 如下:
如下:| 时间/min 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
80 | 0.50 | 0.37 | 0.26 | 0.18 | 0.12 | 0.12 |
100 | 0.50 | 0.35 | 0.24 | 0.17 | x | 0.15 |
上表中

(3)如图所示,300
 时
时 的百分含量随着压强的增大而减小,请解释其原因
的百分含量随着压强的增大而减小,请解释其原因
(4)
 可用高浓度NaOH溶液吸收。
可用高浓度NaOH溶液吸收。①若4.48L
 (标准状况)和0.35mol NaOH溶液完全反应,生成的碳酸钠和碳酸氢钠的物质的量之比为
(标准状况)和0.35mol NaOH溶液完全反应,生成的碳酸钠和碳酸氢钠的物质的量之比为②继续通入二氧化碳至溶液中碳酸钠和碳酸氢钠(碳酸氢钠溶液呈碱性)的物质的量之比1∶1,则溶液中各离子浓度大小顺序为
③若使碳酸氢钠溶液中
 的比值变小,可加入的物质是
的比值变小,可加入的物质是a.通入HCl b.NaOH固体 c.通入
 d.
d. 固体
固体
您最近一年使用:0次



