名校
1 . 丙烯腈(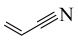 )是一种重要的化工原料,以
)是一种重要的化工原料,以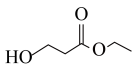 为原料合成丙烯腈的过程如下:
为原料合成丙烯腈的过程如下:

向密闭容器中通入一定量的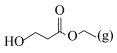 和
和 ,测得平衡时体系中含碳物质(乙醇除外)的物质的量分数[如:丙烯腈的物质的量分数
,测得平衡时体系中含碳物质(乙醇除外)的物质的量分数[如:丙烯腈的物质的量分数 ]随温度的变化如图。下列说法错误的是
]随温度的变化如图。下列说法错误的是
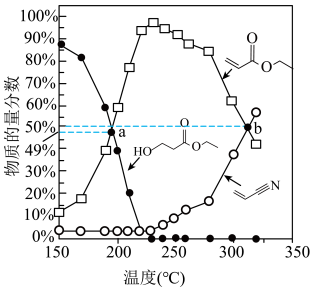
| A.“脱水”反应为吸热反应 |
| B.低于225℃时,“腈化”过程转化率低 |
C.a点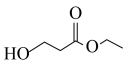 的转化率为51% 的转化率为51% |
D.b点 和 和 的物质的量之比为3:1 的物质的量之比为3:1 |
您最近一年使用:0次
2024-05-24更新
|
190次组卷
|
3卷引用:山东省德州市2024届高三下学期高考适应性练习(二)化学试题
解题方法
2 . 丙烯是重要的化工原料,丙烷直接脱氢制丙烯的相关反应及能量变化如图。
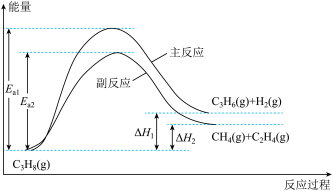
回答下列问题:
(1)主反应的焓变
______ 0(填“>”或“<”);在600℃、1MPa条件下,丙烷脱氢制丙烯反应到达平衡,测得 、
、 的体积分数均为30%,则此时
的体积分数均为30%,则此时 的体积分数为
的体积分数为____________ 。
(2)向密闭容器中充入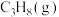 ,发生主反应:
,发生主反应: (忽略副反应的发生)。
(忽略副反应的发生)。
①测得反应速率方程为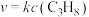 ,k为反应速率常数。已知:
,k为反应速率常数。已知: (R、C为常数,T为温度,Ea为活化能)。实验测得其他条件相同,不同催化剂Cat1、Cat2对k的影响如图甲所示,则催化效能较高的是
(R、C为常数,T为温度,Ea为活化能)。实验测得其他条件相同,不同催化剂Cat1、Cat2对k的影响如图甲所示,则催化效能较高的是______ (填“Catl”或“Cat2”)。
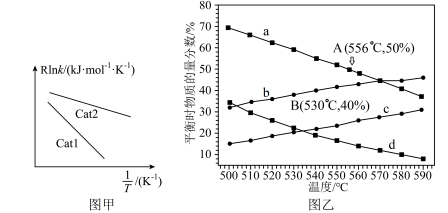
②在100 kPa、10 kPa不同起始压强下达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图乙所示。起始压强为10 kPa,丙烷、丙烯随温度变化的物质的量分数曲线分别是______ 、______ (填代号);A点对应的平衡常数
______ kPa( 为以分压表示的平衡常数);B点丙烷的平衡转化率为
为以分压表示的平衡常数);B点丙烷的平衡转化率为______ 。

回答下列问题:
(1)主反应的焓变

 、
、 的体积分数均为30%,则此时
的体积分数均为30%,则此时 的体积分数为
的体积分数为(2)向密闭容器中充入
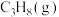 ,发生主反应:
,发生主反应: (忽略副反应的发生)。
(忽略副反应的发生)。①测得反应速率方程为
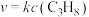 ,k为反应速率常数。已知:
,k为反应速率常数。已知: (R、C为常数,T为温度,Ea为活化能)。实验测得其他条件相同,不同催化剂Cat1、Cat2对k的影响如图甲所示,则催化效能较高的是
(R、C为常数,T为温度,Ea为活化能)。实验测得其他条件相同,不同催化剂Cat1、Cat2对k的影响如图甲所示,则催化效能较高的是
②在100 kPa、10 kPa不同起始压强下达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图乙所示。起始压强为10 kPa,丙烷、丙烯随温度变化的物质的量分数曲线分别是

 为以分压表示的平衡常数);B点丙烷的平衡转化率为
为以分压表示的平衡常数);B点丙烷的平衡转化率为
您最近一年使用:0次
名校
解题方法
3 . 氨是工农业生产中的重要原料,研究氨的合成和转化是一项重要的科研课题。回答下列问题:
(1)已知:工业合成氨合成塔中每产生2molNH3,放出92.2kJ热量,

则1molN-H键断裂吸收的能量为___________ kJ。
(2)在密闭容器中合成氨气,有利于加快反应速率且能提高H2转化率的措施是___________(填字母)
(3)将0.6molN2和0.8molH2充入恒容密闭容器中,在不同温度下,平衡时NH3的体积分数随压强变化的曲线如图。
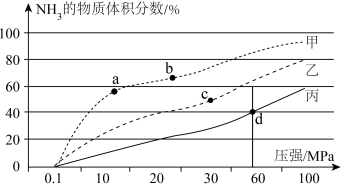
甲、乙、丙中温度从高到低的顺序是___________ 。d点N2的转化率是___________ ,d点Kp=___________ (Kp是以平衡分压表示的平衡常数,平衡分压=平衡时各组分的物质的量分数×总压)。
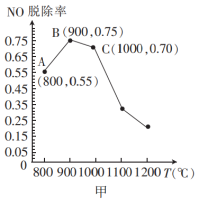
(4)催化氧化法消除NO反应原理为:6NO+4NH3 5N2+6H2O。不同温度条件下,氨气与一氧化氮的物质的量之比为2:1时,得到NO脱除率曲线如图甲所示。脱除NO的最佳温度是
5N2+6H2O。不同温度条件下,氨气与一氧化氮的物质的量之比为2:1时,得到NO脱除率曲线如图甲所示。脱除NO的最佳温度是___________ 。在温度超过1000°C时NO脱除率骤然下降的原因可能是___________ 。
(5)研究发现NH3与NO的反应历程如图乙所示。下列说法正确的是___________(填字母)。

(1)已知:工业合成氨合成塔中每产生2molNH3,放出92.2kJ热量,

则1molN-H键断裂吸收的能量为
(2)在密闭容器中合成氨气,有利于加快反应速率且能提高H2转化率的措施是___________(填字母)
| A.升高反应温度 | B.增大反应的压强 |
| C.及时移走生成的NH3 | D.增加H2的物质的量 |

甲、乙、丙中温度从高到低的顺序是
(4)催化氧化法消除NO反应原理为:6NO+4NH3
 5N2+6H2O。不同温度条件下,氨气与一氧化氮的物质的量之比为2:1时,得到NO脱除率曲线如图甲所示。脱除NO的最佳温度是
5N2+6H2O。不同温度条件下,氨气与一氧化氮的物质的量之比为2:1时,得到NO脱除率曲线如图甲所示。脱除NO的最佳温度是
(5)研究发现NH3与NO的反应历程如图乙所示。下列说法正确的是___________(填字母)。

| A.该反应历程中形成了非极性键和极性键 |
| B.每生成2molN2,转移的电子总数为8NA |
| C.Fe2+能降低总反应的活化能,提高反应速率 |
| D.该反应历程中存在:NO+Fe2+-NH2=Fe2++N2↑+H2O |
您最近一年使用:0次
2023-04-16更新
|
542次组卷
|
4卷引用:化学-2023年高考押题预测卷03(山东卷)(含考试版、全解全析、参考答案、答题卡)
(已下线)化学-2023年高考押题预测卷03(山东卷)(含考试版、全解全析、参考答案、答题卡)广西壮族自治区2023届高三下学期第三次联合调研考试理综化学试题(已下线)山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(原理综合题)2024届四川省泸县第五中学高三上学期一诊模拟考试理综试题
4 . T℃时,向容积为2L的刚性容器中充入1 mol CO2和一定量的H2发生反应:CO2(g)+2H2(g)  HCHO(g) +H2O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始
HCHO(g) +H2O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始 的关系如图所示。已知:初始加入2molH2时,容器内气体的总压强为1.2p kPa。下列说法错误的是
的关系如图所示。已知:初始加入2molH2时,容器内气体的总压强为1.2p kPa。下列说法错误的是

 HCHO(g) +H2O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始
HCHO(g) +H2O(g) ,达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始 的关系如图所示。已知:初始加入2molH2时,容器内气体的总压强为1.2p kPa。下列说法错误的是
的关系如图所示。已知:初始加入2molH2时,容器内气体的总压强为1.2p kPa。下列说法错误的是
A.5 min时反应到达c点, (H2)=0.1 mol·L-1·min-1 (H2)=0.1 mol·L-1·min-1 |
B.随 增大, HCHO的平衡压强不断增大 增大, HCHO的平衡压强不断增大 |
C.b点时反应的平衡常数Kp =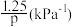 |
| D.c点时,再加入CO2(g)和H2O(g) ,使二者分压均增大0.2p kPa,平衡正向移动 |
您最近一年使用:0次
解题方法
5 . 丙烯腈(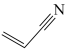 )是一种重要的化工原料,广泛应用在合成纤维、合成橡胶及合成树脂等工业生产中。以3-羟基丙酸乙酯(
)是一种重要的化工原料,广泛应用在合成纤维、合成橡胶及合成树脂等工业生产中。以3-羟基丙酸乙酯( )为原料合成丙烯腈,主要反应过程如下:
)为原料合成丙烯腈,主要反应过程如下:
反应Ⅰ: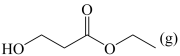
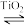
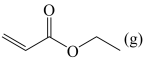


反应Ⅱ: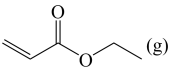 +NH3(g)
+NH3(g)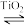
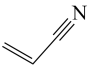 (g)+H2O(g)+
(g)+H2O(g)+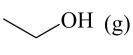

(1)有机物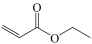 的名称为
的名称为_______ ,反应Ⅰ正反应的活化能_______ 逆反应的活化能(填“大于”或“小于”);反应Ⅱ的反应历程有两步,其中第一步反应的化学方程式为: +NH3(g)
+NH3(g)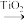
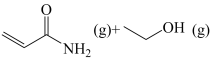 ,则第二步反应的化学方程式为
,则第二步反应的化学方程式为_______ ;实验过程中未检测到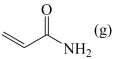 的原因可能为
的原因可能为_______ 。
(2)在盛有催化剂 、压强为200kPa的恒压密闭容器中按体积比2∶15充入
、压强为200kPa的恒压密闭容器中按体积比2∶15充入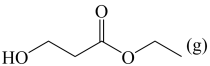 和
和 发生反应,通过实验测得平衡体系中含碳物质(乙醇除外)的物质的量分数随温度的变化如图所示。
发生反应,通过实验测得平衡体系中含碳物质(乙醇除外)的物质的量分数随温度的变化如图所示。
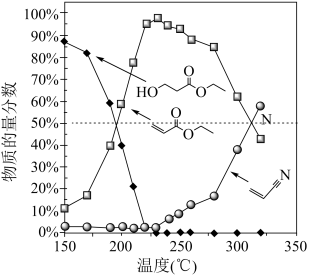
随着温度的升高, (g)的平衡物质的量分数先增大后减小的原因为
(g)的平衡物质的量分数先增大后减小的原因为_______ ,N点对应反应Ⅱ的平衡常数
_______ (x代表物质的量分数)。
(3)在酸性条件下,电解丙烯腈可以制备已二腈 ,则
,则_______ (填“阳极”或“阴极”)产生已二腈,其电极方程式为_______ 。
 )是一种重要的化工原料,广泛应用在合成纤维、合成橡胶及合成树脂等工业生产中。以3-羟基丙酸乙酯(
)是一种重要的化工原料,广泛应用在合成纤维、合成橡胶及合成树脂等工业生产中。以3-羟基丙酸乙酯( )为原料合成丙烯腈,主要反应过程如下:
)为原料合成丙烯腈,主要反应过程如下:反应Ⅰ:

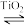



反应Ⅱ:
 +NH3(g)
+NH3(g)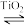
 (g)+H2O(g)+
(g)+H2O(g)+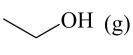

(1)有机物
 的名称为
的名称为 +NH3(g)
+NH3(g)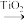
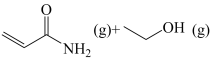 ,则第二步反应的化学方程式为
,则第二步反应的化学方程式为 的原因可能为
的原因可能为(2)在盛有催化剂
 、压强为200kPa的恒压密闭容器中按体积比2∶15充入
、压强为200kPa的恒压密闭容器中按体积比2∶15充入 和
和 发生反应,通过实验测得平衡体系中含碳物质(乙醇除外)的物质的量分数随温度的变化如图所示。
发生反应,通过实验测得平衡体系中含碳物质(乙醇除外)的物质的量分数随温度的变化如图所示。
随着温度的升高,
 (g)的平衡物质的量分数先增大后减小的原因为
(g)的平衡物质的量分数先增大后减小的原因为
(3)在酸性条件下,电解丙烯腈可以制备已二腈
 ,则
,则
您最近一年使用:0次



