1 .
(1)Ⅰ.工业上利用 和
和 合成二甲醚的反应如下:
合成二甲醚的反应如下:
 。
。
温度升高,该化学平衡移动后达到新的平衡, 的产率将
的产率将__________ (填“变大”“变小”或“不变”,下同),混合气体的平均相对分子质量将__________ 。
Ⅱ.某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应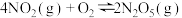
 的影响。
的影响。
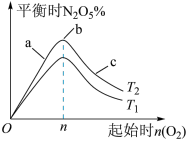
(2)图中 和
和 的关系是
的关系是
________ (填“>”“<”或“=”) 。
。
(3)比较a、b、c三点所处的平衡状态中,反应物 的转化率最大的是
的转化率最大的是__________ (填字母)。
(4)若容器体积为 ,
,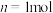 ,
, 的转化率为
的转化率为 ,则此条件下
,则此条件下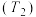 ,反应的平衡常数
,反应的平衡常数
___________ 。
(1)Ⅰ.工业上利用
 和
和 合成二甲醚的反应如下:
合成二甲醚的反应如下:
 。
。温度升高,该化学平衡移动后达到新的平衡,
 的产率将
的产率将Ⅱ.某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应
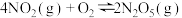
 的影响。
的影响。
(2)图中
 和
和 的关系是
的关系是
 。
。(3)比较a、b、c三点所处的平衡状态中,反应物
 的转化率最大的是
的转化率最大的是(4)若容器体积为
 ,
,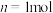 ,
, 的转化率为
的转化率为 ,则此条件下
,则此条件下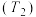 ,反应的平衡常数
,反应的平衡常数
您最近一年使用:0次
14-15高二上·天津和平·期末
名校
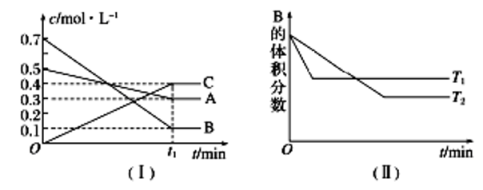
2 . T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为________ ,正反应为_____ (填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有______ (填字母序号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度

根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
您最近一年使用:0次
2018-10-27更新
|
197次组卷
|
9卷引用:2013-2014学年天津市和平区高二上学期期末考试化学试卷
(已下线)2013-2014学年天津市和平区高二上学期期末考试化学试卷湖南省娄底市第四中学2018-2019学年高二上学期10月月考化学试题安徽省砀山县第二中学2019-2020学年高二10月月考化学试题重庆市北碚区2019-2020学年高二11月联合性测试化学试题(已下线)第10单元 化学反应速率与化学平衡(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷四川省苍溪实验中学校2020-2021学年高二上学期期中质量检测化学试题湖北省黄冈麻城市第二中学2021届高三上学期第一次质量检测化学试题新疆自治区阿克苏地区库车县伊西哈拉镇中学2018-2019学年高二上学期期中考试化学试题湖南省株洲市茶陵县第三中学2019-2020学年高二上学期期中考试化学(选考)试题
10-11高三上·北京·阶段练习
3 . 25 C时,在体积为2 L的密闭容器中,气态物质A、B、C的物质的量n随时间1的变化如图1所示,已知反应达到平衡后,降低温度,A的转化率将增大。

(1)根据图1数据。写出该反应的化学方程式:_____________ ;此反应的平衡常数表达式为K=_________ ,从反应开始到第一次平衡时的平均速率v(A)为________ 。
(2)在5~7min内,若K值不变,则此处曲线变化的原因是_________ 。
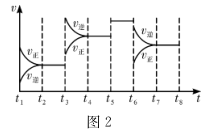
(3)图2表示此反应的反应速率v和时间t的关系,t3、t5、t6时刻各改变一个且互不相同的条件,各阶段的平衡常数如下表所示。K1、K2、K3、K4之间的关系为________ (用“>”“<”或“=”连接)。A的转化率最大的一段时间是___________ 。

(1)根据图1数据。写出该反应的化学方程式:
(2)在5~7min内,若K值不变,则此处曲线变化的原因是
(3)图2表示此反应的反应速率v和时间t的关系,t3、t5、t6时刻各改变一个且互不相同的条件,各阶段的平衡常数如下表所示。K1、K2、K3、K4之间的关系为
| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K1 | K2 | K3 | K4 |

您最近一年使用:0次
2018-02-06更新
|
362次组卷
|
7卷引用:2010年北京市高三上学期起点考试化学试题
(已下线)2010年北京市高三上学期起点考试化学试题(已下线)2014届高考化学二轮复习 专题6化学反应速率和化学平衡练习卷(已下线)2014年高中化学二轮创新训练上 专题6化学反应速率和化学平衡练习卷湖南省长沙市长郡中学2017-2018学年度高二第一学期期末考试化学试题陕西省子洲中学2019-2020学年高二下学期第一次月考化学试题【全国百强校】吉林省实验中学2018-2019学年高二上学期期中考试化学试题福建省永安市第一中学2020-2021学年高二上学期第一次月考化学试题
名校
4 . 汽车尾气(主要成分为NOx和CO)已成为主要的空气污染物来源之一,有发生光化学烟雾污染的潜在危险。
(1)某小组同学为研究光化学烟雾的形成进行了模拟实验。测得烟雾的主要成分为CxHy(烃)、NO、NO2、O3、PAN (CH3COOONO2),各种物质的相对浓度随时间的变化如右图。根据图中数据,下列推论最不合理的是_____ 。(填选项序号字母)

a.NO的消失的速率比CxHy快 b.NO生成NO2
c.CxHy及NO2可以生成PAN及O3 d.O3生成PAN
(2)一定条件下,将2 mol NO与2 mol O2置于恒容密闭容器中发生反应2NO(g)+O2(g) 2NO2(g),下列可判断反应达平衡的是
2NO2(g),下列可判断反应达平衡的是_____ 。(填选项序号字母)
a.体系压强保持不变 b.混合气体密度保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗2 mol NO同时生成2 mol NO2
(3)高温下N2和O2发生N2(g)+O2(g) 2NO(g)反应,是导致汽车尾气中含有NO的原因之一。
2NO(g)反应,是导致汽车尾气中含有NO的原因之一。
①右图是T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图象,据此判断反应N2(g)+O2(g) 2NO(g)为
2NO(g)为_____ (填“吸热”或“放热”)反应。

②2000℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则此刻反应的平衡常数K=_____ 。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为_____ 。

③汽车净化装置里装有含Pd化合物的催化剂,气体在催化剂表面吸附与解吸作用的机理如右图所示。写出其变化的总化学反应方程式:_____ 。
(4)为减少汽车尾气中NOx的排放,常采用CxHy(烃)催化还原NOx消除氮氧化物的污染。
例如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2
若16 g CH4还原NO2至N2,共放出热量867 kJ,则ΔH2=_____ 。若用标准状况下4.48 L CH4还原NO2至N2,共转移的电子总数为_____ (阿伏伽德罗常数的值用NA表示)。
(1)某小组同学为研究光化学烟雾的形成进行了模拟实验。测得烟雾的主要成分为CxHy(烃)、NO、NO2、O3、PAN (CH3COOONO2),各种物质的相对浓度随时间的变化如右图。根据图中数据,下列推论最不合理的是

a.NO的消失的速率比CxHy快 b.NO生成NO2
c.CxHy及NO2可以生成PAN及O3 d.O3生成PAN
(2)一定条件下,将2 mol NO与2 mol O2置于恒容密闭容器中发生反应2NO(g)+O2(g)
 2NO2(g),下列可判断反应达平衡的是
2NO2(g),下列可判断反应达平衡的是a.体系压强保持不变 b.混合气体密度保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗2 mol NO同时生成2 mol NO2
(3)高温下N2和O2发生N2(g)+O2(g)
 2NO(g)反应,是导致汽车尾气中含有NO的原因之一。
2NO(g)反应,是导致汽车尾气中含有NO的原因之一。①右图是T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图象,据此判断反应N2(g)+O2(g)
 2NO(g)为
2NO(g)为
②2000℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则此刻反应的平衡常数K=

③汽车净化装置里装有含Pd化合物的催化剂,气体在催化剂表面吸附与解吸作用的机理如右图所示。写出其变化的总化学反应方程式:
(4)为减少汽车尾气中NOx的排放,常采用CxHy(烃)催化还原NOx消除氮氧化物的污染。
例如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2
若16 g CH4还原NO2至N2,共放出热量867 kJ,则ΔH2=
您最近一年使用:0次
2018-01-25更新
|
1001次组卷
|
3卷引用:四川省资阳市高中2018届高三第二次诊断性考试理科综合化学试题
四川省资阳市高中2018届高三第二次诊断性考试理科综合化学试题【全国百强校】四川省棠湖中学2019届高三二诊模拟理综-化学试题(已下线)练习2 盖斯定律与化学反应热的计算-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)
2014高二·全国·专题练习
解题方法
5 . 可逆反应:aA(气)+bB(气)  cC(气)+dD(气) △H=Q,试根据图回答
cC(气)+dD(气) △H=Q,试根据图回答
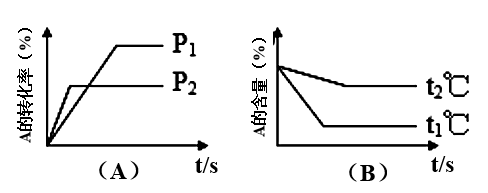
(1)压强P1比P2______ (填大、小)
(2)体积(a+b)比(c+d)____ (填大、小)
(3)温度t1℃比t2℃______ (填高、低)
(4)Q值是______ (填正、负)
 cC(气)+dD(气) △H=Q,试根据图回答
cC(气)+dD(气) △H=Q,试根据图回答
(1)压强P1比P2
(2)体积(a+b)比(c+d)
(3)温度t1℃比t2℃
(4)Q值是
您最近一年使用:0次
2018-01-01更新
|
256次组卷
|
4卷引用:2014年高中化学苏教版选修四专题2 反应速率与化学平衡练习卷
(已下线)2014年高中化学苏教版选修四专题2 反应速率与化学平衡练习卷河北省唐山市滦县二中2017-2018学年高二期中考试化学(理)试卷甘肃省宁县第二中学2020-2021学年高二上学期期末考试化学试题福建省清流一中2017-2018学年高二上学期第二阶段(期中)考试化学(理)试题
名校
6 . 工业上常用CO和H2合成甲醇,反应方程式为:
CO (g) +2H2(g) CH3OH (g) △H,在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,达到平衡时CH3OH的体积分数(V%)与n(H2):n(CO)的关系如图1所示。
CH3OH (g) △H,在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,达到平衡时CH3OH的体积分数(V%)与n(H2):n(CO)的关系如图1所示。
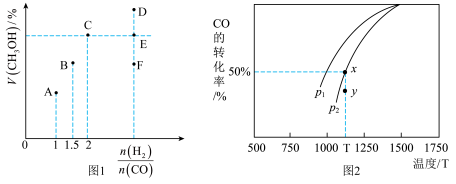
(1)当起始n (H2):n(CO) =2,经过5min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率v(H2)=____ 。若此时再向容器中加入0.15 mol CO (g)和0.05 mol CH3OH (g),达新平衡时H2的转化率将_______ (选填“增大”、“减小”或“不变”)。
(2)当起始n (H2):n(CO) =3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的_____ 点(选填“D”、“E”或“F”)。
(3)由图2可知该反应的△H_____ 0(选填“>”、“<”或“=”,下同),压强pl____ p2;当压强为p2时,在y点:v(正)____ v(逆)。
CO (g) +2H2(g)
 CH3OH (g) △H,在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,达到平衡时CH3OH的体积分数(V%)与n(H2):n(CO)的关系如图1所示。
CH3OH (g) △H,在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,达到平衡时CH3OH的体积分数(V%)与n(H2):n(CO)的关系如图1所示。
(1)当起始n (H2):n(CO) =2,经过5min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率v(H2)=
(2)当起始n (H2):n(CO) =3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的
(3)由图2可知该反应的△H
您最近一年使用:0次
2017-10-22更新
|
621次组卷
|
6卷引用:河南省八市2017-2018学年高二上学期第一次质量检测化学试题



