2024高三·全国·专题练习
解题方法
1 . Ⅰ.H2S与CH4重整,不但可以消除污染,还可以制氢。主要反应为 ;ΔH>0。
;ΔH>0。
(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应: ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。_______ 、_______ (填化学式)。
(3)M点对应温度下,H2S的转化率是_______ 。
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。_______ (填“A”“B”或“C”)组图像。三组图像中,C组图像中平均反应速率最低的可能原因是_______ 。
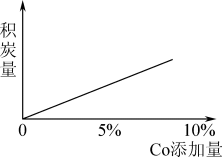
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为____ 。
 ;ΔH>0。
;ΔH>0。(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
| A.混合气体密度不变 |
| B.容器内压强不变 |
| C.2v正(H2S)=v逆(CS2) |
| D.CH4与H2的物质的量分数之比保持不变 |
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应:
 ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。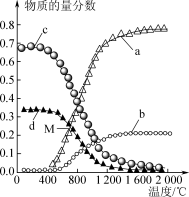
(3)M点对应温度下,H2S的转化率是
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。
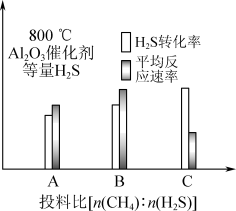
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为
您最近一年使用:0次
2024高三下·全国·专题练习
2 . 二甲醚(DME)在制药、燃料、农药等化学工业中有许多独特的用途。工业上常用合成气制备二甲醚的主要原理如下:①CO(g)+2H2(g)⇌CH3OH(g) ΔH1<0
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2<0
③CO(g)+H2O(g)⇌H2(g)+CO2(g) ΔH3<0
在催化剂作用下,发生上述3个反应,CO的转化率、CH3OH和CO2的产率和随温度变化关系如图1所示。总压分别为100kPa、10kPa时,平衡体系中CO和CH3OCH3(g)的物质的量分数随温度变化关系如图2所示
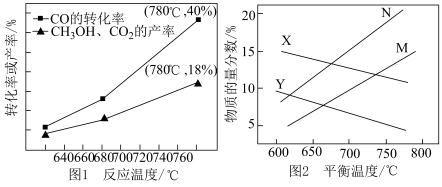
回答下列问题:
(1)图1中CO的转化率随温度升高而上升的原因是_______ 。
(2)图1中780℃时,CH3OCH3的选择性为_______ 。(CH3OCH3选择性= )
)
(3)能提高CH3OCH3选择性的最关键因素是_______ 。
(4)100kPa时,CO和CH3OCH3的物质的量分数随温度变化关系的曲线分别是_______ 、_______ 。
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2<0
③CO(g)+H2O(g)⇌H2(g)+CO2(g) ΔH3<0
在催化剂作用下,发生上述3个反应,CO的转化率、CH3OH和CO2的产率和随温度变化关系如图1所示。总压分别为100kPa、10kPa时,平衡体系中CO和CH3OCH3(g)的物质的量分数随温度变化关系如图2所示

回答下列问题:
(1)图1中CO的转化率随温度升高而上升的原因是
(2)图1中780℃时,CH3OCH3的选择性为
 )
)(3)能提高CH3OCH3选择性的最关键因素是
(4)100kPa时,CO和CH3OCH3的物质的量分数随温度变化关系的曲线分别是
您最近一年使用:0次
2024高三下·全国·专题练习
3 . 空气中CO2含量的控制和CO2资源利用具有重要意义。
已知25℃、101 下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
I.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH1=+41.2kJ·mol-1
II.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-49kJ·mol-1
III.CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH3=-165kJ·mol-1
向刚性密闭容器中通入一定量CO2和H2,发生反应I和反应II,温度对 和CH3OH的物质的量分数影响如图所示。
和CH3OH的物质的量分数影响如图所示。
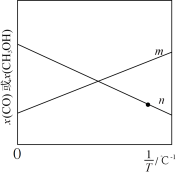
图中表示 物质的量分数的为
物质的量分数的为_______ (填“m”或“n”);为提高CH3OH的选择性,可采取的措施有_______ (写出1条即可)。
已知25℃、101
 下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:I.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH1=+41.2kJ·mol-1
II.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-49kJ·mol-1
III.CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH3=-165kJ·mol-1
向刚性密闭容器中通入一定量CO2和H2,发生反应I和反应II,温度对
 和CH3OH的物质的量分数影响如图所示。
和CH3OH的物质的量分数影响如图所示。
图中表示
 物质的量分数的为
物质的量分数的为
您最近一年使用:0次
2023高三·全国·专题练习
4 . 回答下列问题
(1)已知合成氨反应: N2(g)+
N2(g)+ H2(g)
H2(g)  NH3(g) ΔH=-46.2 kJ·mol-1,标准平衡常数Kθ=
NH3(g) ΔH=-46.2 kJ·mol-1,标准平衡常数Kθ= ,其中pθ为标准压强,p(NH3)、p(N2)、p(H2)为各组分的平衡分压,如p(NH3)=x(NH3)p,p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。若往一密闭容器中加入的N2、H2起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则Kθ=
,其中pθ为标准压强,p(NH3)、p(N2)、p(H2)为各组分的平衡分压,如p(NH3)=x(NH3)p,p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。若往一密闭容器中加入的N2、H2起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则Kθ=___________ (用含w的最简式表示)。
(2)某科研小组向一恒容密闭容器中通入2 mol CH4、2 mol CO2,控制适当条件使其发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH=+247 kJ·mol-1,测出CH4的某个平衡物理量X随着温度、压强的变化如图所示
2CO(g)+2H2(g) ΔH=+247 kJ·mol-1,测出CH4的某个平衡物理量X随着温度、压强的变化如图所示

①X___________ (填“能”或“不能”)表示平衡体系中CH4的体积分数;p1、p2的大小关系为___________ ,b点浓度商Qc与对应温度下的平衡常数K相比,较大的是___________
②若容器容积为2 L,a点时c(CH4)=0.4 mol·L-1,则相应温度下的平衡常数K=___________
(1)已知合成氨反应:
 N2(g)+
N2(g)+ H2(g)
H2(g)  NH3(g) ΔH=-46.2 kJ·mol-1,标准平衡常数Kθ=
NH3(g) ΔH=-46.2 kJ·mol-1,标准平衡常数Kθ= ,其中pθ为标准压强,p(NH3)、p(N2)、p(H2)为各组分的平衡分压,如p(NH3)=x(NH3)p,p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。若往一密闭容器中加入的N2、H2起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则Kθ=
,其中pθ为标准压强,p(NH3)、p(N2)、p(H2)为各组分的平衡分压,如p(NH3)=x(NH3)p,p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。若往一密闭容器中加入的N2、H2起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则Kθ=(2)某科研小组向一恒容密闭容器中通入2 mol CH4、2 mol CO2,控制适当条件使其发生反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH=+247 kJ·mol-1,测出CH4的某个平衡物理量X随着温度、压强的变化如图所示
2CO(g)+2H2(g) ΔH=+247 kJ·mol-1,测出CH4的某个平衡物理量X随着温度、压强的变化如图所示
①X
②若容器容积为2 L,a点时c(CH4)=0.4 mol·L-1,则相应温度下的平衡常数K=
您最近一年使用:0次



