名校
1 . 甲醇是重要的化工原料,发展前景广阔。研究表明, 加氢可以合成甲醇,反应如下:
加氢可以合成甲醇,反应如下: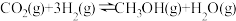
(1)反应的平衡常数表达式为K=___________ 。
(2)有利于提高平衡时 转化率的措施有
转化率的措施有___________ (填字母)。
a.使用催化剂
b.加压
c.增大 和H2的初始投料比
和H2的初始投料比
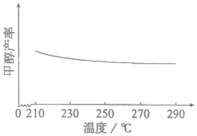
(3)研究温度对甲醇产率的影响时发现,在210~290℃,保持原料气中 和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
___________ 0(填“>”“=”或“<”),依据是___________ 。
 加氢可以合成甲醇,反应如下:
加氢可以合成甲醇,反应如下: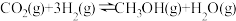
(1)反应的平衡常数表达式为K=
(2)有利于提高平衡时
 转化率的措施有
转化率的措施有a.使用催化剂
b.加压
c.增大
 和H2的初始投料比
和H2的初始投料比(3)研究温度对甲醇产率的影响时发现,在210~290℃,保持原料气中
 和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的

您最近一年使用:0次
2021-12-02更新
|
797次组卷
|
4卷引用:人教2019版选择性必修一第二章 第二节 化学平衡 课后习题
2 . 在容积不变的密闭容器中,一定量的SO2、O2发生反应: 。温度分别为t1和t2时,
。温度分别为t1和t2时, 的体积分数随时间的变化如图。该反应的
的体积分数随时间的变化如图。该反应的
___________ 0(填“>”“<”或“=”,下同);若t1、t2时该反应的化学平衡常数分别为K1、K2,则K1___________ K2。

 。温度分别为t1和t2时,
。温度分别为t1和t2时, 的体积分数随时间的变化如图。该反应的
的体积分数随时间的变化如图。该反应的

您最近一年使用:0次
2021高三·全国·专题练习
3 . 某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将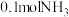 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
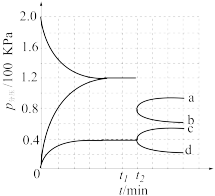
 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________ ;
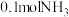 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是
您最近一年使用:0次
20-21高一下·湖北省直辖县级单位·阶段练习
4 . (Ⅰ)在密闭容器中进行下列反应:M(g)+N(g) R(g)+2L(?),此反应规律符合如图图象:
R(g)+2L(?),此反应规律符合如图图象:
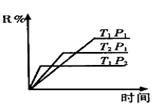
(1)T1___________ T2,正反应的△H___________ 0(填“>”、“<”或“=”,下同)
(2)P1___________ P2,L为___________ (填“固态”或“液态”或“气态”)
(Ⅱ)在密闭容器中进行下列反应:CO2(g)+C(s) 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?
(1)增加C(s),平衡___________ (填“正向移动、逆向移动、不移动”,下同)。
(2)减小密闭容器容积,保持温度不变,则平衡___________ ,c(CO)___________ (填“增大、减小、不变”)
(3)通入N2,保持密闭容器容积和温度不变,则平衡___________ 。
(4)保持密闭容器容积不变,升高温度,则平衡___________ 。
 R(g)+2L(?),此反应规律符合如图图象:
R(g)+2L(?),此反应规律符合如图图象:
(1)T1
(2)P1
(Ⅱ)在密闭容器中进行下列反应:CO2(g)+C(s)
 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?(1)增加C(s),平衡
(2)减小密闭容器容积,保持温度不变,则平衡
(3)通入N2,保持密闭容器容积和温度不变,则平衡
(4)保持密闭容器容积不变,升高温度,则平衡
您最近一年使用:0次
2021高三·全国·专题练习
5 . 二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。回答下列问题:
(1)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
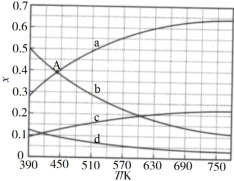
图中,表示C2H4、CO2变化的曲线分别是___ 、___ 。CO2催化加氢合成C2H4反应的ΔH___ 0(填“大于”或“小于”)。
(2)根据图中点A(440K,0.39),计算该温度时反应的平衡常数Kp=___ (MPa)−3(列出计算式。以分压表示,分压=总压×物质的量分数)。
(1)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。

图中,表示C2H4、CO2变化的曲线分别是
(2)根据图中点A(440K,0.39),计算该温度时反应的平衡常数Kp=
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
6 . 醛类物质的用途广泛。如,甲醛蒸气可对空气消毒、甲醛溶液可用于生物标本的防腐等;脂肪醛类一般具有麻醉、催眠作用等。回答下列问题:
利用乙二醛(OHC—CHO)催化氧化法合成乙醛酸的反应原理为:2OHC—CHO(aq)+O2(g) 2OHC—COOH(aq)
2OHC—COOH(aq)
可能发生副反应有:2OHC—COOH(aq)+O2(g) 2H2C2O4(草酸)
2H2C2O4(草酸)
在反应瓶内加入含1molOHC—CHO(乙二醛)的反应液2L,加热至45~60℃,通入氧气并保持氧气压强为0.12MPa,反应3h达平衡状态,得到的混合液中含0.84molOHC—COOH(乙醛酸),0.12molH2C2O4(草酸),0.04molOHC—CHO(乙二醛)(溶液体积变化可忽略不计)。
(1)草酸的平均生成速率为___ mol·L-1·h-1。
(2)通过化学反应原理分析,增大压强有利于加快反应速率,对于乙二醛的转化率的影响是__ (填“增大”或“减小”)。
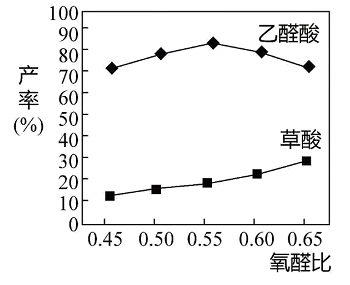
(3)如图所示为起始时氧醛比[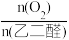 ]对乙醛酸产率的影响,则选择最佳氧醛比为
]对乙醛酸产率的影响,则选择最佳氧醛比为___ 。
利用乙二醛(OHC—CHO)催化氧化法合成乙醛酸的反应原理为:2OHC—CHO(aq)+O2(g)
 2OHC—COOH(aq)
2OHC—COOH(aq)可能发生副反应有:2OHC—COOH(aq)+O2(g)
 2H2C2O4(草酸)
2H2C2O4(草酸)在反应瓶内加入含1molOHC—CHO(乙二醛)的反应液2L,加热至45~60℃,通入氧气并保持氧气压强为0.12MPa,反应3h达平衡状态,得到的混合液中含0.84molOHC—COOH(乙醛酸),0.12molH2C2O4(草酸),0.04molOHC—CHO(乙二醛)(溶液体积变化可忽略不计)。
(1)草酸的平均生成速率为
(2)通过化学反应原理分析,增大压强有利于加快反应速率,对于乙二醛的转化率的影响是
(3)如图所示为起始时氧醛比[
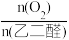 ]对乙醛酸产率的影响,则选择最佳氧醛比为
]对乙醛酸产率的影响,则选择最佳氧醛比为
您最近一年使用:0次
20-21高二下·山东淄博·期中
7 . 在一定条件下,可逆反应mA B+C变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况。
B+C变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况。
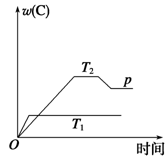
(1)该反应的逆反应为___________ (填“吸热”或“放热”)反应。
(2)若A、B、C均为气体,则m___________ 2(填“大于”、“等于”或“小于”)。
(3)若m=2,则A的状态为___________ 。
(4)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,则平衡向___________ (填“正向移动”、“逆向移动” 或“不移动”)。
(5)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡向___________ (填“正向移动”、“逆向移动” 或“不移动”)。
 B+C变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况。
B+C变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况。
(1)该反应的逆反应为
(2)若A、B、C均为气体,则m
(3)若m=2,则A的状态为
(4)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,则平衡向
(5)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡向
您最近一年使用:0次
2021高三·全国·专题练习
8 . 一定量的CO2与足量的C在恒压密闭容器中发生反应:C(s)+CO2(g)=2CO(g) ΔH=+173 kJ·mol-1,若压强为p kPa,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:

(1)650 ℃时CO2的平衡转化率为___________ 。
(2)t1 ℃时平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数);该温度下达平衡后若再充入等物质的量的CO和CO2气体,则平衡___________ (填“正向”“逆向”或“不”)移动,原因是___________ 。

(1)650 ℃时CO2的平衡转化率为
(2)t1 ℃时平衡常数Kp=
您最近一年使用:0次
2021-05-07更新
|
670次组卷
|
5卷引用:小题29 化学平衡的相关计算——备战2021年高考化学经典小题考前必刷(全国通用)
(已下线)小题29 化学平衡的相关计算——备战2021年高考化学经典小题考前必刷(全国通用)江苏省扬州市高邮市临泽中学2021-2022学年高二9月阶段测试化学试卷江苏省高邮市临泽镇高中2021-2022学年高二上学期9月阶段测试化学试题甘肃省酒泉市玉门油田第一中学2022-2023学年高二上学期期中考试化学试题浙江省金华市江南中学等两校2022-2023学年高二上学期12月阶段测试化学试题
2021·吉林延边·模拟预测
名校
解题方法
9 . CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。请回答下列问题:
I.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
(1)达到平衡时,反应a,b对比:CO2的体积分数φ(a)_______ φ(b)(填“>”、“<”或“=”))。
(2)下列能说明反应a达到平衡状态的是_______ (填字母)。
A.v正(CO2)=3v逆(H2)
B.混合气体的平均摩尔质量不再改变
C.c(CH3OH)=c(H2O)
D.容器内压强不再改变
II.我国科学家研究了不同反应温度对含碳产物组成的影响。
已知:反应1:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH<0
反应2:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0
在密闭容器中通入3mol的的H2和1mol的CO2,分别在1MPa和10MPa下进行反应。实验中对平衡体系组成的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4的影响如图所示。
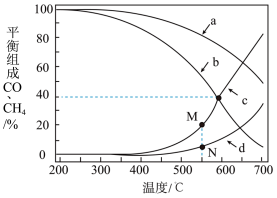
(3)1MPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是_______ 和_______ 。M点平衡组成含量高于N点的原因是_______ 。
(4)图中当CH4和CO平衡组成均为40%时,若容器的体积为1L,该温度下反应1的平衡常数K的值为_______ 。
III.在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的的CO和H2,发生反应CO(g)+2H2(g) ⇌ CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。
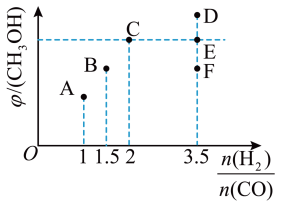
(5)当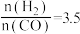 时,达到平衡后,CH3OH的体积分数可能是图象中的
时,达到平衡后,CH3OH的体积分数可能是图象中的_______ (填“D”、“E”或“F”)点。
(6) =
=_______ 时,CH3OH的体积分数最大。
I.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
| CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应a(恒温恒容) | 1 | 3 | 0 | 0 |
| 反应b(绝热恒容) | 0 | 0 | 1 | 1 |
(2)下列能说明反应a达到平衡状态的是
A.v正(CO2)=3v逆(H2)
B.混合气体的平均摩尔质量不再改变
C.c(CH3OH)=c(H2O)
D.容器内压强不再改变
II.我国科学家研究了不同反应温度对含碳产物组成的影响。
已知:反应1:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH<0
反应2:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0
在密闭容器中通入3mol的的H2和1mol的CO2,分别在1MPa和10MPa下进行反应。实验中对平衡体系组成的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4的影响如图所示。

(3)1MPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是
(4)图中当CH4和CO平衡组成均为40%时,若容器的体积为1L,该温度下反应1的平衡常数K的值为
III.在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的的CO和H2,发生反应CO(g)+2H2(g) ⇌ CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。

(5)当
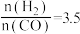 时,达到平衡后,CH3OH的体积分数可能是图象中的
时,达到平衡后,CH3OH的体积分数可能是图象中的(6)
 =
=
您最近一年使用:0次
2021-03-04更新
|
819次组卷
|
4卷引用:第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测
(已下线)第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测江苏省扬州中学2021-2022学年高二上学期期中考试化学试题吉林省延边州2021届高三下学期教学质量检测(2月底) 理综化学试题(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)
2020高三·全国·专题练习
10 . 反应为CO(g)+2H2(g)⇌CH3OH(g) ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
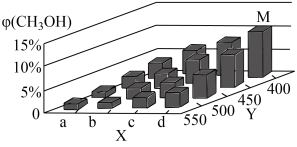
①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为________ 。
②X轴上a点的数值比b点________ (填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是____________________________________________ 。

①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为
②X轴上a点的数值比b点
您最近一年使用:0次



