CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。请回答下列问题:
I.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
(1)达到平衡时,反应a,b对比:CO2的体积分数φ(a)_______ φ(b)(填“>”、“<”或“=”))。
(2)下列能说明反应a达到平衡状态的是_______ (填字母)。
A.v正(CO2)=3v逆(H2)
B.混合气体的平均摩尔质量不再改变
C.c(CH3OH)=c(H2O)
D.容器内压强不再改变
II.我国科学家研究了不同反应温度对含碳产物组成的影响。
已知:反应1:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH<0
反应2:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0
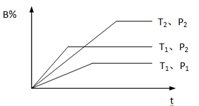
在密闭容器中通入3mol的的H2和1mol的CO2,分别在1MPa和10MPa下进行反应。实验中对平衡体系组成的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4的影响如图所示。
(3)1MPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是_______ 和_______ 。M点平衡组成含量高于N点的原因是_______ 。
(4)图中当CH4和CO平衡组成均为40%时,若容器的体积为1L,该温度下反应1的平衡常数K的值为_______ 。
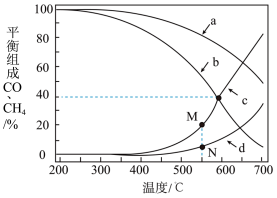
III.在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的的CO和H2,发生反应CO(g)+2H2(g) ⇌ CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。
(5)当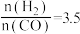 时,达到平衡后,CH3OH的体积分数可能是图象中的
时,达到平衡后,CH3OH的体积分数可能是图象中的_______ (填“D”、“E”或“F”)点。
(6) =
=_______ 时,CH3OH的体积分数最大。
I.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
| CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应a(恒温恒容) | 1 | 3 | 0 | 0 |
| 反应b(绝热恒容) | 0 | 0 | 1 | 1 |
(2)下列能说明反应a达到平衡状态的是
A.v正(CO2)=3v逆(H2)
B.混合气体的平均摩尔质量不再改变
C.c(CH3OH)=c(H2O)
D.容器内压强不再改变
II.我国科学家研究了不同反应温度对含碳产物组成的影响。
已知:反应1:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH<0
反应2:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0
在密闭容器中通入3mol的的H2和1mol的CO2,分别在1MPa和10MPa下进行反应。实验中对平衡体系组成的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4的影响如图所示。

(3)1MPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是
(4)图中当CH4和CO平衡组成均为40%时,若容器的体积为1L,该温度下反应1的平衡常数K的值为
III.在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的的CO和H2,发生反应CO(g)+2H2(g) ⇌ CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。

(5)当
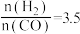 时,达到平衡后,CH3OH的体积分数可能是图象中的
时,达到平衡后,CH3OH的体积分数可能是图象中的(6)
 =
=
2021·吉林延边·模拟预测 查看更多[4]
吉林省延边州2021届高三下学期教学质量检测(2月底) 理综化学试题(已下线)第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测江苏省扬州中学2021-2022学年高二上学期期中考试化学试题(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)
更新时间:2021-03-04 23:37:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为______ (填“吸热”或“放热”)反应,且m+n______ (填“>”“=”或“<”)p。
(2)减压使容器体积增大时,A的质量分数________ 。(填“增大”“减小”或“不变”,下同)
(3)若容积不变加入B,则A的转化率__________ ,B的转化率________ 。
(4)若升高温度,则平衡时B、C的浓度之比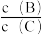 将
将________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量______________________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的逆反应为
(2)减压使容器体积增大时,A的质量分数
(3)若容积不变加入B,则A的转化率
(4)若升高温度,则平衡时B、C的浓度之比
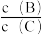 将
将(5)若加入催化剂,平衡时气体混合物的总物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】25℃时,50mL0.10mol·L-1醋酸中存在下述平衡:CH3COOH⇌CH3COO-+H+,请回答以下问题:
(1)加入少量冰醋酸,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”);
(2)加入一定量蒸馏水,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”),c(OH-)将___________ (填“增大”“减小”或“不变”);
(3)加入20mL0.10mol·L-1NaCl溶液,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”)。
(1)加入少量冰醋酸,平衡将
(2)加入一定量蒸馏水,平衡将
(3)加入20mL0.10mol·L-1NaCl溶液,平衡将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验探究1
(1)实验原理: (血红色)
(血红色)
(2)实验步骤:
Ⅰ.小烧杯中加入约 蒸馏水,再滴入5滴
蒸馏水,再滴入5滴 溶液、5滴
溶液、5滴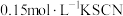 溶液,用玻璃棒搅拌,使其充分混合,将混合均匀的溶液平均注入
溶液,用玻璃棒搅拌,使其充分混合,将混合均匀的溶液平均注入 三支试管中。
三支试管中。
向试管a中滴入5滴 溶液,向试管
溶液,向试管 中滴入5滴
中滴入5滴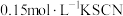 溶液,观察并记录实验现象,与试管
溶液,观察并记录实验现象,与试管 进行对比,完成下表:
进行对比,完成下表:
Ⅱ.继续向上述两支试管中分别加入少量铁粉,观察并记录实验现象,完成下表:
(1)实验原理:
 (血红色)
(血红色)(2)实验步骤:
Ⅰ.小烧杯中加入约
 蒸馏水,再滴入5滴
蒸馏水,再滴入5滴 溶液、5滴
溶液、5滴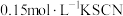 溶液,用玻璃棒搅拌,使其充分混合,将混合均匀的溶液平均注入
溶液,用玻璃棒搅拌,使其充分混合,将混合均匀的溶液平均注入 三支试管中。
三支试管中。向试管a中滴入5滴
 溶液,向试管
溶液,向试管 中滴入5滴
中滴入5滴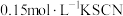 溶液,观察并记录实验现象,与试管
溶液,观察并记录实验现象,与试管 进行对比,完成下表:
进行对比,完成下表:| 实验编号 | 滴加试剂 | 实验现象 | 平衡移动方向 |
 | 5滴 溶液 溶液 | 溶液颜色 | 向 |
 | 5滴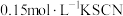 溶液 溶液 | 溶液颜色 | 向 |
 | 不加试剂,对照 |
| 实验编号 | 滴加试剂 | 实验现象 | 平衡移动方向 |
 | 加入少量铁粉 | 溶液颜色 | 向 |
 | 加入少量铁粉 | 溶液颜色 | 向 |
 | 不加试剂,对照 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】合成氨是人类科学技术发展史上的一项重大突破,诺贝尔化学奖曾三次授予与合成氨有关的研究。以下是关于合成氨的有关问题,请回答:
 N2(g)+
N2(g)+  H2(g)
H2(g)  NH3(g) ΔH(298K)= -46.2kJ· mol-l
NH3(g) ΔH(298K)= -46.2kJ· mol-l
在Fe催化剂作用下的反应历程为(*表示吸附态)
化学吸附: N2(g) →2N*; H2(g)→2H*;
表面反应: N*+ H* NH*; NH*+ H*
NH*; NH*+ H* NH2*; NH2* + H*
NH2*; NH2* + H* NH3*
NH3*
脱附: NH3* NH3(g)
NH3(g)
其中,N2的吸附分解反应活化能高、速率小,决定了合成氨的整体反应速率。
(1)平衡后,若想提高H2的转化率,可以采取的措施有 _______。
(2)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应: N2(g) + 3H2(g)  2NH3(g) ΔH = - 92.4kJ·mol-1, 请完成下列问题:
2NH3(g) ΔH = - 92.4kJ·mol-1, 请完成下列问题:
①试比较K1、K2的大小,K1_______ K2 (填“>”、“<”或“=”)
②400℃时,反应2NH3(g) N2(g) + 3H2(g)的化学平衡常数为
N2(g) + 3H2(g)的化学平衡常数为_______ 。当NH3、N2和H2的物质的量分别为2mol、a mol和1mol时,v(N2)正=v(N2)逆。a=_______ 。
(3)关于合成氨工艺的理解,正确的是_______
(4)实际生产中,常用工艺条件: Fe 作催化剂,控制温度500℃,压强3.0×105Pa,原料中N2和H2物质的量之比为1:2.8。分析说明原料气中N2过量的理由有哪些? _______
 N2(g)+
N2(g)+  H2(g)
H2(g)  NH3(g) ΔH(298K)= -46.2kJ· mol-l
NH3(g) ΔH(298K)= -46.2kJ· mol-l在Fe催化剂作用下的反应历程为(*表示吸附态)
化学吸附: N2(g) →2N*; H2(g)→2H*;
表面反应: N*+ H*
 NH*; NH*+ H*
NH*; NH*+ H* NH2*; NH2* + H*
NH2*; NH2* + H* NH3*
NH3*脱附: NH3*
 NH3(g)
NH3(g)其中,N2的吸附分解反应活化能高、速率小,决定了合成氨的整体反应速率。
(1)平衡后,若想提高H2的转化率,可以采取的措施有 _______。
| A.加入催化剂 | B.增大容器体积 |
| C.降低反应体系的温度 | D.加入一定量N2 |
 2NH3(g) ΔH = - 92.4kJ·mol-1, 请完成下列问题:
2NH3(g) ΔH = - 92.4kJ·mol-1, 请完成下列问题:| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②400℃时,反应2NH3(g)
 N2(g) + 3H2(g)的化学平衡常数为
N2(g) + 3H2(g)的化学平衡常数为(3)关于合成氨工艺的理解,正确的是_______
| A.控制温度(500℃) 远高于室温,是为了保证尽可能高的平衡转化率和快的反应速率 |
| B.当温度压强一定时,在原料气(N2 和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率 |
| C.基于NH3有较强的分子间作用力,可将其液化,不断将液氨移去,利于反应正向进行 |
| D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气需经过净化处理,以防止催化剂中毒和安全事故发生 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)如图为1 mol NO2(g)和1 mol CO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。

已知E1=134 kJ·mol-1,E2=368 kJ·mol-1(E1、E2为反应的活化能)。若在反应体系中加入催化剂,化学反应速率增大,则E1、ΔH的变化分别是________ 、________ (填“增大”“减小”或“不变”)。写出该反应的热化学方程式:________________________ 。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。

该反应的ΔH________ (填“>”或“<”)0。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是________________________________ 。
(3)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOx,可以消除氮氧化物的污染。已知:
①CH4(g)+2NO2(g)= N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1
②2NO2(g)N2O4(g) ΔH=-56.9 kJ·mol-1
③H2O(g)= H2O(l) ΔH=-44 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(l)的热化学方程式:________________________ 。
(1)如图为1 mol NO2(g)和1 mol CO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。

已知E1=134 kJ·mol-1,E2=368 kJ·mol-1(E1、E2为反应的活化能)。若在反应体系中加入催化剂,化学反应速率增大,则E1、ΔH的变化分别是
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。

该反应的ΔH
(3)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOx,可以消除氮氧化物的污染。已知:
①CH4(g)+2NO2(g)= N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1
②2NO2(g)N2O4(g) ΔH=-56.9 kJ·mol-1
③H2O(g)= H2O(l) ΔH=-44 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(l)的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】一定条件下,反应室(容积恒定为2 L)中有反应:A(g)+2B(g)=C(g)。
(1)能说明上述反应达到平衡状态的是________ (填字母,下同)。
A.反应中A与B的物质的量浓度之比为1∶2
B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化
D.2v正(A)=v逆(B)
(2)1 mol A(g)与2 mol B(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:
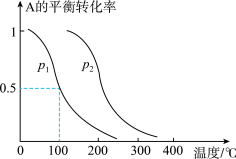
①p1________ (填“<”、“>”或“=”,下同)p2,正反应的ΔH________ 0。
②下列措施中一定能使c(C)/c(A)增大的是________ 。
A.升高温度 B.恒温恒容再充入A
C.恒温恒容再充入B D.恒温恒容再充入1 mol C
(3)100 ℃时将1 mol A和2 mol B通入反应室,保持温度不变,10 min末C(g)的浓度为0.05 mol·L-1,则10 min末B的转化率为________ ,此时v正_______ v逆(填“<”、“>”或“=”)。
(1)能说明上述反应达到平衡状态的是
A.反应中A与B的物质的量浓度之比为1∶2
B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化
D.2v正(A)=v逆(B)
(2)1 mol A(g)与2 mol B(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:

①p1
②下列措施中一定能使c(C)/c(A)增大的是
A.升高温度 B.恒温恒容再充入A
C.恒温恒容再充入B D.恒温恒容再充入1 mol C
(3)100 ℃时将1 mol A和2 mol B通入反应室,保持温度不变,10 min末C(g)的浓度为0.05 mol·L-1,则10 min末B的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)⇌5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5 固体的2L恒容密闭容器中通入2mol CO,测得CO的体积分数 (CO)随时间t变化曲线如图。
(CO)随时间t变化曲线如图。
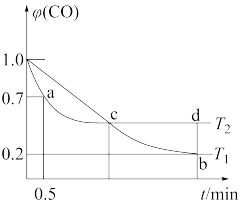
(1)此反应的平衡常数表达式____________ 。
(2)到a点时表示的化学反应速率v(CO)=____________ 。
(3)b点时CO的转化率____________ 。
(4)Kb_______ Kd(填“大于”“小于”或“等于”),原因是_______________ 。
(5)此反应的ΔH________ 0(填“大于”“小于”或“等于”)。
 (CO)随时间t变化曲线如图。
(CO)随时间t变化曲线如图。
(1)此反应的平衡常数表达式
(2)到a点时表示的化学反应速率v(CO)=
(3)b点时CO的转化率
(4)Kb
(5)此反应的ΔH
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氨是化肥工业和化工生产的主要原料,工业合成氨使用的氢气主要来自合成气( ,
, 混合气体)。回答下列问题:
混合气体)。回答下列问题:
(1)合成氨的热化学方程式为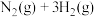


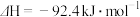 ,升高温度,合成氨反应的平衡常数
,升高温度,合成氨反应的平衡常数_______ (填“增大”“不变”或“减小”)。理论上,为了增大平衡时 的转化率,可采取的措施是
的转化率,可采取的措施是_____ (填字母)。
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物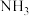
(2)合成氨的原料 可通过反应
可通过反应

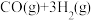
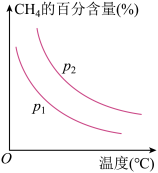
 来获取,已知该反应中,当初始混合气中的
来获取,已知该反应中,当初始混合气中的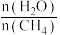 恒定时,温度、压强对平衡混合气中
恒定时,温度、压强对平衡混合气中 的百分含量的影响如图所示:
的百分含量的影响如图所示:
图中两条曲线表示压强的关系是:
________  (填“>”“<”或“=”下同),
(填“>”“<”或“=”下同),
________ 0。
(3) 的另外一个反应为
的另外一个反应为

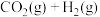
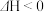 ,一定条件下,反应达到平衡后,采取
,一定条件下,反应达到平衡后,采取______________ 措施可提高 的转化率。
的转化率。
 ,
, 混合气体)。回答下列问题:
混合气体)。回答下列问题:(1)合成氨的热化学方程式为
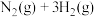


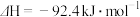 ,升高温度,合成氨反应的平衡常数
,升高温度,合成氨反应的平衡常数 的转化率,可采取的措施是
的转化率,可采取的措施是a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物
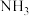
(2)合成氨的原料
 可通过反应
可通过反应

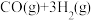
 来获取,已知该反应中,当初始混合气中的
来获取,已知该反应中,当初始混合气中的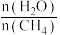 恒定时,温度、压强对平衡混合气中
恒定时,温度、压强对平衡混合气中 的百分含量的影响如图所示:
的百分含量的影响如图所示:图中两条曲线表示压强的关系是:

 (填“>”“<”或“=”下同),
(填“>”“<”或“=”下同),

(3)
 的另外一个反应为
的另外一个反应为

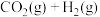
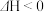 ,一定条件下,反应达到平衡后,采取
,一定条件下,反应达到平衡后,采取 的转化率。
的转化率。
您最近一年使用:0次