某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将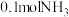 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
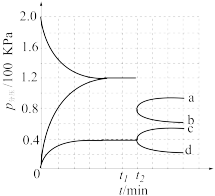
 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________ ;
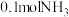 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是
2021高三·全国·专题练习 查看更多[1]
(已下线)专题09 化学反应原理-【微专题·大素养】备战2022年高考化学讲透提分要点
更新时间:2021/11/18 20:41:36
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】回答下列问题
(1)能够使化学平衡移动的因素有________ 、________ 、________ 。
(2)可逆反应A(g)+2B(g) 2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡______ 移动(填正向、逆向、不),B的转化率_______ , v(正) ________ 。(填增大、减小、不变)。
(1)能够使化学平衡移动的因素有
(2)可逆反应A(g)+2B(g)
 2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】镧镍合金是一种良好的储氢材料,向体积恒定的密闭容器中充入氢气发生如下反应:LaNi5(s) + 3H2(g)  LaNi5H6(s) ∆H<0,H2的平衡转化率与其初始充入物质的量(n)、反应温度(T)的关系如图1所示;一定温度下,容器内的压强(p)随时间(t)的变化关系如图2所示。
LaNi5H6(s) ∆H<0,H2的平衡转化率与其初始充入物质的量(n)、反应温度(T)的关系如图1所示;一定温度下,容器内的压强(p)随时间(t)的变化关系如图2所示。
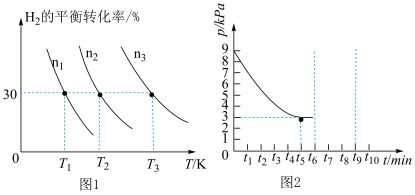
(1)图1中H2初始充入量由大到小的是___________ 。
(2)若保持温度不变,在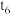 时刻将容器的容积压缩至原来的一半,并在
时刻将容器的容积压缩至原来的一半,并在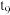 时刻达到平衡。请在图2中画出相应的变化曲线
时刻达到平衡。请在图2中画出相应的变化曲线________ 。
 LaNi5H6(s) ∆H<0,H2的平衡转化率与其初始充入物质的量(n)、反应温度(T)的关系如图1所示;一定温度下,容器内的压强(p)随时间(t)的变化关系如图2所示。
LaNi5H6(s) ∆H<0,H2的平衡转化率与其初始充入物质的量(n)、反应温度(T)的关系如图1所示;一定温度下,容器内的压强(p)随时间(t)的变化关系如图2所示。
(1)图1中H2初始充入量由大到小的是
(2)若保持温度不变,在
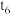 时刻将容器的容积压缩至原来的一半,并在
时刻将容器的容积压缩至原来的一半,并在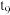 时刻达到平衡。请在图2中画出相应的变化曲线
时刻达到平衡。请在图2中画出相应的变化曲线
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在密闭容器中,使2molN2和6 mol H2混合发生下列反应:N2(g)+3H2(g)⇌2NH3(g) ΔH<0。
(1)当反应达到平衡时,N2和H2的浓度比是_______ ;N2和H2的转化率比是_______ 。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量_______ ,密度_______ (填“变大”、“变小”或“不变”)。
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将_______ (填“正向”、“逆向”或“不”)移动。
(1)当反应达到平衡时,N2和H2的浓度比是
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】运用化学反应原理研究化学反应有重要意义。
(1)硫酸生产中, 催化氧化生成
催化氧化生成 ,
, ,混合体系中
,混合体系中 的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。
的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。
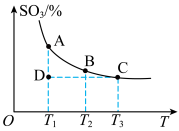
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡___________ (填“向左“向右”或“不”)移动。
②若反应进行到状态D时,
___________ (填“>”“<”或“=”) 。
。
(2)课本里介绍的合成氨技术叫哈伯法: ,应用此法反应达到平衡时反应物的转化率不高。
,应用此法反应达到平衡时反应物的转化率不高。
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是___________ (填字母)。
A.使用更高效的催化剂 B.升高温度
C.及时分离出氨 D.充入氮气,增大氮气的浓度(保持容器体积不变)
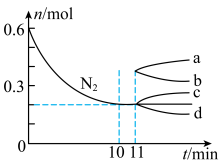
②若在某温度下,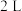 的密闭容器中发生合成氨的反应,下图表示
的密闭容器中发生合成氨的反应,下图表示 的物质的量随时间的变化曲线。从第
的物质的量随时间的变化曲线。从第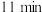 起,压缩容器的体积为
起,压缩容器的体积为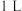 ,则
,则 的变化曲线为
的变化曲线为___________ (填字母)。
(1)硫酸生产中,
 催化氧化生成
催化氧化生成 ,
, ,混合体系中
,混合体系中 的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。
的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡
②若反应进行到状态D时,

 。
。(2)课本里介绍的合成氨技术叫哈伯法:
 ,应用此法反应达到平衡时反应物的转化率不高。
,应用此法反应达到平衡时反应物的转化率不高。①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是
A.使用更高效的催化剂 B.升高温度
C.及时分离出氨 D.充入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下,
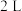 的密闭容器中发生合成氨的反应,下图表示
的密闭容器中发生合成氨的反应,下图表示 的物质的量随时间的变化曲线。从第
的物质的量随时间的变化曲线。从第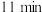 起,压缩容器的体积为
起,压缩容器的体积为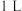 ,则
,则 的变化曲线为
的变化曲线为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】二氧化碳的转化和利用成为实现“碳达峰”、“碳中和”的重要研究课题。回答下列问题:
(1)利用CO2和H2可生产乙烯。相关热化学方程式为:
反应I:2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
反应II:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
某催化剂作用下,在容积为2.0L的恒容密闭容器中充入lmolCO2和3molH2,体系中主要发生上述反应I和反应II两个竞争反应。反应进行tmin时测得两种烃的物质的量随温度的变化如图所示,该催化剂在840℃时主要选择反应________ (填“I”或“II”);840℃之后,C2H4产量下降的原因是_______ 。

520℃时,0~tmin内用氢气表示反应II的平均反应速率:υ(H2)=_______ mol/(L·min)(用含t的代数式表示)。
(2)利用工业废气CO2制甲醇,发生反应III:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
①上述反应自发的条件是________ 。
②在aL密闭容器中,充入不同氢碳比的原料气体,控制温度600K,发生反应III,请在图中画出CH3OH在混合气体中的平衡体积分数随氢碳比递增的变化趋势_________ 。

③一定条件下,将1molCO2和1molH2置于恒容密闭容器中,发生反应III。下列能说明反应达到平衡状态的是_________ 。
A.混合气体的密度保持不变
B.CO2的消耗速率与H2O的消耗速率相等
C.CO2的体积分数保持不变
D.混合气体的平均相对分子质量保持不变
(1)利用CO2和H2可生产乙烯。相关热化学方程式为:
反应I:2CO2(g)+6H2(g)
 CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1反应II:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1某催化剂作用下,在容积为2.0L的恒容密闭容器中充入lmolCO2和3molH2,体系中主要发生上述反应I和反应II两个竞争反应。反应进行tmin时测得两种烃的物质的量随温度的变化如图所示,该催化剂在840℃时主要选择反应

520℃时,0~tmin内用氢气表示反应II的平均反应速率:υ(H2)=
(2)利用工业废气CO2制甲醇,发生反应III:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。①上述反应自发的条件是
②在aL密闭容器中,充入不同氢碳比的原料气体,控制温度600K,发生反应III,请在图中画出CH3OH在混合气体中的平衡体积分数随氢碳比递增的变化趋势

③一定条件下,将1molCO2和1molH2置于恒容密闭容器中,发生反应III。下列能说明反应达到平衡状态的是
A.混合气体的密度保持不变
B.CO2的消耗速率与H2O的消耗速率相等
C.CO2的体积分数保持不变
D.混合气体的平均相对分子质量保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】甲醇是一种重要的试剂,氢气和二氧化碳在一定条件下可合成甲醇:CO2(g)+3H2 (g)  CH3 OH(g)+H2O(g),在密闭容器中充入3mol氢气和1mol二氧化碳,测得混合气体中甲醇的体积分数与温度的关系如图A所示:
CH3 OH(g)+H2O(g),在密闭容器中充入3mol氢气和1mol二氧化碳,测得混合气体中甲醇的体积分数与温度的关系如图A所示:
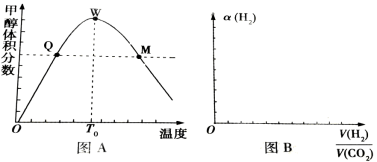
试回答下列问题:
(1)该反应是______ (填“放热”或“吸热”)反应。该反应平衡常数的表达式是:______ ,为了降低合成甲醇的成本可采用的措施是______ (任意写一条合理的建议)
(2)解释0~T0内,甲醇的体积分数变化趋势:______________________ 。
(3)氢气在Q点的转化率______ (填“大于”、“小于”或“等于”,下同)氢气在W点的转化率;其它条件相同,甲醇在Q点的正反应速率______ 甲醇在M点的正反应速率。
(4)图B表示氢气转化率α(H2)与投料比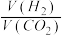 的关系,请在图B中画出两条变化曲线并标出曲线对应的条件,两条曲线对应的条件分别为:一条曲线对应的压强是1.01×105Pa;另一条曲线对应的压强是3.03×105Pa(其它条件相同)
的关系,请在图B中画出两条变化曲线并标出曲线对应的条件,两条曲线对应的条件分别为:一条曲线对应的压强是1.01×105Pa;另一条曲线对应的压强是3.03×105Pa(其它条件相同)___________ .
 CH3 OH(g)+H2O(g),在密闭容器中充入3mol氢气和1mol二氧化碳,测得混合气体中甲醇的体积分数与温度的关系如图A所示:
CH3 OH(g)+H2O(g),在密闭容器中充入3mol氢气和1mol二氧化碳,测得混合气体中甲醇的体积分数与温度的关系如图A所示:
试回答下列问题:
(1)该反应是
(2)解释0~T0内,甲醇的体积分数变化趋势:
(3)氢气在Q点的转化率
(4)图B表示氢气转化率α(H2)与投料比
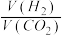 的关系,请在图B中画出两条变化曲线并标出曲线对应的条件,两条曲线对应的条件分别为:一条曲线对应的压强是1.01×105Pa;另一条曲线对应的压强是3.03×105Pa(其它条件相同)
的关系,请在图B中画出两条变化曲线并标出曲线对应的条件,两条曲线对应的条件分别为:一条曲线对应的压强是1.01×105Pa;另一条曲线对应的压强是3.03×105Pa(其它条件相同)
您最近一年使用:0次



