解题方法
1 . 下列有关化学反应原理的说法中正确的是( )
| A.需要加热的反应都是非自发反应,不需要加热的反应都是自发反应 |
| B.反应2CO(g)=C(s)+O2(g) ∆H>0,则不能自发进行 |
| C.Ksp小的强电解质,其溶解度一定也小 |
| D.若反应可以自发,则该反应的速率一定较快 |
您最近一年使用:0次
20-21高二上·全国·课时练习
名校
解题方法
2 . 对于化学反应能否自发进行,下列说法中错误的是( )
| A.若∆H<0,∆S>0,任何温度下都能自发进行 |
| B.若∆H>0,∆S<0,任何温度下都不能自发进行 |
| C.需要加热才能够进行的过程肯定不是自发过程 |
| D.非自发过程在一定条件下可能变成自发过程 |
您最近一年使用:0次
20-21高二上·全国·课时练习
解题方法
3 . 下列说法不正确的是( )
| A.NH4NO3溶于水吸热,所以其溶解于水不是自发过程 |
| B.同一种物质气态时熵值最大,液态时次之,固态时熵值最小 |
| C.反应(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)的熵值增加 |
| D.由于合成氨反应∆H<0,∆S<0,所以该反应低温下能自发进行 |
您最近一年使用:0次
4 . 碳、氮化合物在生产、生活中具有重要作用。回答下列问题:
(1)已知在298K 和101kPa条件下,有如下反应:
反应I:C(s)+O2(g)= CO2(g) ΔH 1=-393.5mol·L-1
反应II:2C(s)+O2(g)= 2CO(g) ΔH 2=-221mol·L-1
反应III:N2(g)+O2(g)= 2NO(g) ΔH 3=180.5mol·L-1
①汽车尾气净化原理为反应IV:2NO(g)+2CO(g) N2(g)+2CO2(g),其反应热ΔH =
N2(g)+2CO2(g),其反应热ΔH =__________ ,该反应能自发进行的条件是_________ (填“低温”或“高温”)。
②在恒容密闭容器中发生IV的反应,下列有关该反应的说法中正确的是_____________ (填字母)。
A.升高温度,平衡常数减小
B.体系达到平衡后,加入催化剂,平衡正向移动
C.增大c(CO),平衡逆向移动,NO的转化率降低
D.其他条件不变,向平衡体系充入CO2气体,K值减小
E.该反应过程中,气体的密度始终保持不变
(2)利用电解法可以消除废水溶液中 CN-,其原理为:碱性条件下,阳极Cl-先转化为ClO-,再将CN-氧化为两种无污染的气体。
①阳极电极反应式为______________________________________________ 。
②阳极附近溶液中除去CN-的离子方程式为______________________________ 。
(1)已知在298K 和101kPa条件下,有如下反应:
反应I:C(s)+O2(g)= CO2(g) ΔH 1=-393.5mol·L-1
反应II:2C(s)+O2(g)= 2CO(g) ΔH 2=-221mol·L-1
反应III:N2(g)+O2(g)= 2NO(g) ΔH 3=180.5mol·L-1
①汽车尾气净化原理为反应IV:2NO(g)+2CO(g)
 N2(g)+2CO2(g),其反应热ΔH =
N2(g)+2CO2(g),其反应热ΔH =②在恒容密闭容器中发生IV的反应,下列有关该反应的说法中正确的是
A.升高温度,平衡常数减小
B.体系达到平衡后,加入催化剂,平衡正向移动
C.增大c(CO),平衡逆向移动,NO的转化率降低
D.其他条件不变,向平衡体系充入CO2气体,K值减小
E.该反应过程中,气体的密度始终保持不变
(2)利用电解法可以消除废水溶液中 CN-,其原理为:碱性条件下,阳极Cl-先转化为ClO-,再将CN-氧化为两种无污染的气体。
①阳极电极反应式为
②阳极附近溶液中除去CN-的离子方程式为
您最近一年使用:0次
解题方法
5 . 判断下列4个反应在什么条件下能自发进行?
(1)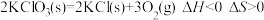
________
(2)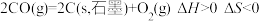
________
(3)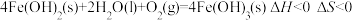
________
(4)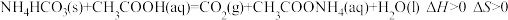
________
(1)
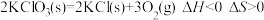
(2)
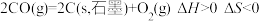
(3)
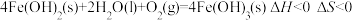
(4)
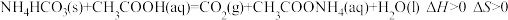
您最近一年使用:0次
6 . 下列关于干冰转化为二氧化碳气体的过程,判断正确的是
A.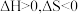 | B. | C. | D. |
您最近一年使用:0次
解题方法
7 . 下列说法不正确的是
A. 与 与 的反应是熵增的放热反应,该反应能自发进行 的反应是熵增的放热反应,该反应能自发进行 |
B.饱和 溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 |
C. 和 和 均可加快 均可加快 分解,同等条件下二者对 分解,同等条件下二者对 分解速率的改变相同 分解速率的改变相同 |
D.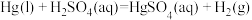 常温下不能自发进行,说明 常温下不能自发进行,说明 |
您最近一年使用:0次
2020-09-16更新
|
161次组卷
|
2卷引用:鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第1节 化学反应的方向
8 . 碳酸铵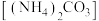 在室温下能自发分解产生氨气、水和二氧化碳,下列说法正确的是
在室温下能自发分解产生氨气、水和二氧化碳,下列说法正确的是
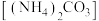 在室温下能自发分解产生氨气、水和二氧化碳,下列说法正确的是
在室温下能自发分解产生氨气、水和二氧化碳,下列说法正确的是| A.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大 |
| B.碳酸铵分解是吸热反应,体系的熵减小 |
| C.碳酸铵分解是吸热反应,根据焓判据能说明它能自发分解 |
| D.碳酸盐都不稳定,室温下都能自发分解 |
您最近一年使用:0次
2020-09-16更新
|
131次组卷
|
2卷引用:鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第1节 化学反应的方向
解题方法
9 . 已知反应 ,则:
,则:
(1)该反应在室温下___________ (填“能”或“不能”)自发进行。
(2)根据题中所给数据进行分析,温度____________ (填“能”或“不能”)成为反应方向的决定因素。
(3)若温度能决定反应方向,则该反应能自发进行的最低温度为_______ K(假设反应的焓变与熵变不随温度变化而变化,结果保留整数)。
 ,则:
,则:(1)该反应在室温下
(2)根据题中所给数据进行分析,温度
(3)若温度能决定反应方向,则该反应能自发进行的最低温度为
您最近一年使用:0次
解题方法
10 . 下列说法正确的是
A.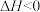 的化学反应均是自发反应 的化学反应均是自发反应 |
B.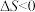 的反应均不能自发进行 的反应均不能自发进行 |
C.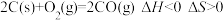 ,该反应一定能自发进行 ,该反应一定能自发进行 |
D.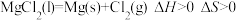 ,该反应一定不能自发进行 ,该反应一定不能自发进行 |
您最近一年使用:0次



