1 . 下列操作会使H2O的电离平衡向电离方向移动且pH<7的是
| A.向水中加少量Na2CO3 | B.向水中加少量FeCl3 |
| C.向水中加少量NaHSO4 | D.向水中加入少量NaCl |
您最近一年使用:0次
2012·山西·模拟预测
2 . 水的电离平衡曲线如图所示,下列说法不正确的是


| A.图中五点KW间的关系:B>C>A=D=E |
| B.若从A点到D点,可采用:温度不变在水中加入少量的酸 |
| C.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性 |
| D.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl 固体的变化 |
您最近一年使用:0次
10-11高三上·四川成都·阶段练习
名校
3 . 下列四种溶液中:①pH值为0的盐酸;②0.lmol/L的盐酸;③0.01mol/L的氢氧化钠溶液;④pH值为11的氢氧化钠溶液。由水电离生成的c(H+)之比依次为
| A.0:1: 12:11 | B.14:13:12:11 |
| C.14:13:2:3 | D.1:10:100:1000 |
您最近一年使用:0次
2010·安徽安庆·一模
4 . 已知H2C2O4是二元弱酸,酸式盐NaHC2O4的溶液呈酸性。30℃时,浓度均为0.1mol•L-1NaHC2O4溶液和Na2C2O4溶液中均存在的关系是
| A.c(H+)•c(OH-) =1×10-14 |
| B.c(H+) +c(H2C2O4) =c(C2O42-)+c(OH-) |
| C.c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+ 2c(C2O42-) |
| D.c(OH-) =c(H+) +c(HC2O4-)+ 2c(H2C2O4) |
您最近一年使用:0次
2010·河北·一模
5 . 浓度均为0.1mol·L-1的三种溶液:①碳酸钠溶液、②氢氧化钠溶液、③醋酸钠溶液,下列说法不正确的是
| A.三种溶液的pH大小顺序是③>①>② |
| B.若将三种溶液稀释相同倍数,pH变化最大的是② |
| C.升高相同的温度,三种溶液的PH均减少 |
| D.水电离出的c(OH-):②>③>① |
您最近一年使用:0次
2010·云南曲靖·一模
6 . 下列叙述正确的是
| A.pH为3的盐酸中,其c(H+)是pH为1的盐酸中的3倍 |
| B.0.1mol/LKOH溶液和0.1mol/L 氨水中,其c(OH-)相等 |
C.在25℃时,无论是酸性、碱性还是中性溶液中,其c(H+)和c(OH-)的乘积都等于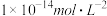 |
| D.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
您最近一年使用:0次
2010·全国·模拟预测
7 . 水的电离平衡曲线如图所示,下列说法不正确的是:
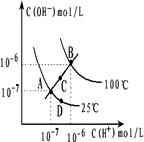

| A.图中四点Kw间的关系: A=D<C<B |
| B.若从A点到D点,可采用:温度不变在水中加入少量酸 |
| C.若从A点到C点,可采用:温度不变在水中加入少量NH4Cl固体 |
| D.若处在B点,将pH=2的硫酸与pH=10的KOH的两种溶液等体积混合后,溶液显中性 |
您最近一年使用:0次
2010·福建·三模
8 . 下列表述中,不正确的是
| A.用稀盐酸洗涤AgCl沉淀比用水洗涤,损耗AgCl少 |
| B.等体积的 pH均等于3的盐酸和AlCl3溶液中,电离的水分子数前者一定小于后者 |
| C.高效催化剂可使水分解,同时释放能量 |
| D.明矾用于净水和氯气用于自来水的杀菌消毒,两个反应遵循的化学原理不同 |
您最近一年使用:0次
2010·广西柳州·三模
9 . 25°C时,重水(D2O)的离子积为1.6×10-15也可用pH值一样的定义来规定其酸碱度:pD==-lgCD+,下列叙述正确的是
①中性D2O的pD=7
②在1LD2O中,溶解0.01molDCl,其pD值为1
③1L0.1mol/L的NaOD的重水溶液,pD=12
④在100mL0.25rnoL/LDCl的重水溶液中,加入50mL0.2mol/L NaOD的重水溶液,反应后溶液的pD=1
⑤温度升高,CD+×COD-的值会升高
①中性D2O的pD=7
②在1LD2O中,溶解0.01molDCl,其pD值为1
③1L0.1mol/L的NaOD的重水溶液,pD=12
④在100mL0.25rnoL/LDCl的重水溶液中,加入50mL0.2mol/L NaOD的重水溶液,反应后溶液的pD=1
⑤温度升高,CD+×COD-的值会升高
| A.②③ | B.③④ | C.①② | D.④⑤ |
您最近一年使用:0次
10 . 一定温度下,水溶液中H+和OH-的浓度变化如图所示,下列说法不正确的是


| A.该温度下,加入NaHSO4可能引起由b向a的变化 |
| B.该温度下,pH=2的盐酸与pH=12的氢氧化钠溶液等体积混合,所得溶液显中性 |
| C.该温度下,加入Na2CO3溶液能引起b向c的变化 |
| D.降低温度可能引起b向d的变化 |
您最近一年使用:0次



