1 . 已知AG的定义为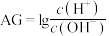 ,室温下用0.1
,室温下用0.1 的HCl溶液滴定10.00mL 0.1
的HCl溶液滴定10.00mL 0.1 某一元碱MOH溶液,滴定过程中AG与HCl溶液体积变化关系如图所示。下列说法正确的是
某一元碱MOH溶液,滴定过程中AG与HCl溶液体积变化关系如图所示。下列说法正确的是
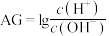 ,室温下用0.1
,室温下用0.1 的HCl溶液滴定10.00mL 0.1
的HCl溶液滴定10.00mL 0.1 某一元碱MOH溶液,滴定过程中AG与HCl溶液体积变化关系如图所示。下列说法正确的是
某一元碱MOH溶液,滴定过程中AG与HCl溶液体积变化关系如图所示。下列说法正确的是 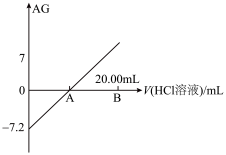
A.MOH的电离常数的数量级为 |
| B.A点时水的电离程度最大 |
| C.A点时加入HCl溶液的体积等于10.00mL |
D.B点时溶液中存在: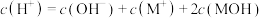 |
您最近半年使用:0次
2 . 常温下,向20 mL 0.1 mol⋅L HCOOH溶液中滴加V mL 0.1 mol⋅L
HCOOH溶液中滴加V mL 0.1 mol⋅L NaOH溶液,混合溶液的pH与
NaOH溶液,混合溶液的pH与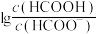 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是
 HCOOH溶液中滴加V mL 0.1 mol⋅L
HCOOH溶液中滴加V mL 0.1 mol⋅L NaOH溶液,混合溶液的pH与
NaOH溶液,混合溶液的pH与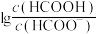 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是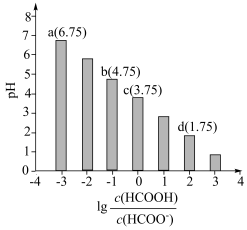
A.当 时,随着 时,随着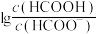 减小,水的电离程度减小 减小,水的电离程度减小 |
B.当 时达到图像c点 时达到图像c点 |
C.当 时,该溶液呈碱性 时,该溶液呈碱性 |
D.常温下,HCOOH的电离常数 的数量级为 的数量级为 |
您最近半年使用:0次
解题方法
3 .  用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。
 .配制溶液
.配制溶液
(1)配制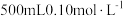 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为___________  。
。
(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有___________ (填标号)。 .实验探究
.实验探究
探究温度对 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。
(3) 溶液显碱性的原因是
溶液显碱性的原因是___________ (用离子方程式表示)。
(4)实验1中测得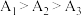 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中___________ 发挥主导作用。实验1中测得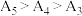 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。
(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料: 溶液中存在平衡:
溶液中存在平衡: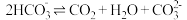 。
。
提出猜想:对于 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。
实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
实验结论:②根据实验1~3的结果,小组同学认为猜想成立,其判断依据是___________ 。
拓展总结:③ 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: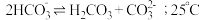 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为___________ [保留两位有效数字;已知: 时,
时,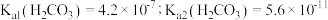 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。
(6)写出 在生产或生活中的一种应用
在生产或生活中的一种应用___________ 。
 用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。 .配制溶液
.配制溶液(1)配制
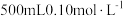 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为 。
。(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有
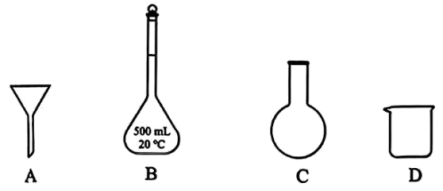
 .实验探究
.实验探究探究温度对
 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。| 实验序号 | 操作 | 测试温度 |  |
| 1 | 采用水浴加热,将 溶液从 溶液从 持续升温至 持续升温至 ,每隔 ,每隔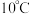 测量并记录溶液 测量并记录溶液 |  |  |
 |  | ||
 |  | ||
 |  | ||
 | 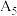 |
 溶液显碱性的原因是
溶液显碱性的原因是(4)实验1中测得
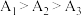 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中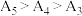 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料:
 溶液中存在平衡:
溶液中存在平衡: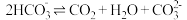 。
。提出猜想:对于
 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
| 实验序号 | 操作 | 测试温度 |  |
| 2 | 采用水浴加热,① ,并记录溶液 ,并记录溶液 |  |  |
| 3 | 采用水浴加热,将 溶液从 溶液从 升温至 升温至 ,然后冷却至 ,然后冷却至 ,并记录溶液 ,并记录溶液 |  |  |
拓展总结:③
 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: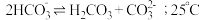 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为 时,
时,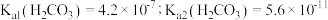 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。(6)写出
 在生产或生活中的一种应用
在生产或生活中的一种应用
您最近半年使用:0次
名校
解题方法
4 . 室温下,某二元弱酸(用H2A表示)的 、
、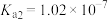 ,NH3⋅H2O的
,NH3⋅H2O的 ,通过下列实验探究NH4HA溶液的性质。
,通过下列实验探究NH4HA溶液的性质。
下列有关说法正确的是
 、
、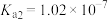 ,NH3⋅H2O的
,NH3⋅H2O的 ,通过下列实验探究NH4HA溶液的性质。
,通过下列实验探究NH4HA溶液的性质。| 实验 | 实验操作 |
| 1 | 用pH试纸测定0.1mol·L-1NH4HA溶液的pH,测得pH约为4.5 |
| 2 | 将0.1mol·L-1NH4HA溶液和0.1mol·L-1NaOH溶液等体积混合,无气体产生 |
| 3 | 向实验2所得溶液中继续滴加一定量0.1mol·L-1NaOH溶液,加热,使产生的气体完全逸出 |
| 4 | 将等体积0.1mol·L-1NH4HA溶液与0.05mol·L-1ZnSO4溶液混合,产生ZnA沉淀 |
A.由实验1可知,0.1mol⋅L-1NH4HA溶液中由水电离出的 |
B.实验2所得溶液中存在: |
C.实验3所得溶液中一定含有Na2A,故反应过程中一定有: |
D.由实验4可知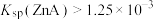 |
您最近半年使用:0次
解题方法
5 . 室温下,向浓度均为 的
的 和
和 混合溶液
混合溶液 中滴加
中滴加 标准盐酸,溶液
标准盐酸,溶液 与
与 关系如图所示。下列叙述正确的是
关系如图所示。下列叙述正确的是
 的
的 和
和 混合溶液
混合溶液 中滴加
中滴加 标准盐酸,溶液
标准盐酸,溶液 与
与 关系如图所示。下列叙述正确的是
关系如图所示。下列叙述正确的是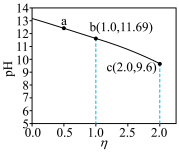
A.水的电离程度: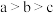 |
B.常温下, 的水解常数 的水解常数 约为 约为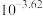 |
C.c点溶液中: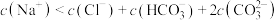 |
D.b点溶液中: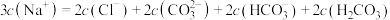 |
您最近半年使用:0次
名校
6 . 常温下,用0.1 mol⋅L 的NaOH溶液滴定10.00 mL 0.1 mol⋅L
的NaOH溶液滴定10.00 mL 0.1 mol⋅L 二元酸
二元酸 ,滴定过程中混合溶液的pH随滴加NaOH溶液的体积的变化曲线如图所示,下列说法正确的是
,滴定过程中混合溶液的pH随滴加NaOH溶液的体积的变化曲线如图所示,下列说法正确的是 的电离常数
的电离常数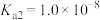 ;忽略混合时溶液体积变化。
;忽略混合时溶液体积变化。
 的NaOH溶液滴定10.00 mL 0.1 mol⋅L
的NaOH溶液滴定10.00 mL 0.1 mol⋅L 二元酸
二元酸 ,滴定过程中混合溶液的pH随滴加NaOH溶液的体积的变化曲线如图所示,下列说法正确的是
,滴定过程中混合溶液的pH随滴加NaOH溶液的体积的变化曲线如图所示,下列说法正确的是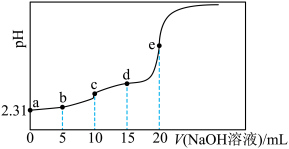
 的电离常数
的电离常数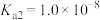 ;忽略混合时溶液体积变化。
;忽略混合时溶液体积变化。A. 的电离常数 的电离常数 约为 约为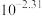 |
| B.e点溶液能使pH试纸变红 |
| C.c点水的电离程度比b点水的电离程度大 |
D.d点溶液中存在: mol⋅L mol⋅L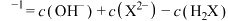 |
您最近半年使用:0次
解题方法
7 . 常温下,分别向相同浓度的NaHCO3、Na2CO3溶液中逐滴加入盐酸,滴加过程中溶液的pH变化如下图所示。下列说法正确的是
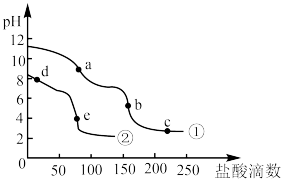
| A.曲线①表示盐酸滴入NaHCO3溶液的过程 |
| B.d、e点水的电离程度:d>e |
| C.a点的KW大于d点的KW |
D.b、c、e点均满足: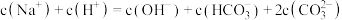 |
您最近半年使用:0次
8 .  为二元弱酸,常温下,现配制一组
为二元弱酸,常温下,现配制一组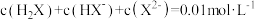 的溶液,在不同pH环境下,不同形态的含X粒子(
的溶液,在不同pH环境下,不同形态的含X粒子( 、
、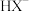 、
、 )的分布系数
)的分布系数 (平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是
(平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是
 为二元弱酸,常温下,现配制一组
为二元弱酸,常温下,现配制一组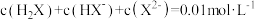 的溶液,在不同pH环境下,不同形态的含X粒子(
的溶液,在不同pH环境下,不同形态的含X粒子( 、
、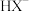 、
、 )的分布系数
)的分布系数 (平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是
(平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是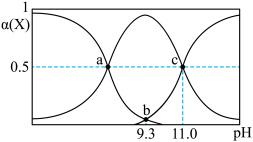
| A.a点对应的溶液的pH为7.6 |
B.在NaHX溶液中存在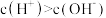 |
C.c点对应的溶液中存在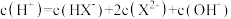 |
D.室温下,a、b、c三点对应的溶液中,由水电离出的 与 与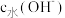 的乘积 的乘积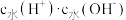 数值由大到小顺序:a>b>c 数值由大到小顺序:a>b>c |
您最近半年使用:0次
2024-04-18更新
|
142次组卷
|
2卷引用:2024届”3+3+3“高考备考诊断性联考卷(二)理综试题-高中化学
9 . 25℃时,用1mol/L的NaOH溶液调节0.10L0.1mol/LH2C2O4溶液的pH,溶液中H2C2O4、 及
及 的物质的量浓度变化如图所示。下列说法错误的是
的物质的量浓度变化如图所示。下列说法错误的是
 及
及 的物质的量浓度变化如图所示。下列说法错误的是
的物质的量浓度变化如图所示。下列说法错误的是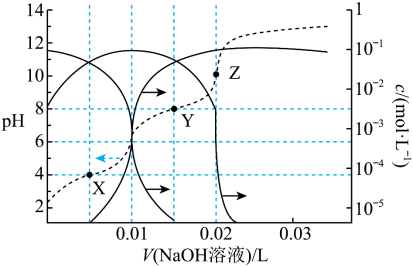
| A.H2C2O4的Ka1=1×10-4 |
B.Y点:c(Na+)<3c( ) ) |
| C.水的电离程度Z>Y>X |
D.1mol/L的NaHC2O4 溶液中:c(Na+) >c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
您最近半年使用:0次
10 . 实验测得体积相同,浓度均为0.10 mol⋅L 的
的 溶液和
溶液和 溶液的pH随温度的变化情况如图所示。下列说法正确的是
溶液的pH随温度的变化情况如图所示。下列说法正确的是
 的
的 溶液和
溶液和 溶液的pH随温度的变化情况如图所示。下列说法正确的是
溶液的pH随温度的变化情况如图所示。下列说法正确的是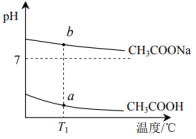
A.b点的 大于a点的 大于a点的 |
| B.溶液中水的电离程度:a点大于b点 |
| C.溶液中离子总数:b点大于a点 |
D.升高温度 溶液的pH减小,说明升温抑制水解 溶液的pH减小,说明升温抑制水解 |
您最近半年使用:0次



