解题方法
1 . 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时pH变化曲线如图所示。
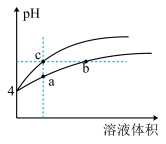
(1)a、b、c三点溶液中水的电离程度大小关系:_______ 。
(2)①b点溶液中c(H+) =_______+_______ (填微粒浓度)。________
②用等浓度的NaOH溶液和b、c处溶液反应,消耗NaOH溶液的体积。
_______ 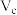 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)阐述a、c两点溶液的导电能力强弱:_______ 。

(1)a、b、c三点溶液中水的电离程度大小关系:
(2)①b点溶液中c(H+) =_______+_______ (填微粒浓度)。
②用等浓度的NaOH溶液和b、c处溶液反应,消耗NaOH溶液的体积。

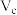 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)阐述a、c两点溶液的导电能力强弱:
您最近一年使用:0次
解题方法
2 . 在某温度时,将1.0mol・L-1氨水滴入10 mL1.0mol・L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示:
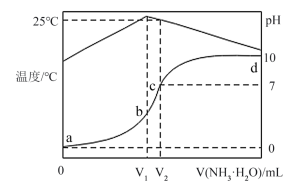
(1)a、b、c、d对应的溶液中水的电离程度由大到小的是_____ 。
(2)氨水体积滴至____ 时(填“V1”或“V2”),氨水与盐酸恰好完全反应,简述判断依据____ ;此时溶液中离子浓度由大到小的顺序是____ 。

(1)a、b、c、d对应的溶液中水的电离程度由大到小的是
(2)氨水体积滴至
您最近一年使用:0次
3 . 研究NO2、NO、SO2 、CO等大气污染气体的处理具有重要意义。利用反应6NO2(g)+8NH3(g)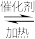 7N2(g)+12H2O(g)可处理NO2。
7N2(g)+12H2O(g)可处理NO2。
(1)在2L的密闭容器中,2分钟内,上述反应混合物的物质的量增加了0.25mol,则2分钟内v(NH3)=______ 。
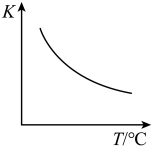
(2)该反应的化学平衡常数表达式K=______ ;已知该反应平衡常数(K)与温度(T)的关系如图所示,若升高温度,则v正反应______ v逆反应(填“大于”、“小于”或“等于”);反应达到平衡后若缩小反应容器体积,其它条件不变,则混合气体的平均式量将______ (填“变大”、“变小”或“不变”)。
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组同学收集某地的雨水进行实验,每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
(3)请写出上述pH变化的原因______ 。
(4)有物质的量浓度相等的三种铵盐溶液:①NH4Cl ②NH4HCO3 ③NH4HSO4,这三种溶液中水的电离程度由大到小的顺序是______ (填编号)。
(5)向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀,用电离平衡原理解释上述现象。______ 。
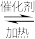 7N2(g)+12H2O(g)可处理NO2。
7N2(g)+12H2O(g)可处理NO2。(1)在2L的密闭容器中,2分钟内,上述反应混合物的物质的量增加了0.25mol,则2分钟内v(NH3)=
(2)该反应的化学平衡常数表达式K=
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组同学收集某地的雨水进行实验,每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
(3)请写出上述pH变化的原因
(4)有物质的量浓度相等的三种铵盐溶液:①NH4Cl ②NH4HCO3 ③NH4HSO4,这三种溶液中水的电离程度由大到小的顺序是
(5)向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀,用电离平衡原理解释上述现象。
您最近一年使用:0次
2019-08-19更新
|
314次组卷
|
2卷引用:上海市青浦区2019届高三高三第二次学业质量调研(二模)化学试题



