1 . 下列事实不能 用平衡移动原理解释的是
A.FeS可用于除去废水中的 |
| B.25℃~100℃,随温度升高,纯水的pH减小 |
C.加热 溶液,液体由黄色变为红褐色 溶液,液体由黄色变为红褐色 |
D.  ,采用高温提高单位时间内 ,采用高温提高单位时间内 的产率 的产率 |
您最近一年使用:0次
解题方法
2 .  用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。
 .配制溶液
.配制溶液
(1)配制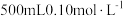 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为___________  。
。
(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有___________ (填标号)。 .实验探究
.实验探究
探究温度对 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。
(3) 溶液显碱性的原因是
溶液显碱性的原因是___________ (用离子方程式表示)。
(4)实验1中测得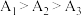 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中___________ 发挥主导作用。实验1中测得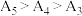 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。
(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料: 溶液中存在平衡:
溶液中存在平衡: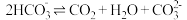 。
。
提出猜想:对于 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。
实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
实验结论:②根据实验1~3的结果,小组同学认为猜想成立,其判断依据是___________ 。
拓展总结:③ 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: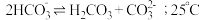 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为___________ [保留两位有效数字;已知: 时,
时,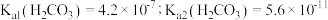 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。
(6)写出 在生产或生活中的一种应用
在生产或生活中的一种应用___________ 。
 用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。 .配制溶液
.配制溶液(1)配制
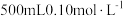 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为 。
。(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有
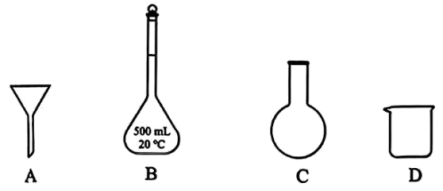
 .实验探究
.实验探究探究温度对
 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。| 实验序号 | 操作 | 测试温度 |  |
| 1 | 采用水浴加热,将 溶液从 溶液从 持续升温至 持续升温至 ,每隔 ,每隔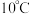 测量并记录溶液 测量并记录溶液 |  |  |
 |  | ||
 |  | ||
 |  | ||
 |  |
 溶液显碱性的原因是
溶液显碱性的原因是(4)实验1中测得
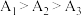 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中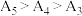 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料:
 溶液中存在平衡:
溶液中存在平衡: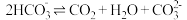 。
。提出猜想:对于
 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
| 实验序号 | 操作 | 测试温度 |  |
| 2 | 采用水浴加热,① ,并记录溶液 ,并记录溶液 |  |  |
| 3 | 采用水浴加热,将 溶液从 溶液从 升温至 升温至 ,然后冷却至 ,然后冷却至 ,并记录溶液 ,并记录溶液 |  |  |
拓展总结:③
 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: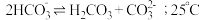 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为 时,
时,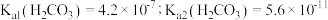 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。(6)写出
 在生产或生活中的一种应用
在生产或生活中的一种应用
您最近一年使用:0次
3 . 为了探究温度对水解平衡的影响,用手持技术测定一定浓度 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是
 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是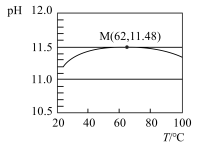
| A.该实验能证明升温促进水解 | B.点M之后 水解放热 水解放热 |
C.点M处溶液中 略大于 略大于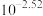 mol/L mol/L | D.点M后pH下降是因为升温对 的影响更大 的影响更大 |
您最近一年使用:0次
名校
解题方法
4 . 常温下 溶液体系中存在平衡关系:
溶液体系中存在平衡关系: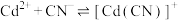 ;
; ;
;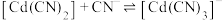 ;
;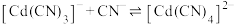 ,平衡常数依次为
,平衡常数依次为 。含
。含 物种的组分分布分数
物种的组分分布分数 、平均配位数
、平均配位数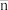 与
与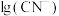 的关系如图所示。已知
的关系如图所示。已知 ,
,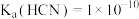 ;
;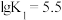 ,
,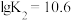 ,
, ,
, 。
。
 溶液体系中存在平衡关系:
溶液体系中存在平衡关系: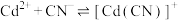 ;
; ;
;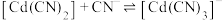 ;
;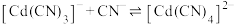 ,平衡常数依次为
,平衡常数依次为 。含
。含 物种的组分分布分数
物种的组分分布分数 、平均配位数
、平均配位数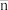 与
与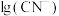 的关系如图所示。已知
的关系如图所示。已知 ,
,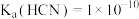 ;
;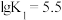 ,
,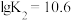 ,
, ,
, 。
。
A.随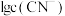 增大,水的电离程度减小 增大,水的电离程度减小 |
B. 时, 时,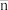 约为3 约为3 |
C.a点时,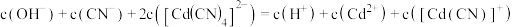 |
D.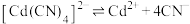 的平衡常数的 的平衡常数的 |
您最近一年使用:0次
2024-04-15更新
|
407次组卷
|
2卷引用:山东省潍坊市2023-2024学年高三下学期一模化学试题
5 . 室温下,向 浓度相同的盐酸与醋酸稀溶液中分别滴加同浓度的
浓度相同的盐酸与醋酸稀溶液中分别滴加同浓度的 溶液,滴加
溶液,滴加 溶液的体积与
溶液的体积与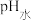 的关系如图所示。已知
的关系如图所示。已知 表示溶液中水电离出的
表示溶液中水电离出的 浓度,
浓度,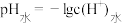 。
。
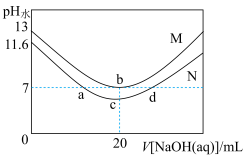
下列说法正确的是
 浓度相同的盐酸与醋酸稀溶液中分别滴加同浓度的
浓度相同的盐酸与醋酸稀溶液中分别滴加同浓度的 溶液,滴加
溶液,滴加 溶液的体积与
溶液的体积与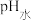 的关系如图所示。已知
的关系如图所示。已知 表示溶液中水电离出的
表示溶液中水电离出的 浓度,
浓度,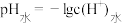 。
。
下列说法正确的是
A.醋酸的初始浓度大于 |
| B.水的电离程度c点小于b点 |
C.若a点滴加 溶液为 溶液为 ,则醋酸电离常数 ,则醋酸电离常数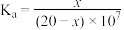 |
D.a,b点溶液显中性,且存在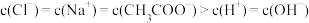 |
您最近一年使用:0次
解题方法
6 . 将摩尔盐[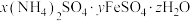 ]溶于水配成溶液,下列说法正确的是
]溶于水配成溶液,下列说法正确的是
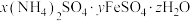 ]溶于水配成溶液,下列说法正确的是
]溶于水配成溶液,下列说法正确的是A.该溶液中还可大量共存 、 、 、 、 |
B.常温下该溶液中水电离出的 可能为 可能为 |
C.加入少量 后再滴入KSCN溶液,溶液变为红色,则证明溶液中含 后再滴入KSCN溶液,溶液变为红色,则证明溶液中含 |
D.向溶液中滴入 溶液使 溶液使 恰好沉淀时, 恰好沉淀时, 和 和 都会参与反应 都会参与反应 |
您最近一年使用:0次
7 . 常温下,向0.02mol·L-1 FeCl3溶液(用少量盐酸酸化)中匀速逐滴加入0.1mol·L-1 NaOH溶液,得到pH-t曲线如图。下列说法正确的是
已知:25℃时,Fe(OH)3的Ksp=2.8×10-39
已知:25℃时,Fe(OH)3的Ksp=2.8×10-39
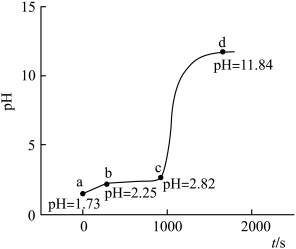
| A.已知a点为滴定起始点,pH=1.73是因为FeCl3溶于水发生了水解反应 |
| B.由a点到b点的过程中,滴加的NaOH溶液与FeCl3发生反应 |
| C.该条件下,Fe3+的沉淀pH范围约为2.25~2.82 |
| D.d点的溶液中,由水电离出的c(OH—)约为10-2.16mol·L-1 |
您最近一年使用:0次
2024-03-26更新
|
521次组卷
|
3卷引用:北京市顺义区2023-2024学年高三上学期第一次统练化学试题
北京市顺义区2023-2024学年高三上学期第一次统练化学试题 (已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)北京交通大学附属中学2023-2024学年高三下学期3月月考化学试题
名校
8 . 1922年范斯莱克(Vanslyke)提出用缓冲容量β来描述缓冲溶液缓冲能力大小,β越大,缓冲能力越大。下图是常温下,CH3COOH和CH3COONa组成缓冲溶液的β-pH关系图,其中A、B两条曲线分别对应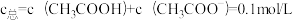 和
和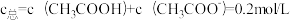 。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
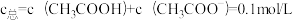 和
和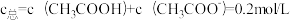 。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是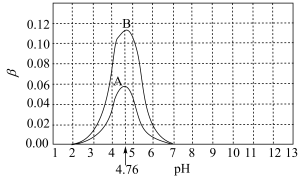
| A.向pH=4.76的上述缓冲溶液中加入少量NaOH溶液,水的电离程度会增大 |
B.A曲线上任意一点的溶液中均存在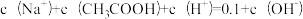 |
| C.B曲线代表的溶液缓冲能力最大时,溶液中c(Na+)>c(CH3COOH) |
D.pH=4时,A、B曲线所代表的溶液中 相等 相等 |
您最近一年使用:0次
2024-03-16更新
|
221次组卷
|
2卷引用:2024届甘肃省兰州市高三下学期诊断考试化学试卷
名校
解题方法
9 . 下列实验操作及现象与结论不一致的是
| 实验操作及现象 | 结论 | |
| A | 测定不同温度下蒸馏水的 , , 随温度升高而降低 随温度升高而降低 | 水的电离程度随温度升高而增大 |
| B | 向新制的 溶液中滴入少量蔗糖溶液并加热,不产生砖红色沉淀 溶液中滴入少量蔗糖溶液并加热,不产生砖红色沉淀 | 蔗糖不属于还原糖 |
| C | 将少量乙酸乙酯加入 溶液中,出现分层,静置一段时间后酯层消失 溶液中,出现分层,静置一段时间后酯层消失 | 乙酸乙酯可在碱性条件下水解 |
| D | 向 溶液( 溶液( )中滴加 )中滴加 溶液,紫色褪去 溶液,紫色褪去 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-22更新
|
834次组卷
|
4卷引用:2024年1月甘肃普通高等学校招生考试适应性测试化学试题
2024年1月甘肃普通高等学校招生考试适应性测试化学试题(已下线)选择题6-10(已下线)热点08 表格型实验方案的设计与评价四川省遂宁市射洪市四川省射洪中学校2023-2024学年高三下学期开学理综试题-高中化学
名校
10 . 实验室模拟侯氏制碱碳酸化制 的过程,将
的过程,将 通入饱和氨盐水(溶质为
通入饱和氨盐水(溶质为 、
、 ),实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数
),实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数 与pH的关系如图2。
与pH的关系如图2。
 的过程,将
的过程,将 通入饱和氨盐水(溶质为
通入饱和氨盐水(溶质为 、
、 ),实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数
),实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数 与pH的关系如图2。
与pH的关系如图2。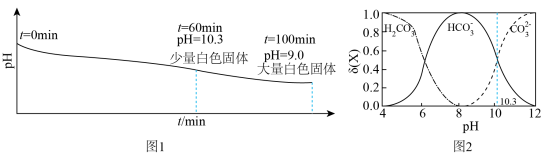
A.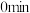 ,溶液中 ,溶液中 |
B. ,发生反应: ,发生反应: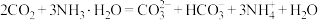 |
C.水的电离程度: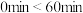 |
D.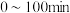 , ,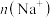 、 、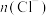 均保持不变 均保持不变 |
您最近一年使用:0次
2024-01-19更新
|
479次组卷
|
4卷引用:福建省宁德市福古霞三校2024届高三3月份适应性检测化学试题



