1 . 下列说法正确的是
| A.某酸和某碱等体积混合,充分反应后,溶液呈酸性,可以推测BOH为弱碱 |
B. 的盐酸和 的盐酸和 的氨水等体积混合后,恰好完全反应,则所用盐酸和氨水的物质的量浓度相等 的氨水等体积混合后,恰好完全反应,则所用盐酸和氨水的物质的量浓度相等 |
C. 的NaCl溶液和 的NaCl溶液和 的 的 溶液,水的电离程度相同 溶液,水的电离程度相同 |
| D.同物质的量浓度的盐酸与醋酸分别中和同体积同浓度的NaOH溶液,消耗醋酸的体积多 |
您最近一年使用:0次
2022-02-22更新
|
354次组卷
|
2卷引用:浙江省浙南联盟2022届高三第二次模拟考试化学试题
名校
解题方法
2 . 下列说法正确的是
| A.25℃时,pH均为11的烧碱溶液与纯碱溶液中,水的电离程度相同 |
B.25℃时,pH=9的某酸式盐NaHA的水溶液中: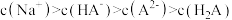 |
C.等物质的量浓度的K2S和KHS混合溶液中: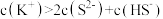 |
| D.用NaOH标准溶液滴定未知浓度的盐酸,达到滴定终点时发现滴定管尖嘴部分有悬滴,会使测定结果偏小 |
您最近一年使用:0次
2022-02-12更新
|
478次组卷
|
6卷引用:福建省闽粤名校联盟2021-2022学年高三下学期2月联考化学试题
3 . 常温下,向20mL1mol·L-1CuCl2溶液中滴加2mol·L-1Na2S溶液的滴定曲线如图所示。已知:pCu=-lgc(Cu2+),lg2.5=0.4,常温下Ksp(FeS)=6.3×10-18;Kal(H2S)=1.2×10-7,Ka2(H2S)=7.1×10-15。下列说法中正确的是
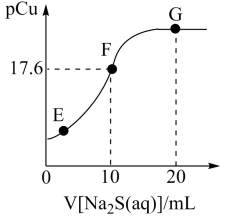

| A.常温下,S2-的水解常数Kh(S2-)约为8.3×10-8 |
| B.E→F→G的过程中,水的电离度一直在减小 |
| C.向1mol·L-1FeSO4(aq)中加入足量CuS固体,产生FeS沉淀 |
| D.25℃时,Cu2++H2S=CuS↓+2H+的K约为1.36×1014 |
您最近一年使用:0次
4 . 常温下,弱酸HA与弱碱MOH分别用强碱或强酸调节pH时,HA、A—、MOH和M+的分布分数δ(X)与溶液pH的关系如图所示。
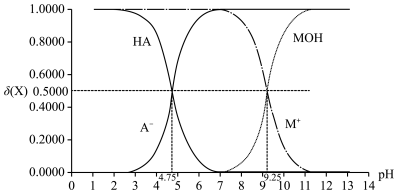
已知:以HA分子为例,存在δ(HA)= ]。下列说法正确的是
]。下列说法正确的是

已知:以HA分子为例,存在δ(HA)=
 ]。下列说法正确的是
]。下列说法正确的是| A.MA溶液中水的电离程度高于纯水 |
| B.MOH的电离常数Kb(MOH)=10-9.25 |
| C.等物质的量浓度的HA和NaA的混合溶液中pH>7 |
| D.pH=7的HA与NaOH的混合溶液及HA与MOH的混合溶液中δ(HA)后者大于前者 |
您最近一年使用:0次
2022-01-22更新
|
733次组卷
|
4卷引用:广东省肇庆市2021-2022学年高三第二次模拟考试化学试题
名校
5 . 溶液的pH与水的电离密切相关,以下说法一定正确的是
| A.90°C的纯水pH=7 |
| B.将醋酸滴入氢氧化钠溶液,促进了水的电离 |
| C.电解质溶液中都存在水的电离平衡 |
| D.室温下pH相同的盐酸和明矾溶液,水的电离程度相同 |
您最近一年使用:0次
2022-01-16更新
|
165次组卷
|
3卷引用:上海市静安区2022届高三一模化学试题
名校
解题方法
6 . HX为一元弱酸,YOH为一元强碱。常温下,向难溶强电解质(YX)的悬浊液中加入某酸,测得c(Y+)与c(H+)的变化关系如图实线所示。下列说法错误的是
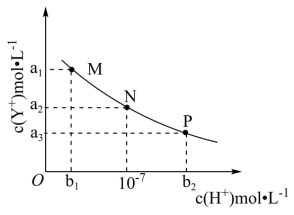

| A.M点时,c(X-)<c(Y+) |
| B.水的电离程度:N>P |
| C.实验时可加入的酸为盐酸 |
| D.难溶物YX的溶度积K为a22 |
您最近一年使用:0次
2021-12-30更新
|
1297次组卷
|
8卷引用:四川省成都市2021-2022学年高三上学期第一次诊断性检测理综化学试题
四川省成都市2021-2022学年高三上学期第一次诊断性检测理综化学试题宁夏回族自治区石嘴山市平罗中学2022届高三第三次模拟理科综合化学试题(已下线)卷02 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型142 有关沉淀溶解平衡图像湖南省株洲市第二中学2023届高三第七次月考化学试题湖南省株洲市第一中学2023届高三第七次月考化学试题四川省双流棠湖中学2023-2024学年高三上学期10月月考理综化学试题
7 . 常温下,下列说法不正确的是
| A.在0.1mol•L-1的醋酸溶液中,加入0.1mol•L-1的氯化钠溶液,醋酸的电离程度增大 |
| B.V1LpH=11的NaOH溶液与V2LpH=3的HA溶液混合,若混合液显中性,则V1≤V2 |
| C.体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量),前者用时少 |
| D.在Mg(OH)2悬浊液中加入少量NH4Cl固体,c(Mg2+)增大 |
您最近一年使用:0次
解题方法
8 . 探究某酸HR是否为弱酸,下列说法不正确的是
| A.加热NaR溶液时,溶液的pH变小,则HR为弱酸 |
B.25℃时,向 溶液中加入 溶液中加入 溶液,当水电离的 溶液,当水电离的 ,滴加NaOH溶液的体积可出现两种情况,则HR为弱酸 ,滴加NaOH溶液的体积可出现两种情况,则HR为弱酸 |
C.25℃时测NaR溶液的pH,若 ,则HR为弱酸 ,则HR为弱酸 |
D.25℃时, 的HR和 的HR和 的 的 溶液等体积混合后,溶液显酸性,则HR为弱酸 溶液等体积混合后,溶液显酸性,则HR为弱酸 |
您最近一年使用:0次
解题方法
9 . 室温下实验室用 的氢氧化钠溶液滴定
的氢氧化钠溶液滴定 醋酸溶液,滴定曲线如图所示(设
醋酸溶液,滴定曲线如图所示(设 )。下列有关叙述正确的是
)。下列有关叙述正确的是
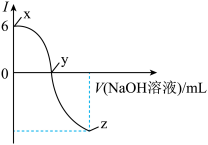
 的氢氧化钠溶液滴定
的氢氧化钠溶液滴定 醋酸溶液,滴定曲线如图所示(设
醋酸溶液,滴定曲线如图所示(设 )。下列有关叙述正确的是
)。下列有关叙述正确的是
| A.该条件下,醋酸的电离度(已电离的醋酸分子数与原醋酸分子数的比)约为1% |
B.y点处加入的NaOH溶液体积小于 |
| C.x→y→z的过程中,水的电离程度逐渐增大 |
D.y→z的曲线上任意一点,始终存在 |
您最近一年使用:0次



