常温下 溶液体系中存在平衡关系:
溶液体系中存在平衡关系: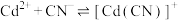 ;
; ;
;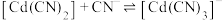 ;
;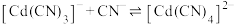 ,平衡常数依次为
,平衡常数依次为 。含
。含 物种的组分分布分数
物种的组分分布分数 、平均配位数
、平均配位数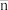 与
与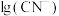 的关系如图所示。已知
的关系如图所示。已知 ,
,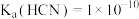 ;
;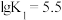 ,
,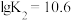 ,
, ,
, 。
。
 溶液体系中存在平衡关系:
溶液体系中存在平衡关系: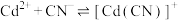 ;
; ;
;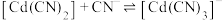 ;
;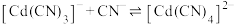 ,平衡常数依次为
,平衡常数依次为 。含
。含 物种的组分分布分数
物种的组分分布分数 、平均配位数
、平均配位数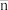 与
与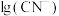 的关系如图所示。已知
的关系如图所示。已知 ,
,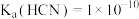 ;
;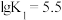 ,
,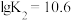 ,
, ,
, 。
。
A.随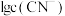 增大,水的电离程度减小 增大,水的电离程度减小 |
B. 时, 时,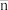 约为3 约为3 |
C.a点时,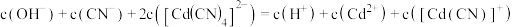 |
D.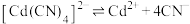 的平衡常数的 的平衡常数的 |
更新时间:2024-04-15 14:24:06
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】T ℃时,某1 L恒容密闭容器中存在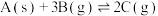 的反应,测得部分数据如表所示:
的反应,测得部分数据如表所示:
下列说法错误的是
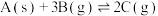 的反应,测得部分数据如表所示:
的反应,测得部分数据如表所示:| 物质 | A | B | C |
| 初始量/mol | 0.2 | 0.3 | 0 |
| 4 min末量/mol | 0.12 | b | c |
| 平衡量/mol | a | d | 0.18 |
A.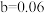 |
B.T ℃时,该反应的平衡常数为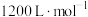 |
| C.若升高温度后C的平衡产率增大,则该反应是放热反应 |
| D.若向容器中再加入一定量A,平衡后C的体积分数增大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
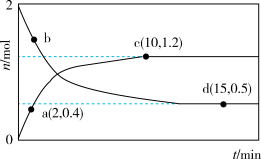
【推荐2】在160℃、200℃条件下,分别向两个容积为2L的刚性容器中充入2molCO(g)和2molN2O(g),发生反应:CO(g)+N2O(g) CO2(g)+N2(g) ΔH<0。实验测得两容器中CO或N2的物质的量随时间的变化关系如图所示。下列说法正确的是
CO2(g)+N2(g) ΔH<0。实验测得两容器中CO或N2的物质的量随时间的变化关系如图所示。下列说法正确的是
 CO2(g)+N2(g) ΔH<0。实验测得两容器中CO或N2的物质的量随时间的变化关系如图所示。下列说法正确的是
CO2(g)+N2(g) ΔH<0。实验测得两容器中CO或N2的物质的量随时间的变化关系如图所示。下列说法正确的是
| A.CO的转化率:d﹥c |
| B.ac段N2的平均反应速率为0.10mol/(L·min) |
| C.该反应达到平衡状态时c(CO)+c(CO2)=2mol/L |
| D.200℃时,该反应的平衡常数Kc=2.25 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】在一定条件下,下列叙述与图像对应正确的是
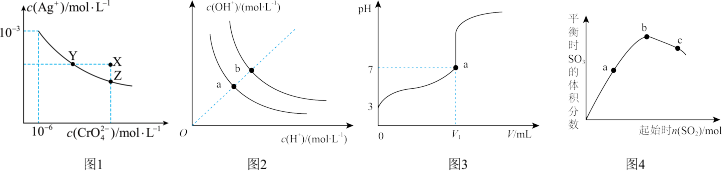

A.图1表示T℃时, 在水溶液中的沉淀溶解平衡曲线, 在水溶液中的沉淀溶解平衡曲线, 的 的 为 为 |
B.图2表示不同温度下水中 和 和 的浓度变化曲线,图中a点对应温度低于b点 的浓度变化曲线,图中a点对应温度低于b点 |
C.图3表示某温度下向 溶液中逐滴加入NaOH溶液,该滴定过程宜选用甲基橙作指示剂 溶液中逐滴加入NaOH溶液,该滴定过程宜选用甲基橙作指示剂 |
D.图4表示在一定温度下,改变起始时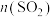 对反应 对反应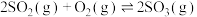 的影响,a、b、c三点中,a点时 的影响,a、b、c三点中,a点时 的转化率最大 的转化率最大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】常温下,向10.00mL浓度均为 的NaOH溶液和二甲胺
的NaOH溶液和二甲胺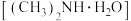 的混合溶液中逐滴加入盐酸。利用传感器测得该过程溶液中的阳离子总浓度变化曲线如图;已知二甲胺在水中电离与氨相似,常温下
的混合溶液中逐滴加入盐酸。利用传感器测得该过程溶液中的阳离子总浓度变化曲线如图;已知二甲胺在水中电离与氨相似,常温下 。下列说法正确的是
。下列说法正确的是

 的NaOH溶液和二甲胺
的NaOH溶液和二甲胺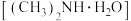 的混合溶液中逐滴加入盐酸。利用传感器测得该过程溶液中的阳离子总浓度变化曲线如图;已知二甲胺在水中电离与氨相似,常温下
的混合溶液中逐滴加入盐酸。利用传感器测得该过程溶液中的阳离子总浓度变化曲线如图;已知二甲胺在水中电离与氨相似,常温下 。下列说法正确的是
。下列说法正确的是
| A.从a到c的过程中,水的电离程度最大的是c点 |
B.a点溶液中,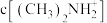 约为 约为 |
C.c点溶液中: |
D. 时, 时, |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列溶液中浓度关系正确的是
A.小苏打溶液中:c(Na+)+ c(H+)= +c(OH-) +c(OH-) |
| B.常温时,将0.1 mol/L的CH3COOH溶液加水稀释后,溶液的pH降低,水的电离程度增加 |
| C.0.1 mo/L的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(A2-)>c(H2A) |
| D.物质的量浓度相等的CH3COOH溶液和CH3COONa溶液等体积混合:c (CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】常温下, 电离常数为
电离常数为 ,二元酸亚磷酸
,二元酸亚磷酸 的电离常数
的电离常数 ,
, 。若温度均为常温且忽略反应过程中的温度变化,下列说法正确的是
。若温度均为常温且忽略反应过程中的温度变化,下列说法正确的是
 电离常数为
电离常数为 ,二元酸亚磷酸
,二元酸亚磷酸 的电离常数
的电离常数 ,
, 。若温度均为常温且忽略反应过程中的温度变化,下列说法正确的是
。若温度均为常温且忽略反应过程中的温度变化,下列说法正确的是A. 溶液中, 溶液中, |
B.向 的氨水中滴加等浓度的 的氨水中滴加等浓度的 溶液,加入 溶液,加入 溶液时,水的电离程度达到最大值 溶液时,水的电离程度达到最大值 |
C. 溶液中, 溶液中, |
D. 属于正盐,其水溶液显碱性 属于正盐,其水溶液显碱性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】常温下,向20.00mL 0.1000 mol ·L-1CH3COONa溶液中逐滴加入0.1000 mol ·L-1盐酸,溶液的pH与所加盐酸体积的关系如下图所示(不考虑挥发)。下列说法正确的是


| A.点①所示溶液中:c(CH3COOH)=c(Cl-)>c(OH-)=c(H+) |
| B.点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) |
| C.点③所示溶液中:c(Na+)>c(CH3COOH)>c(H+)>c(CH3COO-) |
| D.整个过程中可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-) |
您最近一年使用:0次



 的
的 溶液中加入下列物质,对所得溶液的分析正确的是
溶液中加入下列物质,对所得溶液的分析正确的是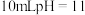 的
的 溶液
溶液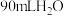
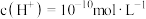
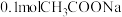 固体
固体 比原
比原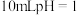 的
的 溶液
溶液

