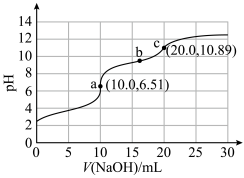
1 . 向10mLHCOOH-NH4Cl混合溶液(浓度均为0.1mol·L−1)中滴加0.1mol·L−1NaOH溶液,并监测溶液pH变化,实验数据如图。由该实验可得到的结论是
| A.HCOOH电离方程式为HCOOH=H++HCOO− |
| B.由a点数据可推出电离能力:HCOOH>NH3·H2O |
| C.b点溶液中的OH−主要来自HCOO−水解 |
| D.0.05mol·L−1氨水的pH<10.89 |
您最近一年使用:0次
2024-04-13更新
|
479次组卷
|
3卷引用:湖南省衡阳县第四中学2023-2024学年高三下学期4月月考化学试题
名校
2 . 无水FeCl2为黄绿色晶体,在空气中易被氧化和易吸水,不溶于氯仿等有机溶剂。回答下列问题:
I.FeCl2的制备及产率测定:制备反应原理为2FeCl3+C6H5Cl 2FeCl2+C6H4Cl2+HCl(C6H5Cl为氯苯,沸点132℃),产率通过测定HCl的量进行计算。制备装置如图所示(夹持及加热装置略去):
2FeCl2+C6H4Cl2+HCl(C6H5Cl为氯苯,沸点132℃),产率通过测定HCl的量进行计算。制备装置如图所示(夹持及加热装置略去):
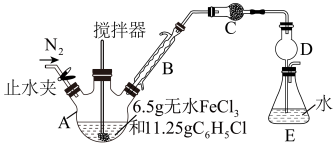
(1)仪器A的名称是____ ,仪器B的作用是____ ,装置C中的试剂是____ (填化学式)。
(2)为测定FeCl2的产率,用1.00mol·L-1NaOH溶液滴定溶于水的HCl,达到滴定终点时消耗NaOH溶液19.00mL,则FeCl2的产率为____ 。下列操作中,导致产率测定值偏低的是____ 。
a.滴定终点时俯视读数
b.滴定管未用NaOH标准溶液润洗
c.配制NaOH标准溶液时,转移溶液未洗涤烧杯
d.滴定前滴定管内无气泡,滴定结束后有气泡
II.FeCl2性质探究:将FeCl2晶体配成溶液后进行如表实验。
已知:Ba2+与SCN-可在溶液中大量共存;SCN-易被氧化为SO 。
。
(3)对实验ⅰ中溶液为浅红色的原因,甲同学提出以下假设:
假设1:加入氯水的量少,生成的Fe3+浓度低;
假设2:氯水氧化性强,____ 。
取实验ⅰ中浅红色溶液,____ (填实验操作),溶液浅红色消失,从而排除了假设1;向2mL水中滴加0.5mL0.1mol·L-1KSCN溶液,滴加0.5mL饱和氯水,加入____ ,产生白色沉淀,说明假设2正确。
(4)分析实验ⅱ“一段时间后,溶液褪为无色”的原因是____ (用离子方程式表示,已知SCN-中C元素为+4价)。
I.FeCl2的制备及产率测定:制备反应原理为2FeCl3+C6H5Cl
 2FeCl2+C6H4Cl2+HCl(C6H5Cl为氯苯,沸点132℃),产率通过测定HCl的量进行计算。制备装置如图所示(夹持及加热装置略去):
2FeCl2+C6H4Cl2+HCl(C6H5Cl为氯苯,沸点132℃),产率通过测定HCl的量进行计算。制备装置如图所示(夹持及加热装置略去):
(1)仪器A的名称是
(2)为测定FeCl2的产率,用1.00mol·L-1NaOH溶液滴定溶于水的HCl,达到滴定终点时消耗NaOH溶液19.00mL,则FeCl2的产率为
a.滴定终点时俯视读数
b.滴定管未用NaOH标准溶液润洗
c.配制NaOH标准溶液时,转移溶液未洗涤烧杯
d.滴定前滴定管内无气泡,滴定结束后有气泡
II.FeCl2性质探究:将FeCl2晶体配成溶液后进行如表实验。
| 序号 | 装置 | 试剂 | 实验现象 | |
| 实验ⅰ |  | 0.5mL0.1mol·L-1 KSCN溶液、1mL0.1mol·L-1 FeCl2(pH=1)溶液 | 0.5mL饱和氯水 | 溶液立即变为浅红色 |
| 实验ⅱ | 1mLl.5mol·L-1 HNO3溶液 | 滴入硝酸后,溶液变为红色,一段时间后,溶液褪为无色,且溶液中产生无色气泡,试管上方呈红棕色。 | ||
 。
。(3)对实验ⅰ中溶液为浅红色的原因,甲同学提出以下假设:
假设1:加入氯水的量少,生成的Fe3+浓度低;
假设2:氯水氧化性强,
取实验ⅰ中浅红色溶液,
(4)分析实验ⅱ“一段时间后,溶液褪为无色”的原因是
您最近一年使用:0次
2022-05-11更新
|
483次组卷
|
3卷引用:湖南省益阳市第一中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
3 . 实验小组用双指示剂法准确测定 样品(杂质为
样品(杂质为 )的纯度。步骤如下:
)的纯度。步骤如下:
①称取m g样品,配制成100mL溶液;
②取出25mL溶液置于锥形瓶中,加入2滴酚酞溶液,用浓度为 的盐酸滴定至溶液恰好褪色(溶质为
的盐酸滴定至溶液恰好褪色(溶质为 和
和 ),消耗盐酸体积为
),消耗盐酸体积为 ;
;
③滴入2滴甲基橙溶液,继续滴定至终点,消耗盐酸体积为 。
。
下列说法正确的是
 样品(杂质为
样品(杂质为 )的纯度。步骤如下:
)的纯度。步骤如下:①称取m g样品,配制成100mL溶液;
②取出25mL溶液置于锥形瓶中,加入2滴酚酞溶液,用浓度为
 的盐酸滴定至溶液恰好褪色(溶质为
的盐酸滴定至溶液恰好褪色(溶质为 和
和 ),消耗盐酸体积为
),消耗盐酸体积为 ;
;③滴入2滴甲基橙溶液,继续滴定至终点,消耗盐酸体积为
 。
。下列说法正确的是
| A.①中配制溶液时,需在容量瓶中加入100mL水 |
B.②中溶液恰好褪色时: |
C. 样品纯度为 样品纯度为 |
| D.配制溶液时放置时间过长,会导致最终测定结果偏高 |
您最近一年使用:0次
2022-04-01更新
|
1438次组卷
|
15卷引用:湖南省武冈市第一中学2021-2022学年高三下学期第三次模拟考试化学试题
湖南省武冈市第一中学2021-2022学年高三下学期第三次模拟考试化学试题湖南省长沙市第一中学2022-2023学年高三上学期月考卷(五)化学试题北京市海淀区2022届高三一模化学试题(已下线)第05讲 物质的量浓度及溶液配制 (练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题45 定量测量类综合实验-备战2023年高考化学一轮复习考点微专题山东聊城第二中学2022-2023学年高三上学期期中考试化学试题(已下线)北京市海淀区2022届高三一模(选择题11-14)辽宁省本溪市高级中学2022-2023学年高三上学期期中测试化学试题(已下线)2023年高考山东卷化学真题变式题(选择题6-10)(已下线)第2讲 物质的浓度及溶液配制天津市南开中学2023-2024学年高三上学期统练5化学试题北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题吉林省通化市梅河口市第五中学2023-2024学年高二上学期1月期末化学试题辽宁省葫芦岛市第一高级中学2023-2024学年高二上学期化学期末复习提升卷
解题方法
4 . 常温时,采用甲基橙和酚酞双指示剂,用盐酸滴定 溶液﹐溶液中
溶液﹐溶液中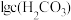 、
、 、
、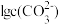 、
、 、
、 随溶液pH的变化及滴定曲线如图所示:
随溶液pH的变化及滴定曲线如图所示:

下列说法不正确的是
 溶液﹐溶液中
溶液﹐溶液中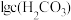 、
、 、
、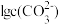 、
、 、
、 随溶液pH的变化及滴定曲线如图所示:
随溶液pH的变化及滴定曲线如图所示:
下列说法不正确的是
| A.整个滴定过程中可先用酚酞再用甲基橙作指示剂 |
| B.n点的pH为m点和q点pH的平均值 |
C.r点溶液中: |
| D.r点到k点对应的变化过程中,溶液中水的电离程度先减小后增大 |
您最近一年使用:0次
2021-05-20更新
|
565次组卷
|
2卷引用:湖南省永州市省重点中学2021届高三5月联考化学试题
2021·全国·模拟预测
名校
解题方法
5 . 电位滴定是利用溶液电位突变指示终点的滴定法。常温下,用cmol·L−1HCl标准溶液测定VmL某生活用品中Na2CO3的含量(假设其它物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位与V(HCl)的关系如图所示。已知:两个滴定终点时消耗盐酸的体积差可计算出Na2CO3的量。
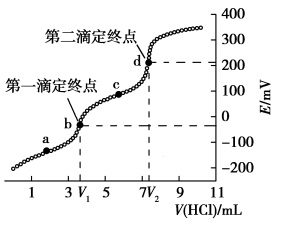
下列说法正确的是

下列说法正确的是
A.a至c点对应溶液中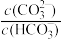 逐渐增大 逐渐增大 |
| B.水的电离程度:a>b>d>c |
C.a溶液中存在:c(Na+)+c(H+)=c( )+2c( )+2c( )+c(OH−) )+c(OH−) |
| D.VmL生活用品中含有Na2CO3的质量为0.106c(V2−V1)g |
您最近一年使用:0次
2021-05-14更新
|
1904次组卷
|
15卷引用:2021年湖南省高考化学试卷变式题1-10
2021年湖南省高考化学试卷变式题1-10湖南师范大学附属中学2021-2022学年高三下学期高考模拟(一)化学试题湖南省岳阳县第一中学2022届高三下学期5月月考化学试题(已下线)化学-学科网2021年高三5月大联考(新课标Ⅰ卷)(已下线)化学-学科网2021年高三5月大联考(新课标Ⅲ卷)(已下线)2021年高考化学押题预测卷(广东卷)(03)(已下线)化学-学科网2021年高三5月大联考(新课标Ⅱ卷)(已下线)专题19 沉淀溶解平衡的图像问题分析-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)辽宁省东北育才学校高中部高三2021-2022下学期开学初第六次模拟考试化学试题辽宁省沈阳市第五中学2021-2022学年高三下学期3月月考化学试题福建省龙岩第一中学2022届高三毕业班模拟训练(二)化学试题(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)江西省南昌市八一中学2022届高三下学期第三次模拟考试理科综合化学试题辽宁省沈阳市第二中学2022-2023学年高三上学期12月阶段测试化学试题巩固训练10



