名校
解题方法
1 . 下表中根据实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 常温下,向 的醋酸溶液中加入少量醋酸铵固体,溶液的pH变大 的醋酸溶液中加入少量醋酸铵固体,溶液的pH变大 | 检验醋酸铵溶液的酸碱性 |
| B | 向 溶液中滴加酸性 溶液中滴加酸性 溶液, 溶液, 溶液褪色 溶液褪色 | 证明 具有还原性 具有还原性 |
| C | 分别用pH试纸测定同浓度的 溶液和 溶液和 溶液的pH 溶液的pH | 酸性: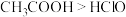 |
| D | 分别测定同浓度 溶液和 溶液和 溶液的导电性 溶液的导电性 | 证明 是弱电解质 是弱电解质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-18更新
|
356次组卷
|
3卷引用:安徽省宣城市2022-2023学年高二上学期11月期中化学试题
2 . 常温下,下列事实能说明HClO是弱电解质的是
| A.HClO溶液的导电能力弱 | B.HClO易溶于水 |
| C.HClO有强氧化性 | D.NaClO溶液呈碱性 |
您最近一年使用:0次
2022-12-04更新
|
140次组卷
|
3卷引用:上海市奉贤区致远高级中学2021-2022学年高二上学期期中教学评估(等级考)化学试题
3 . 下列叙述 I 和叙述 II 均正确且因果关系也一定正确的是
| 选项 | 叙述 I | 叙述 II |
| A | 用pH计分别 测定SO2 和CO2溶于水形成溶液的 p H,前者pH小 | 说明H2SO 3 酸性强于H2CO3 |
| B | SiO2是酸性氧化物 | SiO2 不与任何酸溶液反应 |
| C | Sn 2+容易水解且在空气中能氧化为Sn 4+ | 配制SnCl2溶液时,先将SnCl2溶于适量稀盐酸中,再用蒸馏水稀释,保存时再在试剂瓶中加入入少量锡粒 |
| D | 浓硫酸具有强氧化性 | 浓硫酸能使滤纸变黑 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 将物质分门别类,更有利于物质的研究。下列有关物质分类的说法不正确的是
| A.烧碱、熟石灰均属于碱 |
| B.漂白粉与漂白液均为混合物 |
| C.H2SO4、NaOH均属于强电解质,也都属于离子化合物 |
| D.HClO、HNO3均具有氧化性,都是氧化性酸 |
您最近一年使用:0次
5 . 下列关于弱电解质的电离平衡常数的叙述中,正确的是
| A.弱电解质的电离平衡常数就是电解质溶于水后电离出的各种离子浓度的乘积与未电离分子的浓度的比值 |
| B.弱电解质的电离平衡常数只与弱电解质本身的性质及外界温度有关 |
| C.同一温度下,弱酸的电离平衡常数越大,酸性越强;弱碱的电离平衡常数越大,碱性越弱 |
| D.多元弱酸的各级电离平衡常数相同 |
您最近一年使用:0次
2023-08-14更新
|
515次组卷
|
3卷引用:新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期期中考试化学试卷
6 . A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。

(1)若A的焰色反应为黄色,且A为化合物,回答下列问题:
①A的化学式为___________ ,A与H2O反应的离子方程式为___________ 。
②若X为具有强还原性的非金属单质,通常为黑色粉末,写出E的化学式___________ 。
③若X为一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液,可选择的试剂为___________ (填代号)。
a. NaOH溶液 b. HCl溶液 c.BaCl2溶液 d. Ca(OH)2溶液
(2)若A为黄绿色气体,具有很强的氧化性,则:
①若C为强电解质,则B的化学式为___________ 。
②X可能为___________ (填代号)。
a. NaHCO3 b. Fe c. Na2SO4 d. Na2CO3
③请写出A与冷的石灰乳反应的离子方程式___________ 。

(1)若A的焰色反应为黄色,且A为化合物,回答下列问题:
①A的化学式为
②若X为具有强还原性的非金属单质,通常为黑色粉末,写出E的化学式
③若X为一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液,可选择的试剂为
a. NaOH溶液 b. HCl溶液 c.BaCl2溶液 d. Ca(OH)2溶液
(2)若A为黄绿色气体,具有很强的氧化性,则:
①若C为强电解质,则B的化学式为
②X可能为
a. NaHCO3 b. Fe c. Na2SO4 d. Na2CO3
③请写出A与冷的石灰乳反应的离子方程式
您最近一年使用:0次
名校
解题方法
7 . 下列实验方案的设计和实验目的都正确的是
| 选项 | 实验方案 | 实验目的 |
| A | 将草酸滴加到少量 溶液中,通过观察现象 溶液中,通过观察现象 | 证明 是弱电解质 是弱电解质 |
| B | 向两支试管中各加入1mL1mol/L的酸性 溶液,再向两支试管分别加入2mL1mol/L的 溶液,再向两支试管分别加入2mL1mol/L的 溶液和2mL0.5mol/L的 溶液和2mL0.5mol/L的 溶液,记录高锰酸钾溶液褪色所需时间 溶液,记录高锰酸钾溶液褪色所需时间 | 探究草酸浓度对反应速率影响 |
| C | 向锥形瓶中移入25.00mLHCl溶液,加入2滴酚酞,用标准液NaOH滴定至溶液呈浅红色,且半分钟不褪色,此时单手持滴定管上端并保持其自然垂直读取示数 | 测定HCl浓度 |
| D | 先向三只试管中各加入1mL等浓度 溶液,再同时向三只试管中加入等体积、pH相同的HCl、 溶液,再同时向三只试管中加入等体积、pH相同的HCl、 、 、 溶液,观察现象 溶液,观察现象 | 证明 和酸是否发生歧化反应与阴离子种类无关 和酸是否发生歧化反应与阴离子种类无关 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-25更新
|
160次组卷
|
2卷引用:湖北省武汉市东华中师范大学第一附属中学2023-2024学年高二上学期11月期中化学试题
8 . 在25℃时,将酸HA与碱MOH等体积混合。
(1)若0.01mol/L的强酸HA与0.01mol/L强碱MOH混合,则所得溶液显_______ (填“酸性”、“中性”或“碱性”,下同)。
(2)若pH=3的强酸HA与pH=11的弱碱MOH混合,则所得溶液显__________ 。
(3)若0.01mol/L的强酸HA与0.01mol/L弱碱MOH混合,则所得溶液显__________ ,解释这一现象的离子方程式是__________________________ 。
(1)若0.01mol/L的强酸HA与0.01mol/L强碱MOH混合,则所得溶液显
(2)若pH=3的强酸HA与pH=11的弱碱MOH混合,则所得溶液显
(3)若0.01mol/L的强酸HA与0.01mol/L弱碱MOH混合,则所得溶液显
您最近一年使用:0次



