名校
解题方法
1 . 下列说法不正确 的是
A.测定0.1 醋酸溶液的 醋酸溶液的 可证明醋酸是弱电解质 可证明醋酸是弱电解质 |
| B.稀释氨水,溶液中c(OH-)减小 |
C.常温下,将1  的盐酸稀释至1L, 的盐酸稀释至1L, 约为 约为 |
D.相同温度下,中和相同 、相同体积的盐酸和醋酸溶液,消耗 、相同体积的盐酸和醋酸溶液,消耗 物质的量不同 物质的量不同 |
您最近一年使用:0次
名校
2 . 下列说法中,可以证明醋酸是弱电解质的是
| A.醋酸溶液连接到一电路中,发现灯泡较暗 |
B.0.1mol/L醋酸的 |
| C.50mL0.1mol/L的醋酸溶液恰好中和5mLImol/L的NaOH溶液 |
| D.醋酸能使石蕊试纸变红 |
您最近一年使用:0次
名校
3 . 下列说法正确且一定能证明 是弱电解质的是
是弱电解质的是
①25℃时,用pH试纸测 溶液的pH为4
溶液的pH为4
② 水溶液中含有
水溶液中含有 分子和
分子和 、
、
③ 溶液恰好与
溶液恰好与 溶液完全反应
溶液完全反应
④次氯酸不稳定,在光照条件下易分解
⑤用 溶液做导电性实验,灯泡很暗
溶液做导电性实验,灯泡很暗
 是弱电解质的是
是弱电解质的是①25℃时,用pH试纸测
 溶液的pH为4
溶液的pH为4②
 水溶液中含有
水溶液中含有 分子和
分子和 、
、
③
 溶液恰好与
溶液恰好与 溶液完全反应
溶液完全反应④次氯酸不稳定,在光照条件下易分解
⑤用
 溶液做导电性实验,灯泡很暗
溶液做导电性实验,灯泡很暗| A.①② | B.② | C.①③④ | D.②⑤ |
您最近一年使用:0次
2023-12-14更新
|
326次组卷
|
2卷引用:山东省青岛第二中学2023-2024学年高二上学期期中考试化学试卷
名校
4 . 下列说法不正确的是
| A.25 ℃时,0.1 mol·L-1 CH3COOH溶液的pH>1,证明CH3COOH是弱电解质 |
| B.BaSO4的水溶液不易导电,故BaSO4是弱电解质 |
| C.25 ℃时,0.1 mol·L-1的亚硫酸溶液比等浓度的亚硫酸钠溶液的导电能力弱 |
| D.醋酸、一水合氨、水都是弱电解质 |
您最近一年使用:0次
2021-04-21更新
|
225次组卷
|
3卷引用:江苏省南通市海门实验学校2020-2021学年高二上学期期中考试化学试题
名校
5 . 下列有关电解质溶液的说法正确的是
| A.用CH3COOH溶液做导电实验,灯泡很暗,证明CH3COOH是弱电解质 |
| B.pH相同的醋酸和盐酸,取等体积的两种酸溶液分别稀释至原溶液体积的m倍和n倍,稀释后两溶液的pH仍然相同,则m<n |
| C.常温下,CH3COOH的Ka=1.7×10-5,NH3•H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3•H2O的溶液中的c(OH-)相等 |
D.常温下,在0.10mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体, 的值增大且能使溶液的pH减小 的值增大且能使溶液的pH减小 |
您最近一年使用:0次
6 . 某合作学习小组讨论辨析下列说法,其中说法正确的数目为
①离子反应可能是复分解反应,但一定不是氧化还原反应②电解质在水中一定能导电,非电解质在水中一定不导电③CO2的水溶液可以导电,故 CO2是电解质④同温同压下,等质量的二氧化硫气体和二氧化碳气体密度比为 16:11,体积比为 11:16⑤某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
①离子反应可能是复分解反应,但一定不是氧化还原反应②电解质在水中一定能导电,非电解质在水中一定不导电③CO2的水溶液可以导电,故 CO2是电解质④同温同压下,等质量的二氧化硫气体和二氧化碳气体密度比为 16:11,体积比为 11:16⑤某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
2019-11-14更新
|
122次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2019-2020学年高一上学期期中考试化学试题
名校
7 . 下列关于电解质溶液的说法正确的是
| A.25℃时,某浓度的KHA溶液pH=4,则HA-的电离程度大于水解程度,H2A为弱酸 |
| B.常温下,通过测定0.1mol•L-1NH4Cl溶液的酸碱性能证明NH3•H2O是弱电解质 |
| C.同浓度的盐酸和醋酸稀释相同倍数后,盐酸的pH大于醋酸 |
| D.pH=3的CH3COOH 溶液与pH=11的NaOH溶液等体积混合,所得混合溶液中:c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
您最近一年使用:0次
2019-07-02更新
|
289次组卷
|
2卷引用:浙江省诸暨市牌头中学2018-2019学年高一下学期期中考试化学试题
10-11高二上·湖北·期中
解题方法
8 . 甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下:
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入0.1 mol·L-1的 HA、HCl溶液各10 mL,按图装好,观察现象;
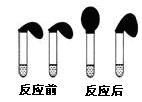
乙:① 用pH计测定物质的量浓度均为0.1 mol·L-1 HA和HCl溶液的pH;
② 再取0.1 mol·L-1的HA和HCl溶液各2滴(1滴约为1/25 mL)分别稀释至100 mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol·L-1的HA溶液的pH_________ 1(填“>”、“<”或“=”) ;甲方案中,说明HA是弱电解质的实验现象是:__________
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后, 试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第______ 步,能证明改变条件弱电解质平衡发生移动。甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1 mol·L-1的HA溶液中,选择加入_________ 试剂(选填“A”“B”“C”“D”,下同);②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol·L-1的HA溶液中,选择加入_____ 试剂。
A. NaA固体(可完全溶于水) B.1 mol·L-1 NaOH溶液
C. 1 mol·L-1 H2SO4 D.2 mol·L-1 HA
(3)pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的有_______

A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
E.稀释后A溶液中水的电离程度比B溶液中水的电离程度小
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入0.1 mol·L-1的 HA、HCl溶液各10 mL,按图装好,观察现象;

乙:① 用pH计测定物质的量浓度均为0.1 mol·L-1 HA和HCl溶液的pH;
② 再取0.1 mol·L-1的HA和HCl溶液各2滴(1滴约为1/25 mL)分别稀释至100 mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol·L-1的HA溶液的pH
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后, 试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
A. NaA固体(可完全溶于水) B.1 mol·L-1 NaOH溶液
C. 1 mol·L-1 H2SO4 D.2 mol·L-1 HA
(3)pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的有

A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
E.稀释后A溶液中水的电离程度比B溶液中水的电离程度小
您最近一年使用:0次
名校
9 . 磷能形成次磷酸 、亚磷酸
、亚磷酸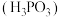 、磷酸
、磷酸 等多种含氧酸,完成下列问题。
等多种含氧酸,完成下列问题。
(1)①已知 是一元弱酸,书写
是一元弱酸,书写 的电离方程式:
的电离方程式:_______ 。
②以下可以证明 是弱酸的是
是弱酸的是_______ 。
A. 溶液与碳酸钙反应,缓慢放出二氧化碳
溶液与碳酸钙反应,缓慢放出二氧化碳
B. 溶液导电能力很弱
溶液导电能力很弱
C.常温时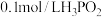 溶液的
溶液的 大于1
大于1
D. 溶液可以使石蕊变红
溶液可以使石蕊变红
(2)亚磷酸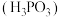 是二元弱酸,
是二元弱酸, 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(3)磷酸 是三元弱酸,
是三元弱酸, 溶液中含磷酸根浓度由大到小排第二位的微粒符号是
溶液中含磷酸根浓度由大到小排第二位的微粒符号是_______ 。
 、亚磷酸
、亚磷酸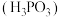 、磷酸
、磷酸 等多种含氧酸,完成下列问题。
等多种含氧酸,完成下列问题。(1)①已知
 是一元弱酸,书写
是一元弱酸,书写 的电离方程式:
的电离方程式:②以下可以证明
 是弱酸的是
是弱酸的是A.
 溶液与碳酸钙反应,缓慢放出二氧化碳
溶液与碳酸钙反应,缓慢放出二氧化碳 B.
 溶液导电能力很弱
溶液导电能力很弱C.常温时
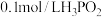 溶液的
溶液的 大于1
大于1 D.
 溶液可以使石蕊变红
溶液可以使石蕊变红(2)亚磷酸
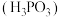 是二元弱酸,
是二元弱酸, 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:(3)磷酸
 是三元弱酸,
是三元弱酸, 溶液中含磷酸根浓度由大到小排第二位的微粒符号是
溶液中含磷酸根浓度由大到小排第二位的微粒符号是
您最近一年使用:0次
10 . 下列事实中一定能证明 是弱电解质的是
是弱电解质的是
①用 溶液做导电实验,灯泡很暗
溶液做导电实验,灯泡很暗
②常温下, 溶液的
溶液的
③等pH等体积的硫酸、 溶液分别和足量锌反应,
溶液分别和足量锌反应, 放出的氢气较多
放出的氢气较多
④20mL0.2mol·L-1醋酸溶液恰好与 溶液完全反应
溶液完全反应
⑤ 的
的 溶液稀释至1000倍,
溶液稀释至1000倍,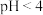
 是弱电解质的是
是弱电解质的是①用
 溶液做导电实验,灯泡很暗
溶液做导电实验,灯泡很暗②常温下,
 溶液的
溶液的
③等pH等体积的硫酸、
 溶液分别和足量锌反应,
溶液分别和足量锌反应, 放出的氢气较多
放出的氢气较多④20mL0.2mol·L-1醋酸溶液恰好与
 溶液完全反应
溶液完全反应⑤
 的
的 溶液稀释至1000倍,
溶液稀释至1000倍,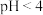
| A.①②④⑤ | B.②③⑤ | C.①②③④⑤ | D.①②⑤ |
您最近一年使用:0次
2023-11-14更新
|
455次组卷
|
3卷引用:浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题



