1 . 为了探究温度对水解平衡的影响,用手持技术测定一定浓度 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是
 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是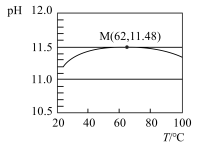
| A.该实验能证明升温促进水解 | B.点M之后 水解放热 水解放热 |
C.点M处溶液中 略大于 略大于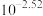 mol/L mol/L | D.点M后pH下降是因为升温对 的影响更大 的影响更大 |
您最近一年使用:0次
解题方法
2 . 某实验小组研究FeCl3溶液与Na2SO3溶液之间的反应,进行如下实验探究:
查阅资料:
| 编号 | 实验试剂及用量 | 开始混合时现象 | 30min时 | 3天后 |
| I | 取1.0mol/LFeCl3溶液2mL滴加1.0mol/LNa2SO3溶液2滴 | 溶液立即变为红色 | 红色明显变浅 | 溶液呈黄绿色 | |
| Ⅱ | 取1.0mol/LNa2SO3溶液2mL滴加1.0mol/LFeCl3溶液2滴 | 溶液立即变为红色,比I中略浅 | 与开始混合时一致 | 溶液呈黄绿色 |

| A.配制 FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度是为了抑制Fe3+的水解 |
| B.上述实验在开始混合时观察到的现象不涉及氧化还原反应,实验Ⅱ中红色比I中略浅的原因可能是Fe3+起始浓度小 |
| C.1~30min立即变红,随后变浅,证明生成红色配合物速率较快,红色配合物生成橙色配合物速率较慢 |
| D.取黄绿色溶液先滴加HCl溶液,再滴加BaCl2溶液,出现白色沉淀,可证明FeCl3溶液与Na2SO3溶液发生了氧化还原反应 |
您最近一年使用:0次
名校
解题方法
3 . 室温下,通过下列实验探究NaHS溶液的性质。
实验1:向0.1 mol/L NaHS溶液中滴加几滴酚酞试剂,溶液变红
实验2:向0.1 mol/L NaHS溶液中通入过量氯气,无淡黄色沉淀产生
实验3:向0.1 mol/L NaHS溶液中加入等体积0.1 mol/L NaOH溶液充分混合
实验4:向0.1 mol/L NaHS溶液中滴加过量 溶液,产生黑色沉淀
溶液,产生黑色沉淀
下列有关说法正确的是
实验1:向0.1 mol/L NaHS溶液中滴加几滴酚酞试剂,溶液变红
实验2:向0.1 mol/L NaHS溶液中通入过量氯气,无淡黄色沉淀产生
实验3:向0.1 mol/L NaHS溶液中加入等体积0.1 mol/L NaOH溶液充分混合
实验4:向0.1 mol/L NaHS溶液中滴加过量
 溶液,产生黑色沉淀
溶液,产生黑色沉淀下列有关说法正确的是
A.实验1证明: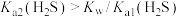 |
B.实验2证明: 不能被 不能被 氧化 氧化 |
C.实验3中所得溶液中: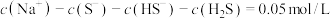 |
D.实验4反应静置后的上层清液中有 |
您最近一年使用:0次
2023-01-08更新
|
571次组卷
|
3卷引用:江苏省决胜新高考2023届高三上学期12月大联考化学试题
名校
4 . 室温下,通过下列实验探究NaHS溶液的性质。
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 向0.1mol•L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红 |
| 2 | 向0.1mol•L-1NaHS溶液中加入等体积0.1mol•L-1NaOH溶液充分混合 |
| 3 | 向0.1mol•L-1NaHS溶液中通入过氯气,无淡黄色沉淀产生 |
| 4 | 向0.1mol•L-1NaHS溶液中滴加过CuCl2溶液,产生黑色沉淀 |
| A.0.1mol/LNaHS溶液中:c(HS-)>c(S2-)>c(H2S) |
| B.实验2所得溶液中:c(Na+)-c(S2-)-c(HS-)-c(H2S)=0.05mol•L-1 |
| C.实验3证明HS-不能被氧化 |
| D.实验4反应静置后的上层清液中有c(Cu2+)•c(S2-)<Ksp(CuS) |
您最近一年使用:0次
2021-12-22更新
|
643次组卷
|
8卷引用:江苏省姜堰中学、如东中学、前黄中学三校2021- 2022学年高三联考化学试题
江苏省姜堰中学、如东中学、前黄中学三校2021- 2022学年高三联考化学试题江苏省前黄高级中学、如东中学、姜堰中学2021-2022学年高三上学期12月份阶段性测试化学试题(已下线)解密10 水溶液中的离子平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)江苏省徐州市第七中学2021-2022学年高三下学期2月检测化学试题(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)江苏省盐城市东台创新高级中学2021-2022学年高二4月份月检测化学试题江苏省盐城市东台创新高级中学2021-2022学年高二下学期5月份月检测化学试题
名校
解题方法
5 . 25°C时,下列说法不正确的是
| A.等体积Na2CO3和NaHCO3溶液,以甲基橙作指示剂,达滴定终点时,消耗等量的HCl标准液,则NaHCO3浓度更大 |
| B.欲证明HA为弱酸,可将pH=3的HA溶液稀释为原体积的10倍后,测定pH>4 |
C.均为0.10 mol·L-1的Na2CO3、Na2SO3、Na2SO4溶液中阴离子的浓度依次减小〔已知:Ka(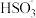 )=6.1×10-8;Ka( )=6.1×10-8;Ka( )=4.7×10-11〕 )=4.7×10-11〕 |
| D.常温下pH=11的纯碱溶液中水电离产生的n(H+)大于该溶液中n(H+) |
您最近一年使用:0次
2021-09-06更新
|
529次组卷
|
4卷引用:江西省南昌市2022届高三摸底考试化学试题
解题方法
6 . 室温下,下列说法不正确的是
| A.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na):③>②>① |
B.0.01mo/LNH4HSO4溶液中离子浓度:c(H+)>c( )>c( )>c( )>c(OH-) )>c(OH-) |
| C.向NaHS溶液中加入等物质的量的KOH后:c(Na+)=c(H2S)+c(HS-)+c(S2-) |
| D.向含白色ZnS的悬浊液中滴入几滴CuSO4溶液,产生黑色沉淀可证明Ksp(ZnS)>Ksp(CuS) |
您最近一年使用:0次
7 . 下列有关元素及其化合物的说法正确的是
| A.古代青铜器表面的铜锈是铜在空气中缓慢氧化生成的氧化物,可溶于盐酸 |
| B.往少量水润湿的蔗糖中注入浓硫酸后,白色固体变为黑色,体现了浓硫酸的脱水性 |
C.将 产品溶于足量稀硫酸后,再滴入 产品溶于足量稀硫酸后,再滴入 溶液,若 溶液,若 溶液褪色,则证明 溶液褪色,则证明 产品中含有 产品中含有 |
D.铵根离子在溶液中水解产生 ,则所有铵盐溶液都呈酸性 ,则所有铵盐溶液都呈酸性 |
您最近一年使用:0次
解题方法
8 . 根据实验目的,下列方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 检验铁锈中是否含 | 将铁锈溶于浓盐酸,滴入 溶液 溶液 | 紫色褪去,铁锈中含有 |
| B | 比较 和 和 的水解常数 的水解常数 | 分别测浓度均为 的 的 和 和 溶液的pH 溶液的pH | 后者大于前者,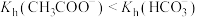 |
| C | 探究温度对反应速率的影响 | 等体积、等物质的量浓度的 与 与 溶液在不同温度下反应 溶液在不同温度下反应 | 温度高的溶液中先出现浑浊,温度升高,该反应速率加快 |
| D | 探究1-溴丙烷中含有溴原子 | 向试管中加入1-溴丙烷和20%的K0H溶液,加热,再向反应后的溶液中加入稀硝酸酸化,滴加 溶液 溶液 | 产生淡黄色沉淀,证明1-溴丙烷中含有溴原子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 化学是以实验为基础的科学。下列实验操作正确且能达到相应实验目的的是
选项 | 实验目的 | 实验操作 |
A | 比较氢氟酸和醋酸的酸性强弱 | 分别测定等物质的量浓度的 和 和 溶液的 溶液的 ,比较 ,比较 大小 大小 |
B | 证明某补血口服液中含有 | 向口服液中先滴加过量酸性 溶液,再滴加 溶液,再滴加 溶液,出现蓝色沉淀 溶液,出现蓝色沉淀 |
C | 证明蔗糖完全水解 | 向蔗糖溶液中加入少量稀硫酸,水浴加热 ,加氢氧化钠溶液至溶液呈碱性,再加入少量新制的 ,加氢氧化钠溶液至溶液呈碱性,再加入少量新制的 ;继续加热 ;继续加热 ,产生砖红色沉淀 ,产生砖红色沉淀 |
D | 验证 具有强氧化性 具有强氧化性 | 向溶有 的 的 溶液中加入 溶液中加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下列实验方案能达到实验目的的是
选项 | 实验方案 | 实验目的 |
A | 在饱和 | 制备 |
B | 在 | 证明异丙醇的极性比水的弱 |
C | 在酸性 | 探究醛基的还原性 |
D | 测定同浓度的 | 探究 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 溶液中加入
溶液中加入 粉末
粉末 胶体
胶体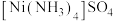 溶液中加入异丙醇
溶液中加入异丙醇 、NaY溶液的pH
、NaY溶液的pH 、HY的酸性强弱
、HY的酸性强弱

