名校
解题方法
1 . 室温下,下列各组离子一定能大量共存的是
A.澄清溶液中: 、 、 、 、 、 、 |
B. 溶液中: 溶液中: 、 、 、 、 、 、 |
C.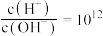 的溶液: 的溶液: 、 、 、 、 、 、 |
D.水电离的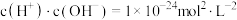 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
2 . 25℃时,下列各组离子在指定溶液中能大量共存的是
A.能使石蕊变红的溶液: , , , , |
B.澄清透明的溶液: , , , , |
C. 的溶液: 的溶液: , , , , |
D.含 的溶液: 的溶液: , , , , |
您最近一年使用:0次
2024-03-02更新
|
98次组卷
|
2卷引用:福建省厦门市2023-2024学年高二上学期期末考试质量检测化学试题
3 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.使甲基橙呈红色的溶液中: |
B.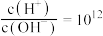 的水溶液中: 的水溶液中: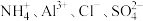 |
C.由水电离出的 的溶液中: 的溶液中: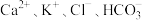 |
D. 的溶液中: 的溶液中: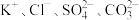 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法不正确的是
A.将 溶液滴入 溶液滴入 溶液中,同时会有气体和沉淀生成 溶液中,同时会有气体和沉淀生成 |
| B.可用红外光谱仪来区分石英玻璃和水晶 |
C.向硫酸铜溶液中滴加过量氨水,形成深蓝色的溶液,是由于生成了 配离子 配离子 |
D.大理石与盐酸反应制取 时,将块状大理石改为粉末状,对增大反应速率有明显效果 时,将块状大理石改为粉末状,对增大反应速率有明显效果 |
您最近一年使用:0次
2024-02-29更新
|
133次组卷
|
3卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题
解题方法
5 . 在下列给定条件的溶液中,一定能大量共存的离子组是
A.中性溶液: 、 、 、 、 、 、 |
B.由水电离的 : : 、 、 、 、 、 、 |
C. 溶液: 溶液: 、 、 、 、 、 、 |
D.常温下,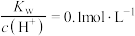 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
6 . 下列有关电极方程式或离子方程式错误的是
A.碱性锌锰电池的正极反应: |
B.铅酸蓄电池充电时的阳极反应: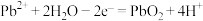 |
C. 溶液滴入 溶液滴入 溶液中: 溶液中: |
D. 溶液和 溶液和 溶液混合: 溶液混合: |
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题。
(1)为探究 与
与 的还原性强弱,取适量制得的
的还原性强弱,取适量制得的 晶体,进行如下实验:
晶体,进行如下实验:
将适量 加入
加入 溶液中,若观察到
溶液中,若观察到___________ ,则可证明还原性 ;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:
;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:___________ 。
(2)为了证明 可以氧化
可以氧化 溶液中的
溶液中的 ,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:___________

(1)为探究
 与
与 的还原性强弱,取适量制得的
的还原性强弱,取适量制得的 晶体,进行如下实验:
晶体,进行如下实验:将适量
 加入
加入 溶液中,若观察到
溶液中,若观察到 ;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:
;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:(2)为了证明
 可以氧化
可以氧化 溶液中的
溶液中的 ,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
您最近一年使用:0次
名校
解题方法
8 . 常温下,下列各组离子在指定溶液中能大量共存的是
| A.pH=13的溶液中:Na+、S2-、Al3+、ClO- |
B.在中性溶液中:K+、Fe3+、Cl-、 |
C.水电离出来的c(H+)=1×10-12的溶液中: 、K+、 、K+、 、Fe2+ 、Fe2+ |
D.弱碱性溶液中可能大量存在Na+、K+、 、 、 |
您最近一年使用:0次
9 . “宏观辨识与微观探析”是化学学科核心素养之一,不能正确表示下列反应的离子方程式是
A.泡沫灭火器原理的离子方程式: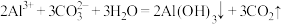 |
B.用过量氨水吸收工业尾气中的 |
C.“胃舒平”消除过多的胃酸: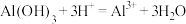 |
D.电解饱和食盐水: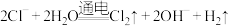 |
您最近一年使用:0次
解题方法
10 . 化学实验是研究物质及其转化的基本方法,是科学探究的一种重要途径。
Ⅰ.为探究不同钠盐对 水解平衡的影响,化学小组设计如下实验。
水解平衡的影响,化学小组设计如下实验。
实验1:常温下,取10.00mL
 溶液置于烧杯中,加入0.01mol的
溶液置于烧杯中,加入0.01mol的 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液 与时间的关系如图1所示。
与时间的关系如图1所示。
实验2:常温下,取10.00mL
 溶液置于烧杯中,加入0.02mol的
溶液置于烧杯中,加入0.02mol的 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液 与时间的关系如图2所示。
与时间的关系如图2所示。

已知:①常温下, 的电离常数为
的电离常数为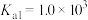 ,
,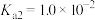 。
。
②在强酸弱碱盐溶液中加入强电解质,溶液中的离子总浓度增大,离子之间的相互牵制作用增强,易水解的阳离子的活性会增强或减弱。
(1) 溶液呈酸性的原因是
溶液呈酸性的原因是______ (用离子方程式表示)。
(2)实验1中20s后溶液的 变化的主要原因为
变化的主要原因为______ 。
(3)实验2中10s后溶液的 变化的主要原因为
变化的主要原因为______ 。
实验结论:不同的钠盐对 溶液水解平衡的影响是不同的。
溶液水解平衡的影响是不同的。
(4)实验讨论:根据上述实验预测向10mL0.1mol/L 中加入少量
中加入少量 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液
______ (填“增大”、“不变”或“减小”)。
Ⅱ.探究Na₂SO₃溶液与溶液的反应原理,某兴趣小组进行了如下实验:
(5)配制
 溶液时;先将
溶液时;先将 固体溶于
固体溶于______ ,再稀释至指定浓度。
(6)针对上述现象,甲同学认为 与
与 发生了相互促进的水解反应得到一种胶体,其离子方程式为
发生了相互促进的水解反应得到一种胶体,其离子方程式为______ ;乙同学认为 与
与 还发生了氧化还原反应,请据此判断两种反应活化能较小的是
还发生了氧化还原反应,请据此判断两种反应活化能较小的是______ (填“水解反应”或“氧化还原反应”)。
提示:经查阅资料和进一步实验探究,证实了 与
与 既发生了水解反应又发生了氧化还原反应。
既发生了水解反应又发生了氧化还原反应。
Ⅰ.为探究不同钠盐对
 水解平衡的影响,化学小组设计如下实验。
水解平衡的影响,化学小组设计如下实验。实验1:常温下,取10.00mL

 溶液置于烧杯中,加入0.01mol的
溶液置于烧杯中,加入0.01mol的 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液 与时间的关系如图1所示。
与时间的关系如图1所示。实验2:常温下,取10.00mL

 溶液置于烧杯中,加入0.02mol的
溶液置于烧杯中,加入0.02mol的 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液 与时间的关系如图2所示。
与时间的关系如图2所示。
已知:①常温下,
 的电离常数为
的电离常数为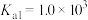 ,
,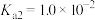 。
。②在强酸弱碱盐溶液中加入强电解质,溶液中的离子总浓度增大,离子之间的相互牵制作用增强,易水解的阳离子的活性会增强或减弱。
(1)
 溶液呈酸性的原因是
溶液呈酸性的原因是(2)实验1中20s后溶液的
 变化的主要原因为
变化的主要原因为(3)实验2中10s后溶液的
 变化的主要原因为
变化的主要原因为实验结论:不同的钠盐对
 溶液水解平衡的影响是不同的。
溶液水解平衡的影响是不同的。(4)实验讨论:根据上述实验预测向10mL0.1mol/L
 中加入少量
中加入少量 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液
Ⅱ.探究Na₂SO₃溶液与溶液的反应原理,某兴趣小组进行了如下实验:
装置 | 现象 |
| 现象ⅰ:一开始液体颜色加深,由棕黄色变为红褐色。 现象ⅱ:一段时间后液体颜色变浅,变为浅黄色。 |
(5)配制

 溶液时;先将
溶液时;先将 固体溶于
固体溶于(6)针对上述现象,甲同学认为
 与
与 发生了相互促进的水解反应得到一种胶体,其离子方程式为
发生了相互促进的水解反应得到一种胶体,其离子方程式为 与
与 还发生了氧化还原反应,请据此判断两种反应活化能较小的是
还发生了氧化还原反应,请据此判断两种反应活化能较小的是提示:经查阅资料和进一步实验探究,证实了
 与
与 既发生了水解反应又发生了氧化还原反应。
既发生了水解反应又发生了氧化还原反应。
您最近一年使用:0次