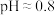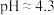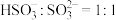解题方法
1 . 采用硫磺熏蒸处理药材会产生一定量的硫残留(其中S元素为+4价),以下是一种简便且准确的分析测定硫含量的方法。
Ⅰ.样品预处理(均在室温下进行):
对xg药材进行处理后,将逸出的 全部收集溶于水形成溶液X。加NaOH溶液将溶液X调为
全部收集溶于水形成溶液X。加NaOH溶液将溶液X调为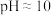 ,此时溶液总体积为V mL(记为溶液Y)。
,此时溶液总体积为V mL(记为溶液Y)。
资料:不同pH下,含硫微粒在溶液中的主要存在形式:
(1) 溶于水后溶液显酸性,用化学用语表示其原因:
溶于水后溶液显酸性,用化学用语表示其原因:___________ 。
(2)用少量NaOH溶液将X溶液pH调至4.3的过程中发生反应的离子方程式是___________ 。
(3)将X溶液pH调至10时, 与消耗的NaOH物质的量之比
与消耗的NaOH物质的量之比
___________ 。
(4)关于室温下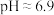 的溶液说法正确的是
的溶液说法正确的是___________ 。
a.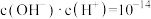
b.
c.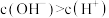
Ⅱ.电化学测定:利用如图电解装置进行测定。
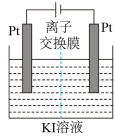
通电片刻后停止通电,加入淀粉溶液。根据电流大小和电解效率理论计算共产生 。用溶液Y对停止通电后的阳极区电解质溶液进行滴定,到达终点时,共用去
。用溶液Y对停止通电后的阳极区电解质溶液进行滴定,到达终点时,共用去 。
。
(5)阳极的电极反应式是___________ 。
(6)确定滴定终点的现象是___________ 。
(7)药材中硫残留量(其中含硫微粒均按 计,
计,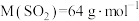 )为
)为___________ mg/g。
Ⅰ.样品预处理(均在室温下进行):
对xg药材进行处理后,将逸出的
 全部收集溶于水形成溶液X。加NaOH溶液将溶液X调为
全部收集溶于水形成溶液X。加NaOH溶液将溶液X调为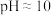 ,此时溶液总体积为V mL(记为溶液Y)。
,此时溶液总体积为V mL(记为溶液Y)。资料:不同pH下,含硫微粒在溶液中的主要存在形式:
| pH |
|
|
|
|
| 含硫微粒在溶液中的主要存在形式 |
|
|
|
|
 溶于水后溶液显酸性,用化学用语表示其原因:
溶于水后溶液显酸性,用化学用语表示其原因:(2)用少量NaOH溶液将X溶液pH调至4.3的过程中发生反应的离子方程式是
(3)将X溶液pH调至10时,
 与消耗的NaOH物质的量之比
与消耗的NaOH物质的量之比
(4)关于室温下
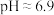 的溶液说法正确的是
的溶液说法正确的是a.
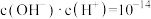
b.

c.
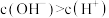
Ⅱ.电化学测定:利用如图电解装置进行测定。

通电片刻后停止通电,加入淀粉溶液。根据电流大小和电解效率理论计算共产生
 。用溶液Y对停止通电后的阳极区电解质溶液进行滴定,到达终点时,共用去
。用溶液Y对停止通电后的阳极区电解质溶液进行滴定,到达终点时,共用去 。
。(5)阳极的电极反应式是
(6)确定滴定终点的现象是
(7)药材中硫残留量(其中含硫微粒均按
 计,
计,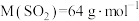 )为
)为
您最近一年使用:0次
名校
解题方法
2 . 室温下,通过下列实验探究 溶液的性质。
溶液的性质。
下列有关说法错误的是
 溶液的性质。
溶液的性质。| 选项 | 实验操作和现象 |
| 1 | 向  溶液中滴加酸性高锰酸钾溶液,溶液紫红色褪去 溶液中滴加酸性高锰酸钾溶液,溶液紫红色褪去 |
| 2 | 用pH试纸测定  溶液的pH,测得pH约为8 溶液的pH,测得pH约为8 |
| 3 | 向  溶液中加入过量 溶液中加入过量  溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 4 | 向  溶液中滴加等体积的 溶液中滴加等体积的 HCl溶液,测得pH约为5.5 HCl溶液,测得pH约为5.5 |
A.实验1说明 具有还原性 具有还原性 |
B.  溶液中存在 溶液中存在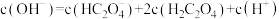 |
C.实验3反应静置后的上层清液中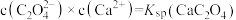 |
D.实验4得到的溶液中 |
您最近一年使用:0次
2022-01-19更新
|
194次组卷
|
4卷引用:湖北省新高考联考协作体2021-2022学年高二上学期期末考试化学试题
湖北省新高考联考协作体2021-2022学年高二上学期期末考试化学试题天津市第四十二中学2022-2023学年高二上学期末考试化学试题(已下线)专项03 四大平衡常数的综合应用-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)天津市第四十二中学2023-2024学年高二上学期第二次月考化学试题
名校
解题方法
3 . 根据水溶液的离子平衡知识,填写下题:
(1)下列物质中,属于强电解质的是_______ (均填序号);属于弱电解质的是_______ 。
①水②氨水③盐酸④冰醋酸⑤硫酸钡⑥氯化银⑦氯化钠⑧氢气⑨醋酸铵
(2)苏打水溶液显碱性原因(用离子方程式表示)_______ 。
(3)醋酸溶液呈_______ (填“酸性”,“中性”或“碱性”),其电离方程式为:_______ ;
(4)常温下,0.lmol·L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3)_______ c(CO )(填“>”、“=”或“<”)。
)(填“>”、“=”或“<”)。
(5)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应完成后溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显_______ 性(填“酸”“碱”或“中”),a_______ 0.01mol·L-1(填“>”、“=”或“<”)。
(6)若分别将pH=2的盐酸和醋酸稀释100倍,则稀释后溶液的pH:盐酸_______ 醋酸(填“>”、“=”或“<”)。
(1)下列物质中,属于强电解质的是
①水②氨水③盐酸④冰醋酸⑤硫酸钡⑥氯化银⑦氯化钠⑧氢气⑨醋酸铵
(2)苏打水溶液显碱性原因(用离子方程式表示)
(3)醋酸溶液呈
(4)常温下,0.lmol·L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3)
 )(填“>”、“=”或“<”)。
)(填“>”、“=”或“<”)。(5)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应完成后溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(6)若分别将pH=2的盐酸和醋酸稀释100倍,则稀释后溶液的pH:盐酸
您最近一年使用:0次
2022-11-16更新
|
167次组卷
|
2卷引用:黑龙江省佳木斯市第十二中学2022-2023学年高二上学期期中考试化学试题
名校
4 . 回答下列问题
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①写出该混合溶液中存在的电荷守恒关系式_______ 。
②向其中加入少量KOH溶液时,发生反应的离子方程式是_______ 。
③现将 溶液和
溶液和 溶液等体积混合,得到缓冲溶液。
溶液等体积混合,得到缓冲溶液。
a.若HA为HCN,该溶液显碱性,则溶液中c(Na+)_______ c(CN-) (填“<”、“=”或“>”)。
b.若HA为 ,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是
,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是_______ 。
(2)常温下,向 溶液中逐滴加入
溶液中逐滴加入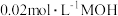 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:

①常温下一定浓度的MCl稀溶液的pH_______ (填“>”“<”或“=”)7,用离子方程式表示其原因_______ 。
②K点对应的溶液中,c(M+)+c(MOH)_______ (填“>”“<”或“=”)2c(Cl-)
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①写出该混合溶液中存在的电荷守恒关系式
②向其中加入少量KOH溶液时,发生反应的离子方程式是
③现将
 溶液和
溶液和 溶液等体积混合,得到缓冲溶液。
溶液等体积混合,得到缓冲溶液。a.若HA为HCN,该溶液显碱性,则溶液中c(Na+)
b.若HA为
 ,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是
,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是(2)常温下,向
 溶液中逐滴加入
溶液中逐滴加入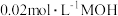 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
①常温下一定浓度的MCl稀溶液的pH
②K点对应的溶液中,c(M+)+c(MOH)
您最近一年使用:0次