名校
1 .  (亚磷酸)主要用作制造塑料稳定剂的原料。
(亚磷酸)主要用作制造塑料稳定剂的原料。
(1)已知 。
。 属于
属于_______ (填“一”“二”或“三”)元酸, 属于
属于_______ (填“正盐”或“酸式盐”)。
(2)25℃,亚磷酸溶液中的 、
、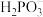 、
、 的物质的量分数
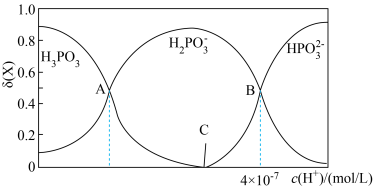
的物质的量分数 随
随 的变化如图所示。已知:
的变化如图所示。已知: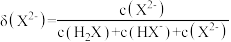 。
。
①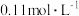 的
的 溶液的pH为2,
溶液的pH为2, 的电离平衡常数
的电离平衡常数 约为
约为_______ ( 的后续电离和水的电离忽略不计)。
的后续电离和水的电离忽略不计)。
②图像中C点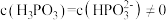 ,那C点对应的
,那C点对应的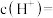
_______  。
。
③A、B、C三点水的电离程度由大到小的顺序为_______ 。
④浓度均为 的
的 和
和 的溶液混合,加水稀释10倍后的溶液中
的溶液混合,加水稀释10倍后的溶液中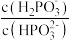 将
将_______ (填“增大”“不变”或“减小”)。
(3)亚磷酸可用电解 溶液来制得,装置如图所示:
溶液来制得,装置如图所示:
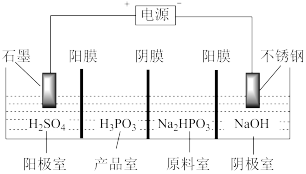
①阴极室的电极反应式为_______ 。
②产品室中发生反应生成产品的总的离子方程式为_______ 。
 (亚磷酸)主要用作制造塑料稳定剂的原料。
(亚磷酸)主要用作制造塑料稳定剂的原料。(1)已知
 。
。 属于
属于 属于
属于(2)25℃,亚磷酸溶液中的
 、
、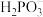 、
、 的物质的量分数
的物质的量分数 随
随 的变化如图所示。已知:
的变化如图所示。已知: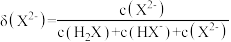 。
。
①
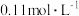 的
的 溶液的pH为2,
溶液的pH为2, 的电离平衡常数
的电离平衡常数 约为
约为 的后续电离和水的电离忽略不计)。
的后续电离和水的电离忽略不计)。②图像中C点
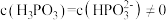 ,那C点对应的
,那C点对应的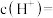
 。
。③A、B、C三点水的电离程度由大到小的顺序为
④浓度均为
 的
的 和
和 的溶液混合,加水稀释10倍后的溶液中
的溶液混合,加水稀释10倍后的溶液中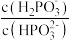 将
将(3)亚磷酸可用电解
 溶液来制得,装置如图所示:
溶液来制得,装置如图所示:
①阴极室的电极反应式为
②产品室中发生反应生成产品的总的离子方程式为
您最近一年使用:0次
名校
2 .  溶液在稀释过程中,溶液中逐渐增大的量是
溶液在稀释过程中,溶液中逐渐增大的量是
① ②
② ③pH ④
③pH ④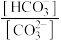
 溶液在稀释过程中,溶液中逐渐增大的量是
溶液在稀释过程中,溶液中逐渐增大的量是①
 ②
② ③pH ④
③pH ④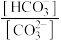
| A.①③ | B.①④ | C.②③ | D.②④ |
您最近一年使用:0次
2023-11-06更新
|
497次组卷
|
6卷引用:上海市上海中学2022-2023学年高二上学期期中考试化学试题
上海市上海中学2022-2023学年高二上学期期中考试化学试题【精品卷】3.3.2 影响盐类水解的主要因素课堂例题-人教版2023-2024学年选择性必修1(已下线)寒假作业06 盐类的水解-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)河北省高碑店市崇德实验中学2023-2024学年高二上学期期中考试化学试题 上海市新中高级中学2023-2024学年高二下学期阶段检测化学试题 陕西省兴平市南郊高级中学2023-2024学年高二上学期第三次化学质量检测题
名校
3 . 兴趣小组为探究FeCl3在溶液中显黄色的原因,进行如下实验。
下列说法不正确 的是
| 序号 | 操作 | 试剂a | 试剂b | 现象 |
| ① | 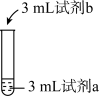 | 0.2mol/L FeCl3 | 蒸馏水 | 溶液为黄色 |
| ② | 0.2mol/L FeCl3 | 2mol/L盐酸 | 溶液为浅黄色 | |
| ③ | 0.2mol/L Fe(NO3)3 | 蒸馏水 | 溶液为浅黄色 | |
| ④ | 0.2mol/L Fe(NO3)3 | 2mol/L硝酸 | 溶液接近无色 |
| A.②中的溶液颜色比①中的浅,主要是因为Fe3+的水解平衡逆向移动 |
| B.由③④可知,Fe(NO3)3溶液显浅黄色与Fe3+水解有关 |
| C.由以上实验可推知,FeCl3溶液显黄色与Fe3+水解、Cl-存在均有关 |
| D.由以上实验可推知,导致②③溶液均为浅黄色的原因相同 |
您最近一年使用:0次
2023-11-02更新
|
376次组卷
|
6卷引用:北京市海淀区2023-2024学年高三上学期期中测试化学试题
名校
4 .  溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法错误的是
。下列说法错误的是
 溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法错误的是
。下列说法错误的是A.通入 ,溶液pH减小 ,溶液pH减小 | B.升高温度,平衡常数增大 |
| C.加水稀释,溶液中所有离子的浓度都减小 | D.加入 固体, 固体,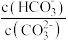 减小 减小 |
您最近一年使用:0次
2023-10-28更新
|
631次组卷
|
4卷引用:吉林省长春市东北师范大学附属中学2023-2024学年高二上学期10月期中化学试题
名校
5 . 在一定条件下,Na2CO3溶液存在水解平衡: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.稀释溶液,各物质浓度均减小,平衡不移动 |
| B.加入少量NaHCO3固体,平衡向正反应方向移动 |
C.升高温度,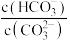 减小 减小 |
| D.加入NaOH固体,溶液pH增大 |
您最近一年使用:0次
2023-10-15更新
|
1100次组卷
|
4卷引用:重庆市育才中学2023-2024学年高二上学期10月月考化学试题
6 . 对盐溶液进行稀释,盐类的水解程度和盐溶液中生成的弱电解质浓度的变化一致吗_______ 。
您最近一年使用:0次
7 . 改变外界条件后,水解平衡若向右移动,水解程度一定会增大吗_______ 。
您最近一年使用:0次
8 .  溶液与
溶液与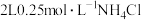 溶液含
溶液含 物质的量不相同。(_______)
物质的量不相同。(_______)
 溶液与
溶液与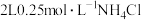 溶液含
溶液含 物质的量不相同。(_______)
物质的量不相同。(_______)
您最近一年使用:0次
名校
解题方法
9 . 下列说法不正确的是
| A.在一定条件下,Na2S溶液加入CuSO4固体,HS-浓度减小 |
| B.加水稀释,水解常数Kh增大,pH减小 |
| C.25℃时,Ka(HCOOH)=1.0×10-4,该温度下HCOO-的水解常数为1.0×10-10 |
| D.某温度下,一元弱酸HA的Ka越小,则NaA的Kh越大 |
您最近一年使用:0次
2023-08-14更新
|
690次组卷
|
4卷引用:微专题(8) 水解常数及应用
解题方法
10 . 影响盐类水解的外界因素
(1)温度:盐的水解是吸热反应,因此升高温度,水解程度___________ 。
(2)浓度:盐溶液的浓度越小,电解质离子相互碰撞结合成电解质分子的几率___________ ,水解程度___________ 。
(3)酸碱性:向盐溶液中加入H+,可抑制___________ 离子水解;向盐溶液中加入OH-,能抑制___________ 离子水解。
(1)温度:盐的水解是吸热反应,因此升高温度,水解程度
(2)浓度:盐溶液的浓度越小,电解质离子相互碰撞结合成电解质分子的几率
(3)酸碱性:向盐溶液中加入H+,可抑制
您最近一年使用:0次



