名校
1 . 石灰乳中存在下列平衡:Ca(OH)2(s)⇌Ca2+(aq)+2OH- (aq),加入下列溶液,可使Ca(OH)2减少的是
| A.NaOH溶液 | B.AlCl3溶液 | C.Na2CO3溶液 | D.CaCl2溶液 |
您最近一年使用:0次
2022-09-26更新
|
62次组卷
|
2卷引用:重庆市巫山县官渡中学2020-2021年高二下学期第一次月考化学试题
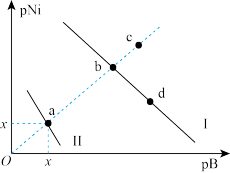
2 . 已知25℃时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7;pNi=-lgc(Ni2+),pB=-lgc(S2-)或-lgc(CO )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液,产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液,产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误 的是
 )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液,产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液,产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法
| A.常温下NiCO3的溶解度大于NiS的溶解度 |
| B.对于曲线I,加热b点溶液,b点向c点移动 |
| C.向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动 |
| D.x对应的值为10.5 |
您最近一年使用:0次
3 . 已知:AgX(X=Cl、Br)溶液中,p(Ag+)=-1gc(Ag+),p(X-)=-lgc(X-)。t℃时,p(X-)与p(Ag+)的相互关系如图。下列说法不正确的是
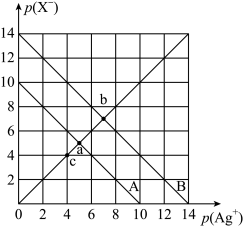

| A.A线表示的是AgBr |
| B.t℃时,c点浓度溶液中会有AgCl固体析出 |
| C.取a、b两点处溶液等体积混合,向溶液中加入足量浓硝酸银溶液,生成的沉淀n(AgBr)>n(AgCl) |
D.t℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数K=104 AgBr(s)+Cl-(aq)的平衡常数K=104 |
您最近一年使用:0次
解题方法
4 . 室温下,向10mL浓度均为0.1mol/L的CuCl2、FeCl2和ZnCl2溶液中分别滴加等浓度的Na2S溶液,滴加过程中pc[pc=-lgc(M2+),M2+为Cu2+或Fe2+或Zn2+]与Na2S溶液体积的关系如图所示。已知:Ksp(CuS)<Ksp(ZnS),Ksp(FeS)=6.25×10-18,lg25=1.4。下列说法正确的是
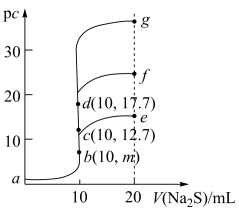

| A.m=8.6 |
| B.a点的CuCl2溶液中:2c(Cu2+)>c(Cl−)+c(OH−) |
| C.a→d→g的过程中,水的电离程度经历由大到小后又增大的过程 |
| D.将足量晶体ZnCl2加入0.1mol/L的Na2S溶液中,c(Zn2+)最大可达到10−24.4mol·L−1 |
您最近一年使用:0次
名校
解题方法
5 . 25℃时,lgS(CaF2)随pH变化如图所示,下列说法错误的是
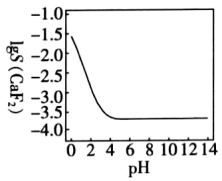
已知:S(CaF2)(单位:mol·L−1)表示CaF2的溶解度。

已知:S(CaF2)(单位:mol·L−1)表示CaF2的溶解度。
| A.CaF2饱和溶液中2c(Ca2+)=c(F-)+c(HF) |
| B.已知Ksp(CaF2)=4×10-11.1,则水中S(CaF2)=10-3.7mol·L-1 |
| C.pH变化时,CaF2溶液中始终存在:c(F-)>c(Ca2+) |
| D.当pH<7时,2c(Ca2+)+c(H+)>c(F-)+c(OH-) |
您最近一年使用:0次
2021-12-25更新
|
764次组卷
|
12卷引用:广东省深圳大学附属中学2022届高三9月调研考试化学试题
广东省深圳大学附属中学2022届高三9月调研考试化学试题福建省南平市2022届高三10月联考化学试卷甘肃省白银市靖远县第四中学2022届高三10月月考化学试题河北省河北衡水中学2021届高三下学期第一次调研考试化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)备战2022年高考化学精准检测卷【全国卷】08山东省2021-2022学年高二12月“山东学情”联考(鲁科版)化学试题河北省邯郸市永年区第二中学2021-2022学年高二12月月考化学试题甘肃省高台县第一中学2021-2022学年高三上学期期中考试化学(理)试题(已下线)一轮巩固卷8-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题安徽省宿州市萧县鹏程中学2021-2022学年高二下学期第一次质量检测化学试题
6 . 要使工业废水中的 沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,
沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,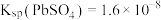 ,
,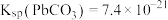 ,
,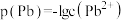 ,
,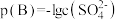 或
或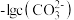 。为研究沉淀效果,在含物质的量浓度相同的
。为研究沉淀效果,在含物质的量浓度相同的 和
和 的混合溶液中滴加
的混合溶液中滴加 溶液产生两种沉淀(温度升高,
溶液产生两种沉淀(温度升高, 、
、 的
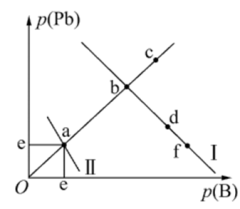
的 均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
 沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,
沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,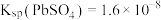 ,
,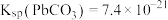 ,
,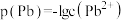 ,
,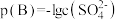 或
或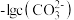 。为研究沉淀效果,在含物质的量浓度相同的
。为研究沉淀效果,在含物质的量浓度相同的 和
和 的混合溶液中滴加
的混合溶液中滴加 溶液产生两种沉淀(温度升高,
溶液产生两种沉淀(温度升高, 、
、 的
的 均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
A.常温下 的溶解度大于 的溶解度大于 的溶解度 的溶解度 |
| B.向d点对应的溶液中加入对应阴离子的钠盐,溶液组成由d点向f点方向移动 |
C.e约为4且对应的阴离子是 |
| D.对于曲线Ⅰ,对b点的溶液加热(忽略水分蒸发),溶液组成由b点向c点移动 |
您最近一年使用:0次
名校
7 . 常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1mol·L-1的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)随滴入的Na2S溶液体积的变化如图所示。下列叙述正确的是
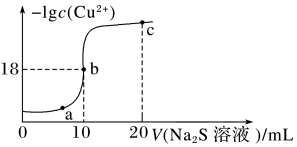

| A.将CuCl2溶液蒸干可得到CuCl2晶体 |
| B.Ksp(CuS)的数量级为10-36 |
| C.a、b、c三点溶液中,b点水的电离程度最大 |
| D.c点溶液中:2c(Cl-)=c(Na+) |
您最近一年使用:0次
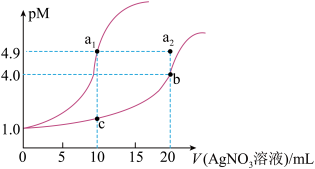
8 . 某温度下,向10mL0.1mol·L-1 NaCl溶液和10 mL 0.1mol·L-1 K2CrO4溶液中分别滴加0.l mol·L-1 AgNO3溶液。滴加过程中pM[-lgc(Cl-)或-lgc(CrO )]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
)]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
 )]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
)]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是
A.该温度下, |
B. 、b、c三点所示溶液中 、b、c三点所示溶液中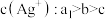 |
| C.若将上述NaCl溶液浓度改为0.2mol·L-1,则a1点会平移至a2点 |
| D.用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂 |
您最近一年使用:0次
2021高三·全国·专题练习
9 . 常温下,金属离子(Mn+)浓度的负对数随溶液pH变化的关系如图所示[已知:pM=-lgc(Mn+),且假设c(Mn+)≤10-6mol·L-1认为该金属离子已沉淀完全]。下列说法正确的是
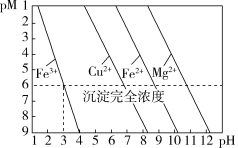

| A.常温下,Ksp[Mg(OH)2]>Ksp[Fe(OH)2] |
| B.可以通过调节溶液pH的方法分步沉淀Cu2+和Fe2+ |
| C.除去Cu2+中少量Fe3+,可控制溶液3≤pH<4 |
| D.pM与Ksp之间的关系式为pM=lgKsp-nlgc(OH-) |
您最近一年使用:0次
2021高三·全国·专题练习
10 . 常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1mol·L-1的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)随滴入的Na2S溶液体积的变化如图所示。下列叙述正确的是
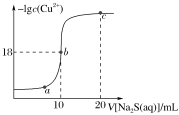

| A.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
| B.Ksp(CuS)的数量级为10-36 |
| C.a、b、c三点溶液中,b点水的电离程度最大 |
| D.c点溶液中:2c(Cl-)=c(Na+) |
您最近一年使用:0次



