1 . 常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑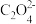 的水解)。下列叙述错误的是
的水解)。下列叙述错误的是

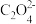 的水解)。下列叙述错误的是
的水解)。下列叙述错误的是
| A.Ksp(Ag2C2O4)的数量级等于10-11 |
| B.a点表示Ag2C2O4的不饱和溶液 |
C.向c(Cl-)=c(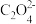 )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 |
D.Ag2C2O4(s)+2Cl-(aq) ⇌2AgCl(s)+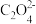 (aq)的平衡常数K=109.04 (aq)的平衡常数K=109.04 |
您最近一年使用:0次
2021-04-24更新
|
619次组卷
|
5卷引用:河南省六市(南阳市、驻马店市、信阳市、漯河市、周口市、三门峡市)2021届高三4月第二次联合调研检测理综化学试题
河南省六市(南阳市、驻马店市、信阳市、漯河市、周口市、三门峡市)2021届高三4月第二次联合调研检测理综化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)难点6 水溶液中的四大平衡常数-2021年高考化学专练【热点·重点·难点】(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练新疆岳普湖县2021-2022学年高二下学期第一次学情调研测试化学试题
解题方法
2 . 常温下,向20mL0.1mol·L-1BaCl2溶液中滴加0.2mol·L-1Na2CO3溶液的滴定曲线如图所示。已知:pBa=-lgc(Ba2+),pKa=-lgKa;常温下H2CO3:pKa1=6.4,pKa2=10.3。下列说法正确的是
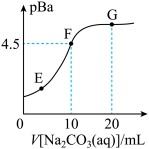

| A.常温下,Na2CO3溶液的pKh1=3.7(Kh1为一级水解常数) |
| B.常温下,Ksp(BaCO3)≈1.0×10-9 |
| C.E、F、G三点的Ksp从大到小的顺序为:G>F>E |
| D.其他条件相同,用MgCl2溶液替代BaCl2溶液,F点向G点迁移 |
您最近一年使用:0次
解题方法
3 . 0.004 mol·L-1AgNO3与0.004 mol·L-1K2CrO4等体积混合,此时有无Ag2CrO4沉淀生成?_______ (Ag2CrO4的Ksp=1.1×10-12 mol3·L-3)。
您最近一年使用:0次
2021-04-23更新
|
592次组卷
|
3卷引用:课前-3.4.2 沉淀溶解平衡的应用-课前、课中、课后(人教版2019选择性必修1)
解题方法
4 . 将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小排列的顺序是
①20 mL 0.01 mol·L-1NH4Cl溶液
②30 mL 0.02 mol·L-1 CaCl2溶液
③40 mL 0.03 mol·L-1盐酸
④10 mL蒸馏水
⑤50 mL 0.05 mol·L-1AgNO3溶液
①20 mL 0.01 mol·L-1NH4Cl溶液
②30 mL 0.02 mol·L-1 CaCl2溶液
③40 mL 0.03 mol·L-1盐酸
④10 mL蒸馏水
⑤50 mL 0.05 mol·L-1AgNO3溶液
| A.①②③④⑤ | B.④①③②⑤ | C.⑤④②①③ | D.④③⑤②① |
您最近一年使用:0次
解题方法
5 . 已知25 ℃时,AgCl的溶度积Ksp=1.8×10-10 mol2·L-2,则下列说法正确的是
| A.向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) |
| C.温度一定,当溶液中c(Ag+)·c(Cl-)=Ksp时,此溶液为AgCl饱和溶液 |
| D.将固体AgCl加入到KI溶液中,固体由白色变为黄色,AgCl完全转化为AgI,AgCl的溶解度小于AgI的溶解度 |
您最近一年使用:0次
2021-04-23更新
|
535次组卷
|
5卷引用:作业10 沉淀溶解平衡-2021年高二化学暑假作业(人教版2019)
(已下线)作业10 沉淀溶解平衡-2021年高二化学暑假作业(人教版2019)(已下线)3.4.1 沉淀溶解平衡原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)广西百色市德保高中2021-2022学年高二上学期段考化学试题福建省莆田第十五中学2018-2019学年高二下学期期中测试化学试题(已下线)第21讲 难溶电解质的沉淀溶解平衡(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
6 . 下列事实与平衡移动原理无关的是
| A.加压能增大氨气在水中的溶解度 |
B.用碳酸钠溶液将水垢中的 转化为疏松的 转化为疏松的 |
C.将 溶液滴入双氧水中,瞬间有大量气泡冒出 溶液滴入双氧水中,瞬间有大量气泡冒出 |
| D.将石灰石投入新制氯水中,氯水的漂白性增强 |
您最近一年使用:0次
名校
解题方法
7 . 锌冶炼过程中产生的锌渣主要成分为铁酸锌(ZnFe2O4)和二氧化硅,以及少量的铜、铁、锌的氧化物和硫化物。利用酸溶的方法可溶出金属离子,使锌渣得到充分利用。
(1)铁酸锌酸溶。铁酸锌难溶于水,其晶胞由A、B结构按照1∶1交替累积而成,如图所示。将铁酸锌粉末投入到1L1mol·L-1H2SO4中,保温80℃,匀速搅拌。浸出液中Fe3+和Zn2+的浓度随时间的变化如表所示。
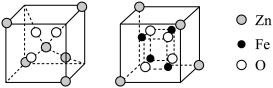
①B结构的化学式为___ 。
②铁酸锌和硫酸反应的离子方程式为___ 。
③酸溶时,溶出效率较高的金属离子是___ 。
(2)锌渣酸溶。将锌渣分别在SO2—1mol·L-1H2SO4、1mol·L-1H2SO4以及SO2—H2O三种体系中实验,均保持80℃,匀速搅拌,所得结果如图所示。已知:25℃时,Ksp(FeS)=6.3×10-17;Ksp(ZnS)=2.9×10-25;Ksp(CuS)=6.3×10-36;Ksp(Cu2S)=2.5×10-48;FeS和ZnS可溶于稀硫酸,CuS和Cu2S不溶于稀硫酸。
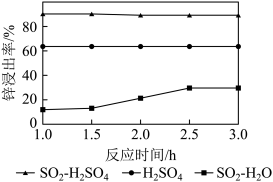
①在SO2—H2SO4体系中,Zn2+浸出率较高的原因是___ 。
②在SO2—H2SO4体系中,溶渣中Cu2S的质量增加,原因是___ 。
(1)铁酸锌酸溶。铁酸锌难溶于水,其晶胞由A、B结构按照1∶1交替累积而成,如图所示。将铁酸锌粉末投入到1L1mol·L-1H2SO4中,保温80℃,匀速搅拌。浸出液中Fe3+和Zn2+的浓度随时间的变化如表所示。

| 时间/h | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 |
| c(Zn2+)/mol•L-1 | 0.10 | 0.11 | 0.15 | 0.21 | 0.21 |
| c(Fe3+)/mol•L-1 | 0.12 | 0.13 | 0.16 | 0.21 | 0.30 |
②铁酸锌和硫酸反应的离子方程式为
③酸溶时,溶出效率较高的金属离子是
(2)锌渣酸溶。将锌渣分别在SO2—1mol·L-1H2SO4、1mol·L-1H2SO4以及SO2—H2O三种体系中实验,均保持80℃,匀速搅拌,所得结果如图所示。已知:25℃时,Ksp(FeS)=6.3×10-17;Ksp(ZnS)=2.9×10-25;Ksp(CuS)=6.3×10-36;Ksp(Cu2S)=2.5×10-48;FeS和ZnS可溶于稀硫酸,CuS和Cu2S不溶于稀硫酸。

①在SO2—H2SO4体系中,Zn2+浸出率较高的原因是
②在SO2—H2SO4体系中,溶渣中Cu2S的质量增加,原因是
您最近一年使用:0次
2021-04-21更新
|
631次组卷
|
4卷引用:江苏省苏锡常镇四市2021届高三教学情况调研(一)化学试题
江苏省苏锡常镇四市2021届高三教学情况调研(一)化学试题(已下线)押江苏卷第15题 化学工业流程综合题 -备战2022年高考化学临考题号押题(江苏卷)江苏省南京市金陵中学2021-2022学年高三下学期3月学情调研化学试题江苏省泰州中学2023-2024学年高三上学期期初调研考试化学试题
名校
8 . t℃时,AgCl(s)与AgI(s)分别在溶液中达到沉淀溶解平衡,其中AgI的溶解度更小,相关离子浓度的关系如图所示。下列说法正确的是
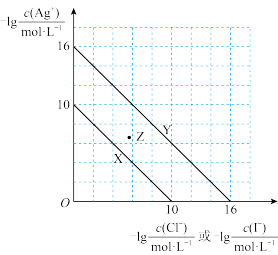

A.曲线Y表示-lg 与-lg 与-lg 的变化关系 的变化关系 |
| B.t℃时,向Z点对应的溶液中加入蒸馏水,可使溶液变为曲线X对应的饱和溶液 |
| C.t℃时,向浓度均为0.1mol/L的KI与KCl混合溶液中加入AgNO3溶液,当Cl-刚好完全沉淀时,此时c(I-)=1×10-11mol/L |
D.t℃时,AgCl(s)+I-(aq) AgI(s)+Cl-(aq)的平衡常数K=1×103 AgI(s)+Cl-(aq)的平衡常数K=1×103 |
您最近一年使用:0次
2021-04-20更新
|
234次组卷
|
2卷引用:江西省景德镇市浮梁一中2020-2021学年高二下学期4月月考化学试题
名校
9 . 纯净的氯化钠是不潮解的,但粗盐很容易潮解,这主要是因为其中含有杂质MgCl2的缘故。为得到纯净的氯化钠,有人设计了一个实验:把买来的粗盐放入纯氯化钠饱和溶液一段时间,过滤,洗涤,可得纯净的氯化钠晶体。则下列说法正确的是
| A.设计实验的根据是NaCl的溶解平衡 |
| B.设计实验的根据是MgCl2比NaCl易溶于水 |
| C.在整个过程中NaCl饱和溶液浓度会变大(温度不变) |
| D.粗盐的晶粒大一些有利于提纯 |
您最近一年使用:0次
名校
10 . 用Ksp表示难溶物的溶度积。下列有关沉淀溶解平衡的说法中,正确的是
| A.在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp增大 |
| B.在CaCO3的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动 |
| C.温度升高,沉淀物的Ksp一定增大 |
| D.25℃时,Ksp(AgCl)> Ksp(AgI),向AgCl的悬浊液中加入KI固体,有黄色沉淀生成 |
您最近一年使用:0次
2021-04-16更新
|
177次组卷
|
3卷引用:河北省衡水市第十四中学2020-2021学年高二下学期一调考试化学试题



