名校
解题方法
1 . 下列离子方程式符合题意的是
A.等物质的量浓度的盐酸与Na2CO3溶液等体积混合:2H++CO =CO2↑+H2O =CO2↑+H2O |
| B.加入Na2S除去废水中的Cu2+:S2-+Cu2+=CuS↓ |
| C.将NaClO碱性溶液与含Fe2+的溶液混合: ClO-+2Fe2++H2O=Cl-+2Fe3++2OH- |
D.用铜电极电解硫酸铜溶液:2Cu2+ + 2H2O 2Cu + O2↑ + 4H+ 2Cu + O2↑ + 4H+ |
您最近一年使用:0次
名校
2 . 某兴趣小组利用工业废弃的铁铜合金制备碳式碳酸铜的简易流程如图。下列叙述错误的是


| A.“沉降”反应中溶液与Na2CO3以不同方式或不同用量比混合不影响产品成分 |
| B.“过滤1”所得的滤液中的溶质主要为硫酸铜 |
| C.“滤渣”的主要成分为氢氧化铁 |
| D.“溶解”时发生了氧化还原反应 |
您最近一年使用:0次
2022-03-26更新
|
866次组卷
|
9卷引用:河北省名校联盟2021-2022学年高三下学期联合调研化学试题
河北省名校联盟2021-2022学年高三下学期联合调研化学试题(已下线)化学-2022年高考押题预测卷02(山东卷)上海交通大学附属中学2021-2022学年高三下学期期中考试化学试题湖北省襄阳市第五中学2022届高三下学期适应性考试(二模)化学试题湖南省长沙市长沙县第一中学2021-2022学年高三下学期期中考试化学试题湖南省长沙市望城区第一中学2022届高三下学期期中考试化学试题(已下线)专题14 物质的反应和转化-三年(2020-2022)高考真题分项汇编(已下线)第八章 水溶液中的离子平衡(测)-2023年高考化学一轮复习讲练测(全国通用)湖南省攸县第三中学2022-2023学年高三第六次月考化学试题
名校
解题方法
3 . 某NiO的废料中有FeO、CuO、Al2O3、MgO、SiO2等杂质,用此废料提取NiSO4和Ni的流程如下:

已知:有关金属离子生成氢氧化物沉淀所需的pH如下表:
(1)滤渣1的主要成分为_______ 。
(2)从滤液2中获得NiSO4∙6H2O的实验操作_______ 、_______ 、过滤、洗涤、干燥。
(3)用离子方程式解释加入H2O2的作用______ 。
(4)加NiO调节溶液的pH至3.2,则生成沉淀的离子方程式_______ 。
(5)电解浓缩后的滤液2可获得金属镍,其基本反应原理如图:

若一段时间后,在A、B两极均收集到11.2L气体(标准状况下),能得到Ni______ g。

已知:有关金属离子生成氢氧化物沉淀所需的pH如下表:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀时pH | 1.5 | 3.6 | 7.3 | 7.0 | 9.6 |
| 完全沉淀时pH | 3.8 | 4.7 | 9.3 | 9.0 | 12.0 |
(1)滤渣1的主要成分为
(2)从滤液2中获得NiSO4∙6H2O的实验操作
(3)用离子方程式解释加入H2O2的作用
(4)加NiO调节溶液的pH至3.2,则生成沉淀的离子方程式
(5)电解浓缩后的滤液2可获得金属镍,其基本反应原理如图:

若一段时间后,在A、B两极均收集到11.2L气体(标准状况下),能得到Ni
您最近一年使用:0次
4 . 下列说法正确的是
| A.溶解度小的沉淀不能转化为溶解度大的沉淀 |
B.用 作沉淀剂,可除去废水中的 作沉淀剂,可除去废水中的 和 和 |
C.向 饱和溶液中加入 饱和溶液中加入 固体, 固体,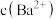 增大 增大 |
D.向AgCl浊液中加入KBr溶液,沉淀颜色变为浅黄色,即可证明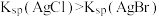 |
您最近一年使用:0次
5 . 下列反应的离子方程式正确的是
A.NaHCO3溶液的水解:HCO +H2O +H2O H3O++CO H3O++CO |
| B.FeI2溶液中滴加少量氯水:2Fe2++Cl2=2Fe3++2Cl− |
C.向NH4HCO3溶液中加过量的NaOH溶液:NH + OH− + OH− NH3↑+H2O NH3↑+H2O |
D.向Mg(OH)2悬浊液中滴加NH4Cl溶液,沉淀溶解:Mg(OH)2+2NH =2NH3·H2O+Mg2+ =2NH3·H2O+Mg2+ |
您最近一年使用:0次
2022-02-22更新
|
347次组卷
|
2卷引用:浙江省浙南名校联考2021-2022学年下学期高三返校联考化学试题
名校
解题方法
6 . 某小组用硫铜矿煅烧废渣(主要含Fe2O3、CuO、FeO)为原料制取Cu2O,流程如图:
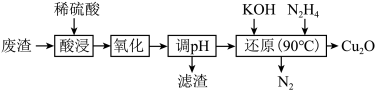
下列说法不正确的是

下列说法不正确的是

| A.“调节pH”主要目的是为了除去Fe3+ |
B.“还原”过程中主要发生的反应为4CuSO4+N2H4+8KOH 2Cu2O+N2↑+4K2SO4+6H2O 2Cu2O+N2↑+4K2SO4+6H2O |
| C.用N2H4还原制取Cu2O的优点是产生N2氛围,可防止产品被氧化 |
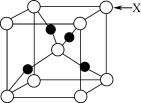
| D.Cu2O的晶胞结构如图所示,其中X代表的是Cu+ |
您最近一年使用:0次
2022-02-15更新
|
817次组卷
|
7卷引用:江苏省南通市通州区2021-2022学年高三上学期期末质量监测化学试题
江苏省南通市通州区2021-2022学年高三上学期期末质量监测化学试题江苏省高邮市2021-2022学年高三下学期期初学情调研化学试题(已下线)黄金卷5-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)江苏省响水中学2021-2022学年高三下学期学情分析(二)化学试题(已下线)押江苏卷第9题 化学工艺流程选择题 -备战2022年高考化学临考题号押题(江苏卷)江苏省南京市宁海中学2021-2022学年高二下学期期末考试化学试题山西省运城市康杰中学2023-2024学年高二下学期开学考试化学试题
7 . 硝酸钾、氯化钠的溶解度曲线如图所示。在60℃时的某溶液中,硝酸钾、氯化钠均刚好达饱和,冷却至0℃时析出晶体的成分是


| A.纯硝酸钾晶体 |
| B.大量硝酸钾,少量氯化钠 |
| C.等量的硝酸钾和氯化钠 |
| D.大量氯化钠,少量硝酸钾 |
您最近一年使用:0次
2022-02-15更新
|
974次组卷
|
3卷引用:课后-1.2.1 有机化合物的分离、提纯-人教2019选择性必修3
名校
8 . 已知: 、
、 ,将含有
,将含有 固体的水垢浸泡在适量的饱和
固体的水垢浸泡在适量的饱和 溶液中,下列说法正确的是
溶液中,下列说法正确的是
 、
、 ,将含有
,将含有 固体的水垢浸泡在适量的饱和
固体的水垢浸泡在适量的饱和 溶液中,下列说法正确的是
溶液中,下列说法正确的是| A.固体逐渐溶解,最后消失 | B.浸泡后的固体加盐酸,有无色无味气体产生 |
| C.浸泡后固体质量不变 | D.浸泡后固体质量增加 |
您最近一年使用:0次
2022-01-23更新
|
170次组卷
|
2卷引用:浙江省台州市2021-2022学年高二上学期期末质量评估化学试题
名校
9 . 常温下,实验测得0.1mol·L-1下列物质的溶液pH如表所示:
(1)Na2CO3溶液显碱性的主要原因为____ (用离子方程式表示)。
(2)上述CH3COONH4溶液中c(NH )
)____ NH4Cl溶液中c(NH )(填“大于”“小于”或“等于”)。
)(填“大于”“小于”或“等于”)。
(3)有同学认为根据前几组实验结果,无需再实验就可以预测a的值,则a=____ 。
(4)推测上述CH3COONa溶液的pH大于NaHCO3溶液pH的可能原因:____ 。
(5)锅炉水垢的主要成分里含有CaSO4,去除水垢时经常先用饱和Na2CO3溶液浸泡,后用盐酸溶解。请应用化学平衡移动原理解释清洗CaSO4的过程:___ 。
物质 | Na2CO3 | CH3COONa | NaHCO3 | CH3COONH4 | NH4Cl |
溶液pH | 11 | 8.9 | 8.3 | 7.0 | a |
(2)上述CH3COONH4溶液中c(NH
 )
) )(填“大于”“小于”或“等于”)。
)(填“大于”“小于”或“等于”)。(3)有同学认为根据前几组实验结果,无需再实验就可以预测a的值,则a=
(4)推测上述CH3COONa溶液的pH大于NaHCO3溶液pH的可能原因:
(5)锅炉水垢的主要成分里含有CaSO4,去除水垢时经常先用饱和Na2CO3溶液浸泡,后用盐酸溶解。请应用化学平衡移动原理解释清洗CaSO4的过程:
您最近一年使用:0次
2022-01-18更新
|
121次组卷
|
2卷引用:山西省大同市2021-2022学年高二上学期期末质量检测化学试题
10 . 根据下列实验操作和现象所得到的实验结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 将废铁屑溶于过量盐酸,滴入KSCN溶液,未见溶液变为红色 | 该废铁屑中不含三价铁的化合物 |
| B | 向Na2SO3溶液中先加入Ba(NO3)2溶液,生成白色沉淀,然后再加入稀盐酸,沉淀不溶解 | Na2SO3溶液已经变质 |
| C | 取少量Mg(OH)2悬浊液,向其中滴加适量CH3COONH4浓溶液,Mg(OH)2溶解 | CH3COONH4溶液呈酸性 |
| D | 在CuSO4溶液中加入KI溶液,再加入苯,振荡,上层呈紫红色,下层有白色沉淀产生 | 铜离子可以氧化碘离子,白色沉淀可能为CuI |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-12-31更新
|
365次组卷
|
3卷引用:河南名校联盟2021-2022学年高二上学期期末考试化学试题



