1 . 根据下列实验操作及现象,能推出相应结论的是
| 实验操作及现象 | 结论 | |
| A | 加热石蜡后生成的气体能使酸性高锰酸钾溶液褪色 | 加热石蜡产生的气体一定是乙烯 |
| B | 向饱和硼酸溶液中加少量NaHCO3粉末,无气泡冒出 | 酸性:碳酸>硼酸 |
| C | 向MgCl2溶液中滴加足量NaOH溶液,有白色沉淀生成,再滴加CuCl2溶液,又有蓝色沉淀生成 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| D | 向淀粉溶液中加稀硫酸共热,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀生成 | 淀粉没有发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-05-28更新
|
232次组卷
|
2卷引用:四川省成都市北大成都附属实验中学2020届高考仿真理科综合化学试题
名校
2 . 下列实验中,与现象对应的结论一定正确的是
| 选项 | 实验 | 现象 | 结论 |
| A. | 常温下,将CH4与Cl2在光照下反应后的混合气体通入石蕊溶液 | 石蕊溶液先变红后褪色 | 反应后含氯的气体共有2种 |
| B. | 向10 mL0.1mol/L NaOH溶液中 先后加入1mL浓度均为0.1mol/L的MgCl2和CuCl2溶液 | 先生成白色沉淀,后生成蓝色沉淀 | Cu(OH)2溶解度小于 Mg(OH)2 |
| C. | 加热NH4HCO3固体,在试管口放一小片湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3溶液显碱性 |
| D. | 将绿豆大小的金属钠分别加入水和乙醇中 | 前者剧烈反应 | 水中羟基氢的活泼性大于乙醇的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-05-25更新
|
877次组卷
|
3卷引用:【市级联考】四川省成都市2019届高三下学期第三次诊断性检测化学试题
名校
3 . 由下列实验操作得出的实验现象和实验结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将石灰石和盐酸反应产生的气体直接通入硅酸钠溶液中 | 生成白色沉淀 | 碳酸的酸性比硅酸强 |
| B | 向FeCl3溶液中通入足量的H2S | 生成两种沉淀 | Fe3+的氧化性强于S |
| C | 向某无色溶液中滴加少量新制氯水 | 加入淀粉后溶液变成蓝色 | 原溶液中含有I— |
| D | 向AgCl固体滴加饱和Na2CrO4溶液 | 有砖红色沉淀生成 | Ksp:Ag2CrO4<AgCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-04-19更新
|
973次组卷
|
3卷引用:四川省泸州市泸县第一中学2020届高三上学期期中考试理综化学试题
名校
4 . 用如图所示装置(夹持已装置省略)进行下列实验,能得出相应实验结论的是
| 选项 | ① | ② | ③ | 实验结论 | 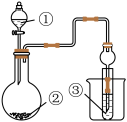 |
| A | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀硫酸 | Na2CO3 | CaCl2溶液 | CO2可与氯化钙反应 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-03-28更新
|
741次组卷
|
2卷引用:【全国百强校】四川省成都市石室中学2019届高三第二次诊断性模拟测试化学试题
5 . 铁及其化合物在日常生活中有广泛的应用,回答下列问题。
(1)用K2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是____________ (用离子方程式表示);但Fe3+净水要腐蚀设备,在腐蚀钢铁设备时,除H+作用外,另一主要原因是________________________________ 。
(2)钢铁腐蚀造成很大损失,用如图装置防止钢铁腐蚀(烧杯中均为食盐水),X极的电极材料应是________________ (填字母)。

A、锌 B、铜 C、银 D、石墨
(3)高铁电池是一种新型的二次电池,电解液为碱性溶液,其反应式如下:
3Zn + 2K2FeO4 + 8H2O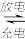 3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
①写出该电池放电时的正极反应式______________________________ 。
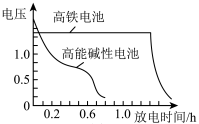
②如图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有______ 。
(4)从保护环境的角度考虑,制备K2FeO4较好的方法为电解法,其装置如图所示。

①石墨做电解池的______ 极(填“阴”或“阳”),溶液中OH-向_____ 移动(填“铁丝网”或“石墨”)
②电解过程中阳极的电极反应式为______________________________ 。
③若维持电流强度为6A,电解5小时,理论上可制得K2FeO4的质量为_________ g(已知F=96500 C/mol,结果保留1位小数)
(5)已知25℃时Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5 mol/L 500 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入____ mL 2 mol/L的盐酸(滴加盐酸前后,溶液总体积不变)。
(1)用K2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是
(2)钢铁腐蚀造成很大损失,用如图装置防止钢铁腐蚀(烧杯中均为食盐水),X极的电极材料应是

A、锌 B、铜 C、银 D、石墨
(3)高铁电池是一种新型的二次电池,电解液为碱性溶液,其反应式如下:
3Zn + 2K2FeO4 + 8H2O
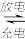 3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH①写出该电池放电时的正极反应式
②如图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

(4)从保护环境的角度考虑,制备K2FeO4较好的方法为电解法,其装置如图所示。

①石墨做电解池的
②电解过程中阳极的电极反应式为
③若维持电流强度为6A,电解5小时,理论上可制得K2FeO4的质量为
(5)已知25℃时Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5 mol/L 500 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入
您最近一年使用:0次
2019-03-25更新
|
308次组卷
|
5卷引用:四川省江油市太白中学2023-2024学年高二上学期12月考试化学试题
四川省江油市太白中学2023-2024学年高二上学期12月考试化学试题【全国百强校】重庆市南开中学2018-2019学年高二上学期期末考试化学试题2019年秋高三化学复习强化练习—— 与浓度积的相关计算(强化练)(已下线)2020年1月5日《每日一题》人教版(选修4)—— 每周一测2020届高三化学大二轮增分强化练—— 金属及其化合物
名校
6 . 下列实验“操作和现象”与“结论”对应且正确的是( )
| 选项 | 操作和现象 | 结论 |
| A | 将少量溴水加入KI溶液中,充分反应后再加入CCl4,振荡,静置,下层液体呈紫色 | 氧化性:Br2>I2 |
| B | 常温下,打磨后的铝片放入浓HNO3中,无明显反应现象 | 常温下,铝不与浓HNO3反应 |
| C | 向一定量AgNO3溶液中,先滴加几滴KCl溶液,再滴加几滴KI溶液,先出现白色沉淀,后出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 用pH计测定NaF溶液和CH3COONa溶液:pH(NaF)<pH(CH3COONa) | 酸性:HF>CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-03-07更新
|
227次组卷
|
3卷引用:四川省威远中学2020届高三上学期第三次月考化学试题
解题方法
7 . 我国是最早发现并使用青铜器的国家,后母戊鼎是我国的一级文物,是世界上出土的最大最重的青铜礼器。现代社会中铜的应用常广泛,铜的回收再利用是化工生产的一个重要领域。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收Cu并制备ZnO的部分实验过程如下:

请回答下列问题:
(1)请写出一种加快铜帽溶解的方法:__________________ 。铜帽溶解时通入空气的作用是___________________________ (用化学方程式表示)。
(2)调节溶液pH时,是将溶液的pH调_________ (填“大”或“小”)到2~3。
(3)电解精炼粗铜时,阴极的电极反应式为___________________________ 。工业上常采用甲醇燃料电池作为电解精炼铜旳电源,写出碱性甲醇燃料电池的负极反应式:___________________________ 。
(4)已知:pH>11时,Zn(OH)2能溶于NaOH溶液生成ZnO22-。室温下,几种离子生成氢氧化物沉淀的pH如下表所小(开始沉淀的pH按金属离子浓度为0.01mol·L-1计算):
①上表中Fe3+沉淀完全的pH为__________________ 。
②由过滤粗铜的滤液制备ZnO的实验步骤依次为(可选用的试剂:30%H2O2、稀硝酸、1.0mol·L-1NaOH溶液):
a.___________________________ ;b.___________________________ ;c.过滤;
d.___________________________ ;e.过滤、洗涤、干燥;f.900℃煅烧。

请回答下列问题:
(1)请写出一种加快铜帽溶解的方法:
(2)调节溶液pH时,是将溶液的pH调
(3)电解精炼粗铜时,阴极的电极反应式为
(4)已知:pH>11时,Zn(OH)2能溶于NaOH溶液生成ZnO22-。室温下,几种离子生成氢氧化物沉淀的pH如下表所小(开始沉淀的pH按金属离子浓度为0.01mol·L-1计算):
| Fe3+ | Fe2+ | Zn2+ | Al3+ | |
| 开始沉淀的pH | 2 | 7.3 | 7.2 | 3.9 |
| 沉淀完全的pH | 8.3 | 8.2 | 5.2 |
②由过滤粗铜的滤液制备ZnO的实验步骤依次为(可选用的试剂:30%H2O2、稀硝酸、1.0mol·L-1NaOH溶液):
a.
d.
您最近一年使用:0次
18-19高二上·山东济宁·阶段练习
名校
8 . 下列说法正确的是
| A.含有AgCl和AgI固体的悬浊液中c(Ag+)>c(Cl-)=c(I-) |
| B.25 ℃时Cu(OH)2在水中的溶解度大于在Cu(NO3)2溶液中的溶解度 |
| C.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| D.25 ℃,AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
您最近一年使用:0次
2019-01-13更新
|
185次组卷
|
8卷引用:四川省遂宁市第二中学2020-2021学年高二下学期期中考试化学试题
9 . 铁、铝是生活中重要的金属材料,铁铝及其化合物有非常重要的用途。
(1)下列说法不正确的是__________ (填序号)。
①配制FeCl3、ACl3溶液时,均是先将固体FeCl3、ACl3溶于较浓的盐酸,再用蒸馏水稀释到所需浓度
②FeCl2、FeCl3、Fe(OH)3均可以通过化合反应生成
③利用氯水和KSCN溶液可以检验FeCl3溶液中有无Fe2+
④加热蒸干Al2(SO4)3溶液残留固体的成分为Al2O3
(2)以高碗铝土矿(主要成分为Al2O3、Fe2O3、SiO2、少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
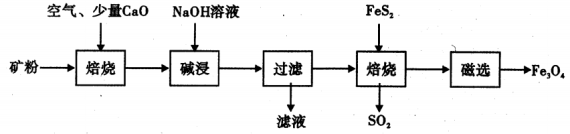
①流程中两次焙烧均会产生SO2,用NaOH溶液吸收处理SO2的离子方程式为___________ 。
②添加1%CaO和不添加CaO的矿粉焙烧其硫去除率随温度变化曲线如图所示。

已知:多数硫酸盐的分解温度都高于600℃
硫去除率=(1-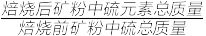 )×100%
)×100%
I.不添加CaO的矿粉在低于500℃焙烧时,去除的硫元素主要来源于__________ 。
Ⅱ.700℃时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是___________________ 。
③“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,写出该反应的化学方程式___________________ 。
(3)已知25℃时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33。
①在25℃下,向浓度均为0.1mo·L-1的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成__________ (填化学式)沉淀。
②溶液中某离子浓度低于1.0×10-5ml·L-1时,可以认为已沉淀完全。现向一定浓度的AlCl3和FeCl3混合溶液中逐滴加入氨水,当Fe3+恰好沉淀完全时,测得c(Al3+)=0.2mol·L-1,所得沉淀中__________ (选填“还含有”或“不含有”)Al(OH)3。理由是___________________ (通过计算说明)。
(1)下列说法不正确的是
①配制FeCl3、ACl3溶液时,均是先将固体FeCl3、ACl3溶于较浓的盐酸,再用蒸馏水稀释到所需浓度
②FeCl2、FeCl3、Fe(OH)3均可以通过化合反应生成
③利用氯水和KSCN溶液可以检验FeCl3溶液中有无Fe2+
④加热蒸干Al2(SO4)3溶液残留固体的成分为Al2O3
(2)以高碗铝土矿(主要成分为Al2O3、Fe2O3、SiO2、少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:

①流程中两次焙烧均会产生SO2,用NaOH溶液吸收处理SO2的离子方程式为
②添加1%CaO和不添加CaO的矿粉焙烧其硫去除率随温度变化曲线如图所示。

已知:多数硫酸盐的分解温度都高于600℃
硫去除率=(1-
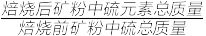 )×100%
)×100%I.不添加CaO的矿粉在低于500℃焙烧时,去除的硫元素主要来源于
Ⅱ.700℃时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是
③“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,写出该反应的化学方程式
(3)已知25℃时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33。
①在25℃下,向浓度均为0.1mo·L-1的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成
②溶液中某离子浓度低于1.0×10-5ml·L-1时,可以认为已沉淀完全。现向一定浓度的AlCl3和FeCl3混合溶液中逐滴加入氨水,当Fe3+恰好沉淀完全时,测得c(Al3+)=0.2mol·L-1,所得沉淀中
您最近一年使用:0次
2019-01-03更新
|
147次组卷
|
2卷引用:【市级联考】四川省内江市2019届高三上学期第一次模拟考试理科综合化学试题
名校
10 . 由下列实验操作及现象能得出相应结论的是
| 操作 | 现象 | 结论 | |
| A. | 将蘸有浓氨水的玻璃棒靠近某溶液 | 有白烟产生 | 该溶液一定为浓盐酸 |
| B. | 向 CH3COONa 溶液中滴入酚酞试液,加热 | 加热后红色加深 | CH3COONa 水解是吸热反应 |
| C. | 向某溶液中加入盐酸,将产生 的气体通入澄清石灰水 | 澄清石灰水变浑浊 | 该溶液中一定有 CO32— |
| D. | 向 NaCl 溶液中滴加过量 AgNO3 溶液,再滴加 KI 溶液 | 先出现白色沉淀, 后出现黄色沉淀 | Ksp(AgI) < Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



