解题方法
1 . 如图所示的各容器中均盛有食盐水,铝在其中都能被腐蚀。其中腐蚀得最慢和最快的分别是


| A.1,2 | B.2,3 | C.3,4 | D.1,4 |
您最近一年使用:0次
2 . 研究电化学腐蚀及防护的装置如下图所示。下列有关说法错误的是
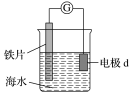

| A.d为锌块,铁片不易被腐蚀 |
| B.d为锌块,铁片上电极反应为2H++2e-==H2↑ |
| C.d为石墨,铁片腐蚀加快 |
| D.d为石墨,石墨上电极反应为O2+2H2O+4e-==4OH- |
您最近一年使用:0次
2018-12-04更新
|
256次组卷
|
3卷引用:【全国百强校】重庆市第一中学校2019届高三上学期期中考试理科综合化学试题
3 . 下列关于电化学原理应用中,正确的是
| A.用惰性电极电解饱和食盐水时,阳极的电极反应式为:2H+-2e-=H2↑ |
| B.氢氧燃料电池的负极反应式:O2 + 2H2O+ 4e-=4OH- |
| C.钢铁发生电化学腐蚀的负极反应式:Fe-2e-=Fe2+ |
| D.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu -2e-=Cu2+ |
您最近一年使用:0次
2016-12-09更新
|
277次组卷
|
2卷引用:2014-2015学年重庆市主城区六校高二上期末联考化学试卷
真题
解题方法
4 . 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)原子序数为29的铜元素位于元素周期表中第_____ 周期。
(2)某青铜器中Sn、Pb的质量分别为119g、20.7g,则该青铜器中Sn和Pb原子的数目之比为____ 。
(3)研究发现,腐蚀严重的青铜器表面大都存在CuCl。关于CuCl在青铜器腐蚀过程中的催化作用,下列叙述正确的是_____ 。
(4)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分CuCl发生复分解反应,该化学方程式为___________ 。
(5)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是______ (填图中字母“a”或“b”或“c”);
②环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈u2(OH)3Cl,其离子方程式为____________ ;
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为____ L(标准状况)。
(1)原子序数为29的铜元素位于元素周期表中第
(2)某青铜器中Sn、Pb的质量分别为119g、20.7g,则该青铜器中Sn和Pb原子的数目之比为
(3)研究发现,腐蚀严重的青铜器表面大都存在CuCl。关于CuCl在青铜器腐蚀过程中的催化作用,下列叙述正确的是
| A.降低了反应的活化能 | B.增大了反应的速率 |
| C.降低了反应的焓变 | D.增大了反应的平衡常数 |
(4)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分CuCl发生复分解反应,该化学方程式为
(5)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是
②环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈u2(OH)3Cl,其离子方程式为
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为
您最近一年使用:0次
2016-12-09更新
|
2068次组卷
|
3卷引用:2015年全国普通高等学校招生统一考试化学(重庆卷)
名校
解题方法
5 . 下列有关物质性质的应用正确的是
| A.氯化钠溶液显中性,可用铝制容器贮存氯化钠溶液 |
| B.碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面油污 |
| C.氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 |
| D.铜的金属性比铁弱,可将海轮浸水部分镶上铜锭以减缓船体腐蚀 |
您最近一年使用:0次
2016-12-09更新
|
473次组卷
|
3卷引用:重庆市云阳江口中学校2021届高三上学期第一次月考化学试题
6 . 合金是建筑航空母舰的主体材料。
(1)航母升降机可由铝合金制造。
①铝元素在周期表中的位置是_______________________ 。工业炼铝的原料由铝土矿提取而得,提取过程中通入的气体为__________ 。
②Al—Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为_________________________ 。焊接过程中使用的保护气为______ (填化学式)。
(2)航母舰体材料为合金钢。
①舰体在海水中发生的电化学腐蚀主要为________________________________ 。
②航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为_________________ 。
(3)航母螺旋桨主要用铜合金制造。
①80.0gCu-Al合金用酸完全溶解后,加入过量氨水,过滤得到白色沉淀39.0,则合金中Cu的质量分数为_________ 。
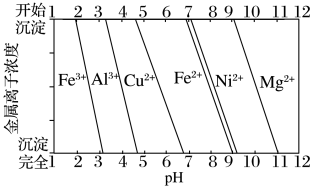
②为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调节pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀。结合如图信息推断该合金中除铜外一定含有_________ 。
(1)航母升降机可由铝合金制造。
①铝元素在周期表中的位置是
②Al—Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为
(2)航母舰体材料为合金钢。
①舰体在海水中发生的电化学腐蚀主要为
②航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为
(3)航母螺旋桨主要用铜合金制造。
①80.0gCu-Al合金用酸完全溶解后,加入过量氨水,过滤得到白色沉淀39.0,则合金中Cu的质量分数为
②为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调节pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀。结合如图信息推断该合金中除铜外一定含有

您最近一年使用:0次
2016-12-09更新
|
1209次组卷
|
5卷引用:2013年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷)
2013年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷)(已下线)2014届高考化学二轮复习必做训练 元素及其化合物练习卷2017届陕西省西安一中高三上期中化学试卷(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (题型专练)(已下线)第5单元 常见的金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷
7 . 下列有关物质性质的应用的说法正确的是
| A.金属活泼性铜比铁弱.可在铁船闸上装铜块减缓其腐蚀 |
| B.MgO的熔点很高,可用于制作耐高温材料 |
| C.铝能置换出氧化铁中的铁,可用于钢铁工业中大量冶炼铁 |
| D.二氧化硫有漂白、杀菌性能,可在食品生产中大量使用 |
您最近一年使用:0次
10-11高一下·广东潮州·期中
名校
解题方法
8 . 下列变化是因原电池反应而引起的是
| A.在空气中金属铝表面迅速氧化形成保护膜 |
| B.常温下,铁被浓硫酸“钝化”形成保护膜 |
| C.在潮湿的空气中钢铁易生锈 |
| D.在潮湿的空气中过氧化钠易变质 |
您最近一年使用:0次
2016-06-16更新
|
236次组卷
|
5卷引用:重庆市第三十中学2018-2019学年高一5月月考化学试题
重庆市第三十中学2018-2019学年高一5月月考化学试题重庆市乌江新高考协作体2023-2024学年高三上学期12月期中联考化学试题(已下线)2010-2011学年广东省潮州金中高一下学期期中考试化学(文)试题2015-2016学年黑龙江省伊春市带岭高中高一下期中化学试卷广东省广州市天河区华南师范大学附属中学2020届高三化学专题训练(7)



