2022高三·全国·专题练习
解题方法
1 . 支撑海港码头基础的钢管桩,常用采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是
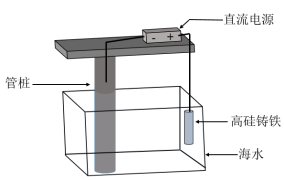

| A.该保护方法叫做外加电流保护法,高硅铸铁的作用是传递电流 |
| B.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零 |
| C.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁 |
| D.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极 |
您最近一年使用:0次
名校
解题方法
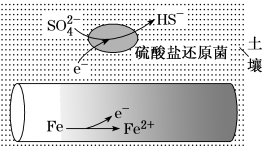
2 . 潮湿土壤中的铁管道在硫酸盐还原菌(最佳生存环境 为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
 为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
| A.铁作负极发生氧化反应 |
B.正极反应为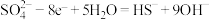 |
| C.将管道连接废锌块可防止腐蚀 |
| D.酸性环境下铁管道不易被硫酸根腐蚀 |
您最近一年使用:0次
2022-07-07更新
|
823次组卷
|
5卷引用:山东省潍坊2021-2022学年高一下学期期末测试化学试题
解题方法
3 . 工业废水中的六价铬[Cr(VI)]常采用还原沉淀法、离子交换法和微生物法等方法进行处理。
(1)室温下,含Cr(VI)的微粒在水溶液中存在如下平衡:
H2CrO4⇌H++HCrO ΔH1
ΔH1
HCrO ⇌H++CrO
⇌H++CrO ΔH2
ΔH2
2HCrO ⇌
⇌ +H2O ΔH3
+H2O ΔH3
室温下,反应2CrO +2H+⇌
+2H+⇌ +H2O的ΔH=
+H2O的ΔH=_______ (用含ΔH1、ΔH2或ΔH3的代数式表示)。
(2)还原沉淀法:使用Na2SO3将Cr(VI)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(VI)具有很强的氧化能力, 将
将 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为_______ 。
②其他条件相同,用Na2SO3处理不同初始pH的含Cr(VI)废水相同时间,当pH<2时,Cr(VI)的去除率随pH降低而降低的原因是_______ 。
(3)微生物法:
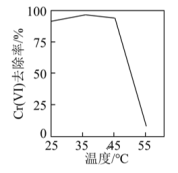
①用硫酸盐还原菌(SRB)处理含Cr(VI)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(VI)的去除率很低的原因是_______ 。
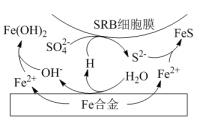
②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,_______ 。
(4)离子交换法:用强碱性离子交换树脂(ROH)与 和HCrO
和HCrO 等发生离子交换,交换过程中发生如下反应:
等发生离子交换,交换过程中发生如下反应:
ROH(s)+HCrO (aq)⇌ RHCrO4(s)+OH-(aq)
(aq)⇌ RHCrO4(s)+OH-(aq)
2ROH(s)+ (aq)⇌ R2CrO4(s)+2OH-(aq)
(aq)⇌ R2CrO4(s)+2OH-(aq)
其他条件相同,当pH>4时,Cr(VI)去除率随pH升高而下降的原因是_______ 。
(1)室温下,含Cr(VI)的微粒在水溶液中存在如下平衡:
H2CrO4⇌H++HCrO
 ΔH1
ΔH1HCrO
 ⇌H++CrO
⇌H++CrO ΔH2
ΔH22HCrO
 ⇌
⇌ +H2O ΔH3
+H2O ΔH3室温下,反应2CrO
 +2H+⇌
+2H+⇌ +H2O的ΔH=
+H2O的ΔH=(2)还原沉淀法:使用Na2SO3将Cr(VI)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(VI)具有很强的氧化能力,
 将
将 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为②其他条件相同,用Na2SO3处理不同初始pH的含Cr(VI)废水相同时间,当pH<2时,Cr(VI)的去除率随pH降低而降低的原因是
(3)微生物法:
①用硫酸盐还原菌(SRB)处理含Cr(VI)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(VI)的去除率很低的原因是

②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,

(4)离子交换法:用强碱性离子交换树脂(ROH)与
 和HCrO
和HCrO 等发生离子交换,交换过程中发生如下反应:
等发生离子交换,交换过程中发生如下反应:ROH(s)+HCrO
 (aq)⇌ RHCrO4(s)+OH-(aq)
(aq)⇌ RHCrO4(s)+OH-(aq)2ROH(s)+
 (aq)⇌ R2CrO4(s)+2OH-(aq)
(aq)⇌ R2CrO4(s)+2OH-(aq)其他条件相同,当pH>4时,Cr(VI)去除率随pH升高而下降的原因是
您最近一年使用:0次
4 . 含可钝化金属的工业管道或反应器,由于会被内部溶液腐蚀,通过外接电源而钝化,称之为阳极保护法。下图是某金属外接电势与电流密度的变化关系,有关说法正确的是
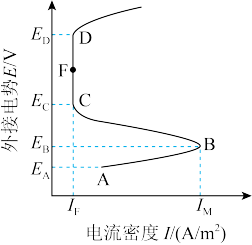

| A.阳极保护法中受保护的金属外接电源的负极 |
| B.电流密度越大,金属受保护程度越好 |
| C.CFD区,金属受到保护 |
| D.外接电势越高,对金属保护性越有效 |
您最近一年使用:0次
2022-06-14更新
|
912次组卷
|
4卷引用:江西省抚州市2022届高三下学期4月教学质量监测理综化学试题
江西省抚州市2022届高三下学期4月教学质量监测理综化学试题(已下线)专题11 金属的腐蚀与防护-备战2023年高考化学母题题源解密(广东卷)(已下线)第19讲 电解池 金属的电化学腐蚀与防护(练)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省大庆实验中学实验三部2023-2024学年高三上学期阶段考试(二)化学试题
5 . 铁及其化合物在生活、生产中有着重要作用。请按要求回答下列问题。
(1)基态Fe原子的简化电子排布式为____ 。
(2)因生产金属铁的工艺和温度等因素不同,产生的铁单质的晶体结构、密度和性质均不同。
①用____ 实验测定铁晶体,测得A、B两种晶胞,其晶胞结构如图:
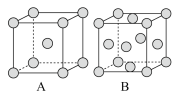
②A、B两种晶胞中含有的铁原子个数比为____ 。
③在A晶胞中,每个铁原子周围与它最近且相等距离的铁原子有____ 个。
(3)常温下,铁不易和水反应,而当撕开暖贴(内有透气的无纺布袋,袋内装有铁粉、活性炭、无机盐、水、吸水性树脂等)的密封外包装时,即可快速均匀发热。利用所学知识解释暖贴发热的原因:___ 。
(4)工业盐酸因含有[FeCl4]—而呈亮黄色,在高浓度Cl—的条件下[FeCl4]—才是稳定存在的。
①[FeCl4]—的中心离子是____ ,配体是____ ;其中的化学键称为____ 。
②取4mL工业盐酸于试管中,逐滴滴加AgNO3饱和溶液,至过量,预计观察到的现象有____ ,由此可知在高浓度Cl—的条件下[FeCl4]—才是稳定存在的。
(1)基态Fe原子的简化电子排布式为
(2)因生产金属铁的工艺和温度等因素不同,产生的铁单质的晶体结构、密度和性质均不同。
①用

②A、B两种晶胞中含有的铁原子个数比为
③在A晶胞中,每个铁原子周围与它最近且相等距离的铁原子有
(3)常温下,铁不易和水反应,而当撕开暖贴(内有透气的无纺布袋,袋内装有铁粉、活性炭、无机盐、水、吸水性树脂等)的密封外包装时,即可快速均匀发热。利用所学知识解释暖贴发热的原因:
(4)工业盐酸因含有[FeCl4]—而呈亮黄色,在高浓度Cl—的条件下[FeCl4]—才是稳定存在的。
①[FeCl4]—的中心离子是
②取4mL工业盐酸于试管中,逐滴滴加AgNO3饱和溶液,至过量,预计观察到的现象有
您最近一年使用:0次
2022-06-01更新
|
766次组卷
|
3卷引用:天津市河西区2022届高考三模化学试题
6 . 实验小组研究金属电化学腐蚀,实验如下:
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
实验Ⅱ
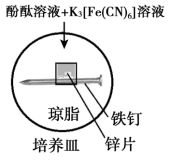
5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
实验Ⅱ

5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
| A.实验Ⅱ中Zn保护了Fe,使铁的腐蚀速率比实验Ⅰ慢 |
B.实验Ⅱ中正极的电极反应式: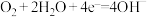 |
C.实验Ⅰ的现象说明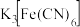 溶液与Fe反应生成了 溶液与Fe反应生成了 |
| D.若将Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色 |
您最近一年使用:0次
2022-09-04更新
|
1375次组卷
|
13卷引用:北京市第十二中学2021-2022学年高一下学期6月月考化学试题
北京市第十二中学2021-2022学年高一下学期6月月考化学试题北京十二中2021-2022学年高一下学期六月月考(等级考)化学试题(已下线)【教材实验热点】17 金属的腐蚀与防护第四章 综合拔高练北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(2卷)试题山东省枣庄市第一中学2022-2023学年高二上学期期末达标化学试题北京市朝阳区2021届高三上学期期末考试化学试题(已下线)2021年高考化学押题预测卷(辽宁卷)(03)(已下线)北京市第四中学2021-2022学年高二上学期期中考试化学试题福建省龙岩市连城县第一中学2023-2024学年高二上学期8月月考化学试题山东省滨州市2023-2024学年高三上学期11月期中考试化学试题
7 . 铁的腐蚀与防护与生产生活密切相关。
Ⅰ.研究铁的腐蚀
实验步骤如下:
步骤1:将铁粉放置于0.002
 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。
步骤2:向15.00 mL 1 NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
步骤3:采集溶液pH随时间变化的数据。
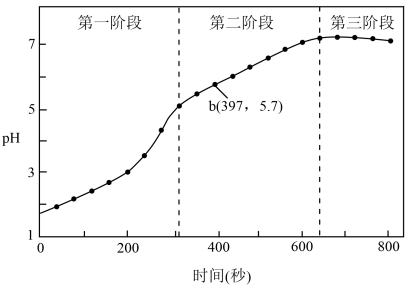
(1)第一阶段,主要发生析氢腐蚀,Cu上发生的电极反应为___________ 。
(2)第二、三阶段主要发生吸氧腐蚀。
①选取b点进行分析,经检验溶液中含有 ,写出Fe被腐蚀的总反应
,写出Fe被腐蚀的总反应___________ 。
②取b点溶液向其中滴加KSCN无明显现象,加入稀盐酸后立即变红。写出b点 被氧化的离子方程式
被氧化的离子方程式___________ 。
③依据b点发生的反应,分析第二阶段pH上升的原因是___________ 。
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知: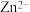 放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
①镀件Fe应与电源的___________ 相连。
②向 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将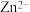 转化为
转化为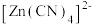 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是___________ 。
(4)电镀后的废水中含有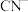 ,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c
,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c 
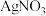 溶液滴定,消耗
溶液滴定,消耗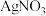 溶液V mL。已知:
溶液V mL。已知: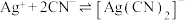 (无色)
(无色) 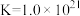 ,
,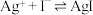
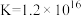 。
。
①滴定终点的现象是___________ 。
②废水中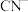 的含量是
的含量是___________  (填计算式)。
(填计算式)。
Ⅰ.研究铁的腐蚀
实验步骤如下:
步骤1:将铁粉放置于0.002

 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。步骤2:向15.00 mL 1
 NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。步骤3:采集溶液pH随时间变化的数据。

(1)第一阶段,主要发生析氢腐蚀,Cu上发生的电极反应为
(2)第二、三阶段主要发生吸氧腐蚀。
①选取b点进行分析,经检验溶液中含有
 ,写出Fe被腐蚀的总反应
,写出Fe被腐蚀的总反应②取b点溶液向其中滴加KSCN无明显现象,加入稀盐酸后立即变红。写出b点
 被氧化的离子方程式
被氧化的离子方程式③依据b点发生的反应,分析第二阶段pH上升的原因是
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知:
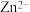 放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。①镀件Fe应与电源的
②向
 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将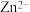 转化为
转化为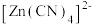 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是(4)电镀后的废水中含有
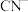 ,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c
,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c 
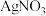 溶液滴定,消耗
溶液滴定,消耗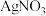 溶液V mL。已知:
溶液V mL。已知: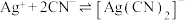 (无色)
(无色) 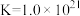 ,
,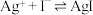
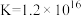 。
。①滴定终点的现象是
②废水中
 的含量是
的含量是 (填计算式)。
(填计算式)。
您最近一年使用:0次
2022-03-25更新
|
730次组卷
|
5卷引用:北京市丰台区2022届高三一模化学试题
8 . 下列说法正确的是
| A.反应物用量增加后,有效碰撞次数增多,反应速率一定增大 |
| B.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| C.△H<0、△S>0的反应在任何温度下都能自发进行 |
| D.铜铁交接处,在潮湿的空气中直接发生反应:Fe-3e-=Fe3+,继而形成铁锈 |
您最近一年使用:0次
2022-02-19更新
|
358次组卷
|
2卷引用:湖北省荆州市八县市2021-2022学年高二上学期期末质量检测化学试题
9 . 某学习小组探究 溶液与
溶液与 溶液在某种条件下的反应。
溶液在某种条件下的反应。
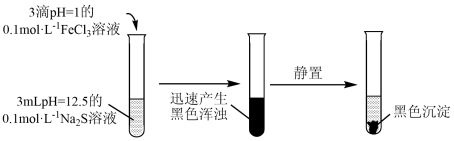
已知:FeS、 均为黑色固体,难溶于水。
均为黑色固体,难溶于水。
(1) 只能大量存在于碱性溶液环境的原因是
只能大量存在于碱性溶液环境的原因是___________ (用化学用语回答)。
(2)小组同学们对试管b中黑色沉淀的提出猜想
猜想1:黑色沉淀是FeS
猜想2:黑色沉淀是
①若猜想1成立,甲同学推测还应该有S生成。甲同学推测所依据的离子方程式___________ 。经检验后确认黑色沉淀中无S单质,猜想1不成立。
②乙同学根据 溶液呈碱性,推测试管b中黑色沉淀除
溶液呈碱性,推测试管b中黑色沉淀除 外,还可能存在
外,还可能存在 ,进行如下实验,以便获得有效信息。
,进行如下实验,以便获得有效信息。
向 浊液中滴加pH=12.5的0.1mol/L
浊液中滴加pH=12.5的0.1mol/L  溶液,观察到红褐色沉淀很快转化为黑色。
溶液,观察到红褐色沉淀很快转化为黑色。
该实验现象能确定的结论是___________ ;不能确定的是___________ 。
(3)丙同学利用电化学原理继续进行探究并设计实验:
丙同学依据实验得出结论:pH=1的0.1mol/L  溶液与pH=12.5的0.1mol/L
溶液与pH=12.5的0.1mol/L  溶液
溶液___________ (填“能”或“不能”)发生氧化还原反应。
(4)综合以上研究,分析试管b中黑色沉淀是 而不是FeS的原因
而不是FeS的原因___________ 。
 溶液与
溶液与 溶液在某种条件下的反应。
溶液在某种条件下的反应。
已知:FeS、
 均为黑色固体,难溶于水。
均为黑色固体,难溶于水。(1)
 只能大量存在于碱性溶液环境的原因是
只能大量存在于碱性溶液环境的原因是(2)小组同学们对试管b中黑色沉淀的提出猜想
猜想1:黑色沉淀是FeS
猜想2:黑色沉淀是

①若猜想1成立,甲同学推测还应该有S生成。甲同学推测所依据的离子方程式
②乙同学根据
 溶液呈碱性,推测试管b中黑色沉淀除
溶液呈碱性,推测试管b中黑色沉淀除 外,还可能存在
外,还可能存在 ,进行如下实验,以便获得有效信息。
,进行如下实验,以便获得有效信息。向
 浊液中滴加pH=12.5的0.1mol/L
浊液中滴加pH=12.5的0.1mol/L  溶液,观察到红褐色沉淀很快转化为黑色。
溶液,观察到红褐色沉淀很快转化为黑色。该实验现象能确定的结论是
(3)丙同学利用电化学原理继续进行探究并设计实验:
| 装置 | 操作及现象 |
 | ①电流计指针有微弱偏转 ②2分钟后,取左侧烧杯溶液,滴加  溶液,有少量蓝色沉淀;2小时后,右侧烧杯有黄色浑浊产生,再取左侧烧杯溶液,滴加 溶液,有少量蓝色沉淀;2小时后,右侧烧杯有黄色浑浊产生,再取左侧烧杯溶液,滴加 溶液,有大量蓝色沉淀。 溶液,有大量蓝色沉淀。 |
 溶液与pH=12.5的0.1mol/L
溶液与pH=12.5的0.1mol/L  溶液
溶液(4)综合以上研究,分析试管b中黑色沉淀是
 而不是FeS的原因
而不是FeS的原因
您最近一年使用:0次
10 . 羰基硫是一种粮食熏蒸剂,能防治某些害虫和真菌的危害,利用CO等制备羰基硫原理:CO+H2S⇌COS+H2。
(1)用FeOOH作催化剂,CO(g)+H2S(g)⇌COS(g)+H2(g)的反应分两步进行,其反应过程能量变化如图1所示。
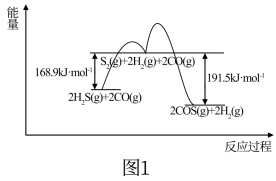
①CO(g)+H2S(g)⇌COS(g)+H2(g) △H=___________ 。
②决定COS生成速率的主要步骤是___________ (填“第1步”或“第2步”)。
(2)在2L的密闭容器中,保持温度不变,开始投入9molH2S和amolCO,经10min达到平衡,Kp=0.2(Kp为以分压表示的平衡常数),n(H2S)=5mol,则CO的平衡转化率α=___________ 。
(3)在2L的密闭容器中,开始时投入amolCO和1molH2S,图2中曲线I和II表示某温度下,CO和H2S投料比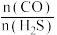 不同时,CO转化率随时间变化关系,则曲线I和II中a值的大小关系为:I
不同时,CO转化率随时间变化关系,则曲线I和II中a值的大小关系为:I___________ II(填“>”“<”或“=”),理由是___________ 。
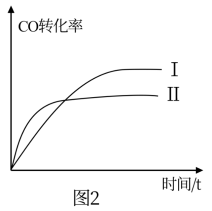
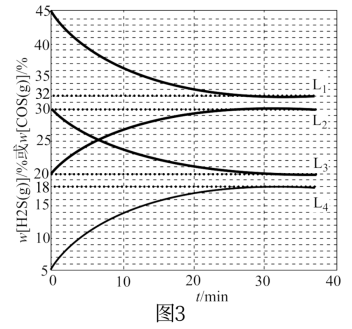
(4)已知起始密闭容器中ω[H2S(g)]和ω[CO(g)]、ω[COS(g)]和ω[H2(g)]分别相等,在240℃时该反应平衡常数K=1,在300℃、340℃时反应中H2S(g)和COS(g)的体积分数(ω)随时间(t)的变化关系如图3所示。则300℃时,ω[COS(g)]随时间变化的曲线为___________ ,340℃时,ω[H2S(g)]随时间变化的曲线为___________ 。
(5)羰基硫在水存在时会缓慢水解生成H2S,会使钢铁设备发生析氢腐蚀,则其正极的电极反应式为___________ ,负极的反应产物为___________ (填化学式)。
(1)用FeOOH作催化剂,CO(g)+H2S(g)⇌COS(g)+H2(g)的反应分两步进行,其反应过程能量变化如图1所示。

①CO(g)+H2S(g)⇌COS(g)+H2(g) △H=
②决定COS生成速率的主要步骤是
(2)在2L的密闭容器中,保持温度不变,开始投入9molH2S和amolCO,经10min达到平衡,Kp=0.2(Kp为以分压表示的平衡常数),n(H2S)=5mol,则CO的平衡转化率α=
(3)在2L的密闭容器中,开始时投入amolCO和1molH2S,图2中曲线I和II表示某温度下,CO和H2S投料比
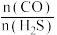 不同时,CO转化率随时间变化关系,则曲线I和II中a值的大小关系为:I
不同时,CO转化率随时间变化关系,则曲线I和II中a值的大小关系为:I
(4)已知起始密闭容器中ω[H2S(g)]和ω[CO(g)]、ω[COS(g)]和ω[H2(g)]分别相等,在240℃时该反应平衡常数K=1,在300℃、340℃时反应中H2S(g)和COS(g)的体积分数(ω)随时间(t)的变化关系如图3所示。则300℃时,ω[COS(g)]随时间变化的曲线为

(5)羰基硫在水存在时会缓慢水解生成H2S,会使钢铁设备发生析氢腐蚀,则其正极的电极反应式为
您最近一年使用:0次



