名校
解题方法
1 . 有机物M是一种制备液晶材料的重要中间体,其合成路线如图所示。
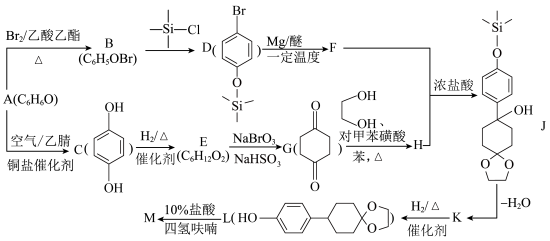
已知:Ⅰ.RX+Mg R-MgX(格林试剂),X=Cl、Br、I;
R-MgX(格林试剂),X=Cl、Br、I;
Ⅱ.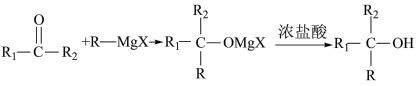 ;
;
Ⅲ.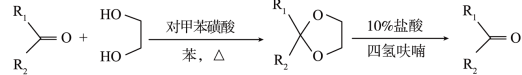 。
。
回答下列问题:
(1)A的俗称是___________ ,B的结构简式为___________ 。
(2)B→D的反应类型是___________ ,反应中使用三甲基氯硅烷(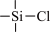 )的作用是
)的作用是___________ ,在本流程中起类似作用的有机物还有___________ (填名称)。
(3)G→H的化学方程式是___________ 。
(4)M的结构简式为___________ ,所含官能团有___________ (填名称)。
(5)符合下列条件的E的同分异构体有___________ 种(不考虑立体异构);其中核磁共振氢谱中显示有6组峰且峰面积之比为6∶2∶1∶1∶1∶1,同时含有1个手性碳原子的有机物结构简式为___________ (写一种)。
①能与金属钠反应产生氢气;②含两个甲基;③能发生银镜反应。

已知:Ⅰ.RX+Mg
 R-MgX(格林试剂),X=Cl、Br、I;
R-MgX(格林试剂),X=Cl、Br、I;Ⅱ.
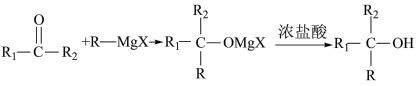 ;
;Ⅲ.
 。
。回答下列问题:
(1)A的俗称是
(2)B→D的反应类型是
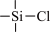 )的作用是
)的作用是(3)G→H的化学方程式是
(4)M的结构简式为
(5)符合下列条件的E的同分异构体有
①能与金属钠反应产生氢气;②含两个甲基;③能发生银镜反应。
您最近一年使用:0次
2024-04-04更新
|
177次组卷
|
2卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题
名校
2 . 某种离子液体的结构如图示,X、Y、Z、M、R为原子序数依次增大的短周期元素,Z的质子数等于X、Y的质子数之和,R为电负性最大的元素。下列说法正确的是
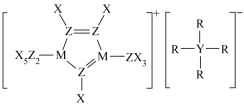
| A.Y的电负性大于Z |
| B.M、X形成的化合物分子间易形成氢键 |
| C.阴离子的空间构型为平面四边形 |
| D.分子的极性:MR3<YR3 |
您最近一年使用:0次
2024-03-24更新
|
338次组卷
|
2卷引用:重庆市第八中学校2022届高三下学期高考适应性月考(七)化学试题
2023高三·全国·专题练习
名校
解题方法
3 . 工业上利用石煤矿粉(主要含 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:

已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为 、
、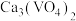 、
、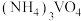 ;
;
②不同pH下,V元素在溶液中的主要存在形式见下表:
③25℃时,
回答下列问题:
(1)“焙烧”时, 发生反应的化学方程式为
发生反应的化学方程式为________ 。
(2)滤渣Ⅰ的成分为_________ (填化学式)。
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到________ 操作单元中循环使用。
(4)“沉钒”中析出 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①_________ 。②________ ;25℃时,测得“转化”后,滤液中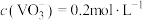 为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少______  。
。
(5)“煅烧”的, 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为
,反应中氧化剂与还原剂物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为_________ 。
 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:
已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为
 、
、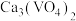 、
、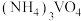 ;
;②不同pH下,V元素在溶液中的主要存在形式见下表:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |

回答下列问题:
(1)“焙烧”时,
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤渣Ⅰ的成分为
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到
(4)“沉钒”中析出
 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①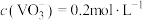 为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少 。
。(5)“煅烧”的,
 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为
,反应中氧化剂与还原剂物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
2024-01-11更新
|
147次组卷
|
5卷引用:四川省绵阳中学2022-2023学年高三上学期高考适应性考试(三)理综试题
四川省绵阳中学2022-2023学年高三上学期高考适应性考试(三)理综试题(已下线)预测卷03-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)先机卷 01 -【热题狂飙】2023年高考化学样卷(全国卷专用)山东省聊城市2022-2023学年高三下学期开学考试化学试题辽宁省葫芦岛市2024届高三一模化学试题
4 . 常温下0.2mol•L-1NaHCO3溶液与0.1mol•L-1Na2CO3溶液等体积混合后,下列关于说法不正确 的是
A.NaHCO3=Na++ | B.c(Na+)>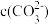 > > >c(OH-) >c(OH-) |
C.c(H+)+c(Na+)=c(OH-)+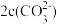 + + | D.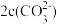 + + + +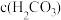 <c(Na+) <c(Na+) |
您最近一年使用:0次
名校
5 . 氨的催化氧化反应是硝酸工业中的重要反应,某条件下 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:
Ⅰ.
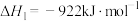
Ⅱ.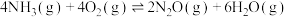
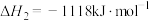
Ⅲ.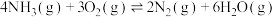

已知:298K时,相关物质的焓的数据如图。
___________  。
。
(2)将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。
②随着温度的升高, 的选择性下降的原因可能为
的选择性下降的原因可能为___________ 。
(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
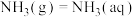

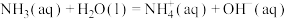

其中p为 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度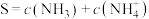 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为___________ 。
(4)由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。
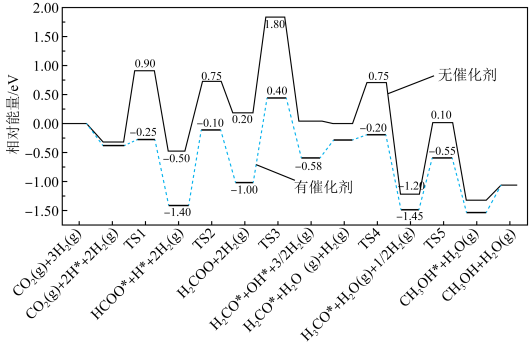
已知: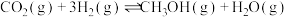 的
的 -49.5kJ/mol
-49.5kJ/mol
反应②:

反应③: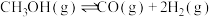
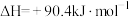
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。___________  。
。
Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入
 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在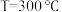 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在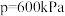 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。
ii. 点
点 的分压为
的分压为___________  ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
___________  (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
iii.图中 点的
点的 高于
高于 点的原因是
点的原因是___________ 。
 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:Ⅰ.

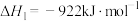
Ⅱ.
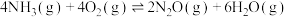
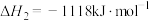
Ⅲ.
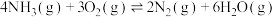

已知:298K时,相关物质的焓的数据如图。


 。
。(2)将一定比例的
 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。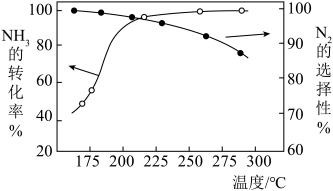
 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。②随着温度的升高,
 的选择性下降的原因可能为
的选择性下降的原因可能为(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
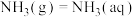

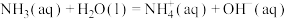

其中p为
 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度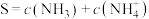 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为(4)由
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。已知:
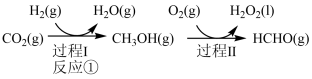
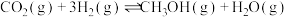 的
的 -49.5kJ/mol
-49.5kJ/mol反应②:


反应③:
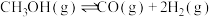
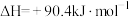
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。
 。
。Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入

 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在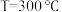 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在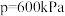 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。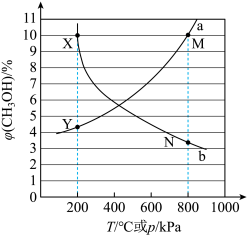
 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。ii.
 点
点 的分压为
的分压为 ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
 (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。iii.图中
 点的
点的 高于
高于 点的原因是
点的原因是
您最近一年使用:0次
名校
6 . 实验室以含锌废液(主要成分为ZnSO4,含少量的Fe2+、Mn2+)为原料制备ZnCO3·2Zn(OH)2的实验流程如下:
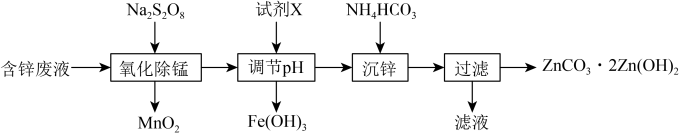
| A.溶液中的Fe2+可以用KSCN溶液检验 |
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO |
| C.调节pH时试剂X可以选用Zn、ZnO、ZnCO3等物质 |
D.沉锌时的离子方程式为3Zn2++6HCO = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O |
您最近一年使用:0次
名校
7 . 关于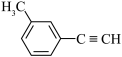 的说法正确的是
的说法正确的是
| A.分子中有6个原子共线 | B.分子中共平面的原子数目最多为14 |
| C.分子中的苯环由单双键交替组成 | D.该有机物的一氯代物有两种 |
您最近一年使用:0次
8 . 现有如图所示的转化关系,已知:A为高级脂肪酸甘油酯。回答下列问题:___________ ,D的结构简式为___________ 。
(2)①的化学方程式为________________ ;③的反应类型为________ 反应。
(3)完全燃烧等物质的量的B和某烷烃消耗等量的氧气,则该烷烃的名称为___________ 。
(4)m g某天然油脂完全水解需要18gNaOH,则m g该油脂的物质的量为___________ mol。
(5)一定量的CH3COOH和O2混合后完全反应生成CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重10.8g,碱石灰增重13.2g。则n(CH3COOH)︰n(O2)=___________ 。

(2)①的化学方程式为
(3)完全燃烧等物质的量的B和某烷烃消耗等量的氧气,则该烷烃的名称为
(4)m g某天然油脂完全水解需要18gNaOH,则m g该油脂的物质的量为
(5)一定量的CH3COOH和O2混合后完全反应生成CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重10.8g,碱石灰增重13.2g。则n(CH3COOH)︰n(O2)=
您最近一年使用:0次
名校
9 . 下列选项中除杂试剂或操作正确的是
选项 | 物质(杂质) | 除杂试剂或操作 |
A | 甲烷(丙烯) | 酸性高锰酸钾溶液 |
B | 乙酸乙酯(乙醇) | 浓硫酸、乙酸、加热 |
C | 二氧化硫(乙烯) | 溴水 |
D | 蛋白质溶液(NaCl) | 渗析 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-20更新
|
950次组卷
|
3卷引用:江西省南昌十九中2021-2022学年高一下学期第三次月考化学试卷
名校
解题方法
10 . 硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图实验装置模拟工业制备 KSCN 并进行相关探究实验。___________ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为___________ 。
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是___________ (写两点)。
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是___________ 。
(5)尾气处理:装置C 中仪器a的名称是___________ ,酸性Fe₂(SO₄)₃溶液用于除去尾气中两种污染性气体,其中一种气体M能使酚酞溶液变红,另一种气体N能使溶液产生淡黄色沉淀,写出除去气体N的离子方程式___________ 。
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知 (白色)]:
(白色)]:___________ [可供选择的试剂:  溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
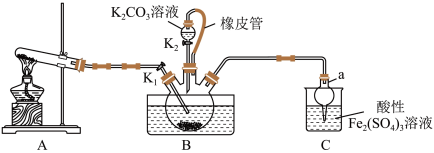

(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至
 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是(5)尾气处理:装置C 中仪器a的名称是
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知
 (白色)]:
(白色)]: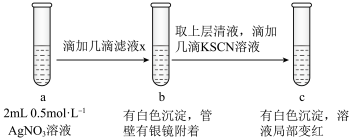
 溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
您最近一年使用:0次
2024-04-16更新
|
285次组卷
|
2卷引用:福建师范大学附属中学2021-2022学年高一下学期期末考试化学试题



