名校
解题方法
1 . 下列实验操作和现象与对应结论或目的不相匹配的是
| 选项 | 实验操作和现象 | 结论或目的 |
| A | 向锌和稀硫酸反应的试管中滴加几滴CuSO4溶液,气泡生成速率加快 | CuSO4是该反应的催化剂 |
| B | 向5 mL0.1 mol/LKI溶液中滴入0.1 mol/LFeCl3溶液5~6滴,加2 mLCCl4振荡,静置后取上层清液滴加KSCN溶液,观察现象 | 验证Fe3+与I的反应有一定限度 |
| C | 将撒有Na2O2的脱脂棉放在石棉网上,然后向其中滴加少量H2O,观察现象 | 验证Na2O2与H2O反应放热 |
| D |  平衡体系中加入少量FeCl3固体,观察溶液颜色变化 平衡体系中加入少量FeCl3固体,观察溶液颜色变化 | 验证勒夏特列原理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-04更新
|
281次组卷
|
3卷引用:河北省九师联盟2021-2022学年高二上学期期中考试化学试题
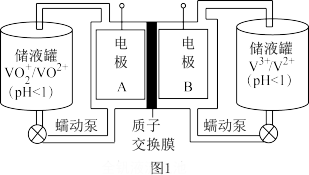
2 . 全钒液流电池是一种新型的绿色环保储能系统,工作原理如图1。该电池放电时总反应为V2++VO +2H+=V3+ +VO2+ +H2O。图2是太阳能电池工作示意图,与图1装置联合可实现能量的转化和储存。下列有关说法错误的是
+2H+=V3+ +VO2+ +H2O。图2是太阳能电池工作示意图,与图1装置联合可实现能量的转化和储存。下列有关说法错误的是

 +2H+=V3+ +VO2+ +H2O。图2是太阳能电池工作示意图,与图1装置联合可实现能量的转化和储存。下列有关说法错误的是
+2H+=V3+ +VO2+ +H2O。图2是太阳能电池工作示意图,与图1装置联合可实现能量的转化和储存。下列有关说法错误的是

| A.储能时,电极A接太阳能电池的N电极,电极B接P电极 |
| B.放电时,电极B的电极反应式为V2+-e-=V3+ |
C.储能时,电极A的电极反应式为VO2+-e- +H2O= +2H+ +2H+ |
| D.放电时,每转移1 mole-就有1 mol H+通过质子交换膜进入电极A区 |
您最近一年使用:0次
2021-11-01更新
|
604次组卷
|
2卷引用:河北省衡水中学2023届高三上学期三调考试化学试题
名校
解题方法
3 . 某课题研究小组设计如图所示装置(电极材料均为铂),该装置可将工业废水中的乙胺(CH3CH2NH2)转化成无毒无害物质。下列分析错误的是
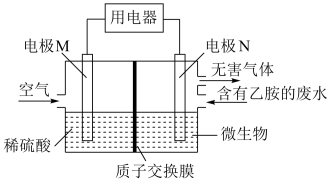

| A.电极N为电池的负极 |
| B.电池工作时,H+由左极区通过质子交换膜移动到右极区 |
| C.电极N的电极反应式为2CH3CH2NH2+8H2O-30e-=4CO2↑+N2↑+30H+ |
| D.当空气(假设含氧气20%)的进入量为7.5mol时,可以处理含乙胺9%(质量分数)的废水0.1kg |
您最近一年使用:0次
名校
解题方法
4 . 根据化学能转化为电能的相关知识,回答下列问题:
I.理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是___ (填化学式),发生__ (填“氧化”或“还原”)反应,电解质溶液是___ (填化学式)溶液。
(2)正极上发生的电极反应为___ 。
(3)若导线上转移的电子为1mol,则消耗的金属铜的质量为___ 。
II.甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入NaOH溶液中,实验装置如图所示。

(4)写出甲中的现象:___ 。
(5)乙中作负极的是___ ,写出负极上的电极反应式:___ 。
(6)如果甲同学与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验得出的结论中,正确的是___ (填标号)。
I.理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上发生的电极反应为
(3)若导线上转移的电子为1mol,则消耗的金属铜的质量为
II.甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入NaOH溶液中,实验装置如图所示。

(4)写出甲中的现象:
(5)乙中作负极的是
(6)如果甲同学与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验得出的结论中,正确的是
| A.镁的金属性不一定比铝的金属性强 |
| B.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| C.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质溶液 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析 |
您最近一年使用:0次
2021-10-29更新
|
747次组卷
|
5卷引用:【石家庄新东方】河北省沧衡八校联盟2020-2021学年高一下学期期中考试化学试题
【石家庄新东方】河北省沧衡八校联盟2020-2021学年高一下学期期中考试化学试题(已下线)周末培优2 电极反应式的书写及新型电源-2021-2022学年高一化学课后培优练(人教版2019必修第二册)重庆市好教育联盟2021-2022学年高一下学期期中考试化学试题吉林省实验中学2021-2022学年高一下学期线上质量检测化学试题安徽省安庆市第七中学2021-2022学年高一下学期期中考试化学试题
5 . 碘、氮及其化合物在生产中应用广泛。
(1)在2HI(g)⇌H2(g)+ I2(g)反应中,三种分子化学键断裂时能量变化如图1所示。其他条件相同,1 mol HI在不同温度分解达平衡时,测得体系中I2的物质的量随温度变化的曲线如图2所示。已知:对于吸热反应,升高温度平衡向右移动。
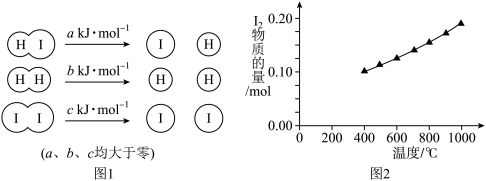
分析图1和图2,比较b+c_______ 2a(填“<”、“>”或“=”),理由是_______ 。
(2)碱性条件下3I2+6OH-=5I-+IO +3H2O,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
+3H2O,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。

①b连接电源的_______ 极。
②简要说明制备KIO3的原理:_______ 。
(3)通过NOx,传感器可监测NOx的含量,其工作原理示意图如下:

①NiO电极上发生的是_______ 反应(填氧化或还原)。
②写出NiO电极的电极反应式:_______ 。
(1)在2HI(g)⇌H2(g)+ I2(g)反应中,三种分子化学键断裂时能量变化如图1所示。其他条件相同,1 mol HI在不同温度分解达平衡时,测得体系中I2的物质的量随温度变化的曲线如图2所示。已知:对于吸热反应,升高温度平衡向右移动。

分析图1和图2,比较b+c
(2)碱性条件下3I2+6OH-=5I-+IO
 +3H2O,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
+3H2O,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
①b连接电源的
②简要说明制备KIO3的原理:
(3)通过NOx,传感器可监测NOx的含量,其工作原理示意图如下:

①NiO电极上发生的是
②写出NiO电极的电极反应式:
您最近一年使用:0次
名校
6 . 下列关于实验现象的描述不正确的是
| A.海水为电解质溶液,铁、铜做电极,铁腐蚀的速率为:铁做阳极>铁做负极 |
| B.在钢铁制品中加入一些铬或镍制成合金,可有效防止金属腐蚀 |
| C.铅蓄电池放电时负极质量减轻,充电时阳极质量增加 |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
您最近一年使用:0次
7 . 为应对全球气候变化,早日实现“碳达峰”“碳中和”目标,研发 利用技术,降低空气中
利用技术,降低空气中 含量成为研究热点。
含量成为研究热点。
I.研究证明, 可作为合成低碳烯烃的原料,目前利用
可作为合成低碳烯烃的原料,目前利用 合成乙烯相关的热化学方程式如下:
合成乙烯相关的热化学方程式如下:
反应ⅰ: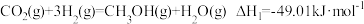
反应ⅱ:
反应ⅲ:
反应ⅳ:
(1)反应ⅰ为反应_____ (填“放热”或“吸热”),能正确表示该反应的图示是______ (填标号)。
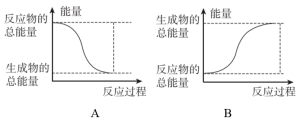
(2)计算可知∆H4=____ ,则利用反应ⅳ生产标准状况下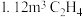 时,放出热量
时,放出热量_______ 。
II.具有广泛应用前景的新型 电化学储能系统吸引了广大科研工作者的研究兴趣。
电化学储能系统吸引了广大科研工作者的研究兴趣。 电池中,
电池中, 为单质锂片,该电池反应产物为碳酸锂和单质碳。
为单质锂片,该电池反应产物为碳酸锂和单质碳。
(3)则该电池中的 在
在___________ (填“正”或“负”)极发生电化学反应。
(4) 电池工作的总反应式为
电池工作的总反应式为___________ 。
III.可利用电还原方法将 转化成燃料。
转化成燃料。
(5) 在碱性介质中电还原为甲醇(
在碱性介质中电还原为甲醇( )的电极反应式为
)的电极反应式为___________ 。
 利用技术,降低空气中
利用技术,降低空气中 含量成为研究热点。
含量成为研究热点。I.研究证明,
 可作为合成低碳烯烃的原料,目前利用
可作为合成低碳烯烃的原料,目前利用 合成乙烯相关的热化学方程式如下:
合成乙烯相关的热化学方程式如下:反应ⅰ:
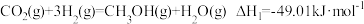
反应ⅱ:

反应ⅲ:

反应ⅳ:

(1)反应ⅰ为反应

(2)计算可知∆H4=
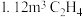 时,放出热量
时,放出热量II.具有广泛应用前景的新型
 电化学储能系统吸引了广大科研工作者的研究兴趣。
电化学储能系统吸引了广大科研工作者的研究兴趣。 电池中,
电池中, 为单质锂片,该电池反应产物为碳酸锂和单质碳。
为单质锂片,该电池反应产物为碳酸锂和单质碳。(3)则该电池中的
 在
在(4)
 电池工作的总反应式为
电池工作的总反应式为III.可利用电还原方法将
 转化成燃料。
转化成燃料。(5)
 在碱性介质中电还原为甲醇(
在碱性介质中电还原为甲醇( )的电极反应式为
)的电极反应式为
您最近一年使用:0次
8 . 关于金属的腐蚀与防护,下列说法错误的是
| A.铁板上使用铜铆钉,会加速铁板的腐蚀 |
| B.白铁皮(镀锌铁)表面镀层被划伤后仍能对铁起到保护作用 |
| C.将铁加工成不锈钢,能减缓钢铁的锈蚀 |
D.钢铁发生析氢腐蚀时,负极的电极反应式为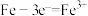 |
您最近一年使用:0次
2021-10-18更新
|
195次组卷
|
2卷引用:河北省省级联测2021-2022学年高二上学期第一次联考化学试卷
解题方法
9 . 某铜锌原电池的结构如图所示,下列说法正确的是
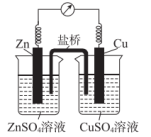

A. 电极为该原电池的正极 电极为该原电池的正极 |
B.电池工作时,电子由 电极流出,经溶液和盐桥流入 电极流出,经溶液和盐桥流入 电极 电极 |
C.若盐桥中的电解质为 ,则电池工作时 ,则电池工作时 向右侧移动 向右侧移动 |
D. 电极上的电极反应式为 电极上的电极反应式为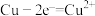 |
您最近一年使用:0次
2021-10-18更新
|
255次组卷
|
3卷引用:河北省省级联测2021-2022学年高二上学期第一次联考化学试卷
河北省省级联测2021-2022学年高二上学期第一次联考化学试卷(已下线)第四章 电化学基础 单元综合检测-2021-2022学年高二化学课后培优练(人教版选修4)浙江省嘉兴市海盐第二高级中学2021-2022学年高二下学期3月阶段检测化学试题
解题方法
10 . 实验探究是提高学习效果的有力手段。某同学用如图所示装置研究原电池原理,下列说法错误的是


| A.若将图1装置的Zn,Cu下端接触,Zn片逐渐溶解,Cu片上能看到气泡产生 |
B.图2中 向Zn片移动 向Zn片移动 |
| C.若将图2中的Zn片改为Mg片,Cu片上产生气泡的速率加快 |
D.图2与图3中,Zn片减轻的质量相等时,正极产物的质量比为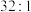 |
您最近一年使用:0次



