名校
解题方法
1 . 当电解质中某离子的浓度越大时,其氧化性或还原性越强。利用这一性质,有人设计出如图所示“浓差电池”(其电动势取决于物质的浓度差,是由一种物质从高浓度向低浓度转移而产生的)。实验开始先断开K1,闭合K2,发现电流计指针发生偏转。下列说法错误的是
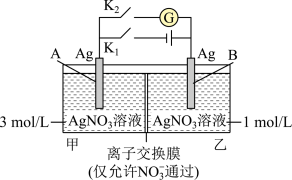

| A.断开K1、闭合K2,一段时间后电流计指针归零,此时两池Ag+浓度相等 |
| B.断开K1、闭合K2,当转移0.1mol e-时,乙池溶液质量增加17.0 g |
| C.当电流计指针归零后,断开K2、闭合K1,一段时间后B电极的质量增加 |
| D.当电流计指针归零后,断开K2、闭合K1,乙池溶液浓度增大 |
您最近一年使用:0次
2020-06-20更新
|
415次组卷
|
2卷引用:河北省石家庄市2020届高中毕业班综合训练(二)理综化学试题
名校
2 . 用下列装置进行相应实验,能达到实验目的的是
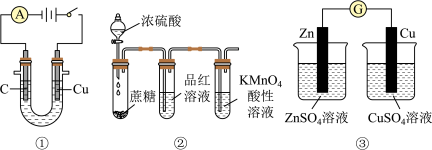



| A.图①所示装置可电解食盐水制氯气和氢气 |
B.图②所示装置可说明浓 具有脱水性、强氧化性, 具有脱水性、强氧化性, 具有氧化性、还原性 具有氧化性、还原性 |
| C.图③装置可以用来验证化学能转化为电能 |
D.用图4所示装置比较 、 、 、 、 的氧化性强弱 的氧化性强弱 |
您最近一年使用:0次
名校
3 . 几种离子在水溶液中有如下转化关系。下列说法正确的是


A.该条件下的氧化性: |
B.反应(1)中,每生成 ,转移3mol电子 ,转移3mol电子 |
C.将反应(2)设计成原电池, 向负极迁移 向负极迁移 |
D. 与 与 反应生成 反应生成 和 和 时,氧化剂与还原剂的物质的量之比为1∶2 时,氧化剂与还原剂的物质的量之比为1∶2 |
您最近一年使用:0次
2022-03-06更新
|
1069次组卷
|
8卷引用:河北省秦皇岛市青龙满族自治县 2021-2022学年高三下学期月考化学试题
河北省秦皇岛市青龙满族自治县 2021-2022学年高三下学期月考化学试题(已下线)秘籍12 原电池原理及应用-备战2022年高考化学抢分秘籍(全国通用)广东省广州市第十六中学2021-2022学年高一下学期期中检测 化学试题(已下线)专题04 氧化还原反应-三年(2020-2022)高考真题分项汇编(已下线)专题04 氧化还原反应-2022年高考真题模拟题分项汇编(已下线)微专题08 氧化性和还原性强弱的实验探究及应用-备战2023年高考化学一轮复习考点微专题广东省江门市新会第一中学2022-2023学年高一下学期3月月考化学试题(已下线)【2023】【高一下】【其他】【余高2】【高中化学】【刘尼尼收集】
解题方法
4 . I.原电池可将化学能转化为电能。由A、B、C、D四种金属按下表中装置进行实验:
(1)装置甲中 向
向___________ 极移动(填“A”或“B”);
(2)四种金属活动性由强到弱的顺序是___________ ;
(3)若装置丙中的电极为质量相等的铁棒和铜棒,电池工作一段时间后,取出洗净、干燥、称量,两电极质量差为6g.则导线中通过电子的物质的量为___________ mol。
II.化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下图为甲烷燃料电池的构造示意图,由此判断

Y极为电池的___________ 极,X极的电极反应方程式为___________ ,电路中每转移0.2mol电子,标准状况下正极上消耗气体的体积是___________ L。
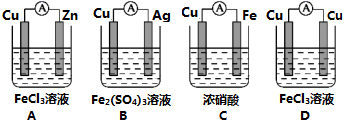
(2)为了验证Fe3+与Cu2+氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是___________ 。
(3)铅蓄电池是常见的化学电源之一,其充电、放电的总反应是:2PbSO4+2H2O Pb +PbO2+2H2SO4.铅蓄电池放电时正极是
Pb +PbO2+2H2SO4.铅蓄电池放电时正极是___________ (填物质化学式),该电极质量___________ (填“增加”或“减少)。若电解液体积为2L(反应过程溶液体积变化忽略不计),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol/L下降到___________ mol/L。
| 装置 | 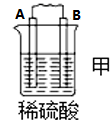 | 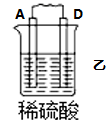 | 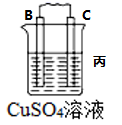 |
| 现象 | B上有气体产生 | D不断溶解 | C质量增加 |
(1)装置甲中
 向
向(2)四种金属活动性由强到弱的顺序是
(3)若装置丙中的电极为质量相等的铁棒和铜棒,电池工作一段时间后,取出洗净、干燥、称量,两电极质量差为6g.则导线中通过电子的物质的量为
II.化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下图为甲烷燃料电池的构造示意图,由此判断

Y极为电池的
(2)为了验证Fe3+与Cu2+氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是

(3)铅蓄电池是常见的化学电源之一,其充电、放电的总反应是:2PbSO4+2H2O
 Pb +PbO2+2H2SO4.铅蓄电池放电时正极是
Pb +PbO2+2H2SO4.铅蓄电池放电时正极是
您最近一年使用:0次
11-12高二下·内蒙古包头·期中
名校
5 . 有关X、Y、Z、W四种金属进行如下实验:
根据以上事实,下列判断或推测错误的是
| ① | 将X和Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
| ② | 将片状的X、W分别投入等浓度盐酸中都有气体产生,W比X反应剧烈 |
| ③ | 用惰性电极电解等物质的量浓度的Y和Z的硝酸盐混合溶液,在阴极上首先析出单质Z |
| A.Z的阳离子氧化性最强 |
| B.W的还原性强于Y的还原性 |
| C.Z放入CuSO4溶液中一定有Cu析出 |
| D.用X、Z和稀硫酸可构成原电池,且X做负极 |
您最近一年使用:0次
2013-01-15更新
|
482次组卷
|
7卷引用:河北省保定市唐县第一中学2020-2021学年高二9月月考化学试题
河北省保定市唐县第一中学2020-2021学年高二9月月考化学试题(已下线)2011-2012学年内蒙古包头三十三中高二下学期期中考试化学试卷(已下线)2012-2013学年内蒙古巴市中学高二12月月考化学试卷(已下线)2014届浙江省杭州十四中高二上学期期末化学试卷 2015-2016学年浙江省海宁市三校高二下学期期中化学试卷模拟卷05(必考+选考)——2020年秋高三化学开学摸底考试卷(全国通用)甘肃省张掖市第二中学2021届高三上学期10月月考化学试题
解题方法
6 . 根据化学能转化为电能的相关知识,回答下列问题:
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是____ ,发生____ (填“氧化”或”还原”)反应,电解质溶液是____ 。
(2)正极上出现的现象是____ 。
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:
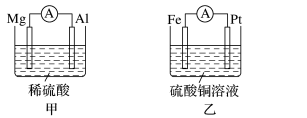
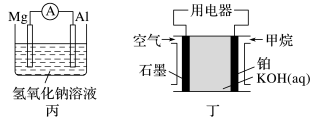
(3)丙装置中负极反应式为____ ,丁装置中负极反应式为____ 。
(4)电池的放电过程中,甲装置中溶液质量____ (填“增加”或“减少”);丁装置中溶液碱性____ (填“增强”或减弱”)。
(5)当甲装置导线中转移0.3mol电子时,正极生成气体____ L(标准状况下);假设开始时乙装置中两电极质量相等,导线中转移0.3mol电子时,两电极质量相差____ g。
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:


(3)丙装置中负极反应式为
(4)电池的放电过程中,甲装置中溶液质量
(5)当甲装置导线中转移0.3mol电子时,正极生成气体
您最近一年使用:0次
名校
解题方法
7 . 某小组研究 分别与
分别与 和
和 的反应:
的反应:
下列说法不正确的是
 分别与
分别与 和
和 的反应:
的反应:| 编号 | 1 | 2 | 3 |
| 实验 | 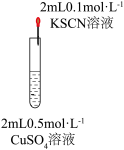 |  | 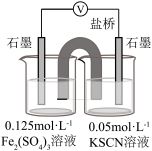 |
| 现象 | 溶液变为黄绿色,产生白色沉淀(白色沉淀为CuSCN) | 溶液变红,向反应后的溶液中滴加 溶液,产生蓝色沉淀,且沉淀量逐渐增多 溶液,产生蓝色沉淀,且沉淀量逐渐增多 | 接通电路后,电压表指针不偏转。一段时间后,取出左侧烧杯中少量溶液,滴加 溶液,没有观察到蓝色沉淀 溶液,没有观察到蓝色沉淀 |
A.实验1中产生白色沉淀说明 被还原 被还原 |
| B.实验2中的现象说明KSCN在溶液中发生了不止一个反应 |
| C.综合实验1~3,说明微粒的氧化性与浓度有关 |
D.若将实验3中 溶液替换为0.25 mol/L 溶液替换为0.25 mol/L  溶液,接通电路后,可推测出电压表指针会发生偏转 溶液,接通电路后,可推测出电压表指针会发生偏转 |
您最近一年使用:0次
2023-09-27更新
|
333次组卷
|
2卷引用:河北省新时代NT教育2024届高三上学期9月阶段测试化学试题
名校
解题方法
8 . 根据下列事实:①A+B2+=A2++B;②E+2H2O=E(OH)2↓+H2↑;③以B、D为电极与D的盐溶液组成原电池,电极反应为:D2++2e﹣=D,B﹣2e﹣═B2+.由此可知A2+、B2+、D2+、E2+的氧化性强弱关系是( )
| A.D2+>B2+>A2+>E2+ | B.B2+>A2+>D2+>E2+ |
| C.D2+>E2+>A2+>B2+ | D.E2+>B2+>A2+>D2+ |
您最近一年使用:0次
2020-03-16更新
|
125次组卷
|
2卷引用:河北省承德市第一中学2019-2020学年高一下学期3月疫情期间直播课堂检测化学试题
9-10高一下·黑龙江鹤岗·期末
名校
解题方法
9 . X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有H2放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为( )
| A.X>Z>Y>M | B.X>Y>Z>M |
| C.M>Z>X>Y | D.X>Z>M>Y |
您最近一年使用:0次
2020-03-19更新
|
262次组卷
|
26卷引用:2010—2011学年河北省保北十二县市高一下学期期中联考化学试卷
(已下线)2010—2011学年河北省保北十二县市高一下学期期中联考化学试卷河北省衡水市武强中学2021-2022学年高二下学期期中考试化学试题(已下线)09~10年鹤岗一中高一下学期期末考试化学卷(已下线)2010年福建省厦门六中高二上学期期中考试化学试卷(已下线)2011-2012学年福建省罗源县第一中学高二上学期期中考试化学(理)试卷(已下线)2012-2013学年山东东营一中高二上学期第一次模块考试化学试卷(已下线)2012-2013学年内蒙古巴市中学高二12月月考化学试卷(已下线)2012-2013学年四川省雅安中学高二下学期期中考试化学试卷(已下线)2012-2013学年浙江省杭州市西湖高级中学高二5月月考化学试卷(已下线)2013-2014学年江苏省响水中学高二上学期期中考试化学试卷(选修)(已下线)2013-2014吉林省吉林一中高二下学期期末考试化学试卷(已下线)2014-2015学年浙江省杭州市西湖高级中学高二10月月考化学试卷2015届上海理工大学附中高三上学期月考化学试卷2014-2015陕西省西安市一中高二上学期期末化学试卷2014-2015学年四川省雅安中学高二下期末模拟化学试卷2014-2015学年重庆市主城区六校高二上期末联考化学试卷2016届辽宁省五校协作体高三上学期期初考试化学试卷2015-2016学年湖北省黄石市有色一中高二上学期10月月考化学试卷2015-2016学年福建省龙海市程溪中学高二上学期期中测试化学试卷2015-2016学年辽宁庄河高中高二下期末化学试卷2017届北京市中央民族大学附中高三上9.12周练化学卷福建省三明市第一中学2017-2018学年高二上学期第一次月考化学试题甘肃省武威市第六中学2018-2019学年高一下学期第二次学段考试化学试题山西省太原市太原师范学院附属中学2019-2020学年高二上学期12月月考理科化学试题课时3 电能转化为化学能——A学习区 夯实基础(苏教版必修2)云南省云天化中学2019-2020学年高二下学期开学考试化学试题
13-14高一下·四川成都·期末
名校
解题方法
10 . 根据下列实验现象,所得结论正确的是
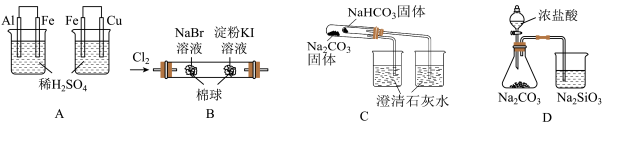

| 实验 | 实验现象 | 结论 |
| A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 氧化性:Al3+>Fe2+>Cu2+ |
| B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 右烧杯中澄清石灰水变浑浊,左边烧杯中无明显变化 | 热稳定性:Na2CO3>NaHCO3 |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-01-09更新
|
839次组卷
|
20卷引用:河北省正定中学2017届高三上学期第三次月考化学试题
河北省正定中学2017届高三上学期第三次月考化学试题【全国百强校】河北省武邑中学2019届高三下学期第一次质检化学试题河北省张家口市宣化区第一中学2020届高三下学期3月月考化学试题河北省石家庄一中东校区2020-2021学年高一第二学期教学质量检测(二)化学试题(已下线)2013-2014学年四川成都外国语学校高一下期末化学试卷安徽省肥东县高级中学2019届高三上学期12月调研化学试题安徽省定远重点中学2019届高三上学期第三次月考化学试题【校级联考】安徽省定远重点中学2019届高三下学期第一次模拟考试化学试题云南省峨山彝族自治县第一中学2018-2019学年高一6月月考化学试题江西省吉安市2018-2019学年高一下学期期末教学质量检测化学试题安徽省滁州市定远县民族中学2020届高三上学期期中考试化学试题安徽省肥东县高级中学2020届高三1月调研考试化学试题吉林省洮南市第一中学2021届高三上学期期中考试化学试题吉林油田高级中学2019-2020学年高二下学期期末考试化学试题陕西省西安高级中学2021-2022学年高三第一次适应性考试化学试题陕西省西安高级中学2021-2022学年高三第一次适应性考试化学试题内蒙古自治区霍林郭勒市第一中学2022-203学年高三上学期9月月考化学试题宁夏固原市第一中学2023届高三上学期第二次月考化学试题宁夏青铜峡市宁朔中学2022-2023学年高三上学期期中考试化学试题陕西师范大学附属中学2024届高三上学期第一次月考化学试题



