解题方法
1 . 完成下列问题。
(1)室温下,甲同学取相同体积的 和
和 溶液混合,探究浓度对反应速率的影响,实验记录如下:
溶液混合,探究浓度对反应速率的影响,实验记录如下:
①该反应的化学方程式为_______ 。
②通过分析比较上表数据,得到的结论是_______ 。
(2)乙同学用 替代
替代 进行上述实验,未观察到溶液变为棕黄色,推测原因是酸性对
进行上述实验,未观察到溶液变为棕黄色,推测原因是酸性对 氧化性有影响,乙同学提出猜测并进行如下探究。
氧化性有影响,乙同学提出猜测并进行如下探究。
提出猜想:其他条件相同时,酸性越强,氧化剂的氧化性越强。
查阅资料:原电池中负极反应一定时,正极氧化剂的氧化性越强,则两极之间电压越高。
设计实验、验证猜想:利用如图装置进行下表实验1~4,记录数据。

①实验1和2中正极的电极反应式为_______ 。
②由实验1和2可知,酸性越强, 的氧化性越强,作出该判断的依据是
的氧化性越强,作出该判断的依据是_______ 。
③测得 ,说明酸性对
,说明酸性对 的氧化性几乎无影响,解释原因:
的氧化性几乎无影响,解释原因:_______ 。
实验结论:若氧化剂被还原时有 参加反应,酸性越强,氧化剂的氧化性越强;若氧化剂被还原时没有
参加反应,酸性越强,氧化剂的氧化性越强;若氧化剂被还原时没有 参加反应,酸性对氧化剂的氧化性几乎没有影响。
参加反应,酸性对氧化剂的氧化性几乎没有影响。
迁移拓展:综合上述探究结果,丙同学进一步提出猜想,其他条件相同时,氧化剂浓度越大,其氧化性越强。
(3)结合乙同学的实验2,丙同学补充进行实验5,验证猜想成立,完成下表中的内容:
猜想成立的依据是:_______ 。
(1)室温下,甲同学取相同体积的
 和
和 溶液混合,探究浓度对反应速率的影响,实验记录如下:
溶液混合,探究浓度对反应速率的影响,实验记录如下:| 实验编号 | 1 | 2 | 3 | 4 | 5 |
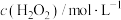 |  |  |  |  |  |
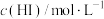 |  |  |  |  |  |
从混合到出现棕黄色时间 | 13 | 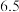 | 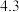 |  |  |
②通过分析比较上表数据,得到的结论是
(2)乙同学用
 替代
替代 进行上述实验,未观察到溶液变为棕黄色,推测原因是酸性对
进行上述实验,未观察到溶液变为棕黄色,推测原因是酸性对 氧化性有影响,乙同学提出猜测并进行如下探究。
氧化性有影响,乙同学提出猜测并进行如下探究。提出猜想:其他条件相同时,酸性越强,氧化剂的氧化性越强。
查阅资料:原电池中负极反应一定时,正极氧化剂的氧化性越强,则两极之间电压越高。
设计实验、验证猜想:利用如图装置进行下表实验1~4,记录数据。
| 序号 | 溶液 | 电压表读数 |
| 1 | 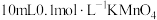 溶液、3滴稀 溶液、3滴稀 | 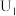 |
| 2 | 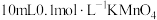 溶液、3滴浓 溶液、3滴浓 |  |
| 3 | 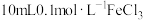 溶液、3滴稀 溶液、3滴稀 | 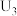 |
| 4 | 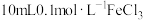 溶液、3滴浓 溶液、3滴浓 | 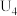 |

①实验1和2中正极的电极反应式为
②由实验1和2可知,酸性越强,
 的氧化性越强,作出该判断的依据是
的氧化性越强,作出该判断的依据是③测得
 ,说明酸性对
,说明酸性对 的氧化性几乎无影响,解释原因:
的氧化性几乎无影响,解释原因:实验结论:若氧化剂被还原时有
 参加反应,酸性越强,氧化剂的氧化性越强;若氧化剂被还原时没有
参加反应,酸性越强,氧化剂的氧化性越强;若氧化剂被还原时没有 参加反应,酸性对氧化剂的氧化性几乎没有影响。
参加反应,酸性对氧化剂的氧化性几乎没有影响。迁移拓展:综合上述探究结果,丙同学进一步提出猜想,其他条件相同时,氧化剂浓度越大,其氧化性越强。
(3)结合乙同学的实验2,丙同学补充进行实验5,验证猜想成立,完成下表中的内容:
| 序号 | 溶液a | 电压表读数 |
| 5 |  |
您最近一年使用:0次
名校
解题方法
2 . 某实验小组学生为探究氧化性: Br2 > Fe3+ > I2,设计下列实验方案。
【查阅资料】电极电势如下表:(已知:电极电势越高,氧化性越强)
(1)FeCl3溶液的配制:取FeCl3固体溶于___________ ,再稀释至指定浓度。配制250mL 0.1mol/L FeCl3溶液,需5.0 mol/L FeCl3溶液的体积为___________ mL,配制过程,图中不需要使用的仪器有___________ (填仪器名称)。

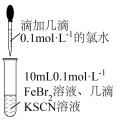
(2)利用FeBr2和氯水,设计实验证明氧化性:Br2 > Fe3+,实验如图所示,实验过程中,能证明氧化性:Br2 > Fe3+的现象是___________ 。
(3)利用0.1mol/L的FeCl3溶液和0.1mol/L的 溶液,不用任何试剂证明氧化性:Fe3+ > I2,FeCl3溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
溶液,不用任何试剂证明氧化性:Fe3+ > I2,FeCl3溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
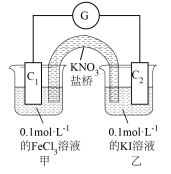
①通过外电路中电子流向:___________ (用C1、C2和→表示),可证明氧化性: 。
。
②也可通过甲池中颜色变化证明,甲池中颜色变化为___________ 。
(4)化学能可转化为电能,写出其在生活中常见的一种应用___________ 。
【查阅资料】电极电势如下表:(已知:电极电势越高,氧化性越强)
| 氧化还原电对(氧化型/还原型) | 电极反应式(氧化型+ne-=还原型) | 电极电势(E0/V) |
| Fe3+ +/ Fe2 | Fe3+ + e- = Fe2+ | 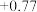 |
| I2 /I- | I2 + 2e- = 2I- | 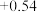 |
| Br2 /Br- | Br2 + 2e- = 2 Br- | 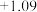 |

(2)利用FeBr2和氯水,设计实验证明氧化性:Br2 > Fe3+,实验如图所示,实验过程中,能证明氧化性:Br2 > Fe3+的现象是

(3)利用0.1mol/L的FeCl3溶液和0.1mol/L的
 溶液,不用任何试剂证明氧化性:Fe3+ > I2,FeCl3溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
溶液,不用任何试剂证明氧化性:Fe3+ > I2,FeCl3溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
①通过外电路中电子流向:
 。
。②也可通过甲池中颜色变化证明,甲池中颜色变化为
(4)化学能可转化为电能,写出其在生活中常见的一种应用
您最近一年使用:0次
名校
3 . 几种离子在水溶液中有如下转化关系。下列说法正确的是


A.该条件下的氧化性: |
B.反应(1)中,每生成 ,转移3mol电子 ,转移3mol电子 |
C.将反应(2)设计成原电池, 向负极迁移 向负极迁移 |
D. 与 与 反应生成 反应生成 和 和 时,氧化剂与还原剂的物质的量之比为1∶2 时,氧化剂与还原剂的物质的量之比为1∶2 |
您最近一年使用:0次
2022-03-06更新
|
1069次组卷
|
8卷引用:广东省广州市第十六中学2021-2022学年高一下学期期中检测 化学试题
广东省广州市第十六中学2021-2022学年高一下学期期中检测 化学试题广东省江门市新会第一中学2022-2023学年高一下学期3月月考化学试题河北省秦皇岛市青龙满族自治县 2021-2022学年高三下学期月考化学试题(已下线)秘籍12 原电池原理及应用-备战2022年高考化学抢分秘籍(全国通用)(已下线)专题04 氧化还原反应-三年(2020-2022)高考真题分项汇编(已下线)专题04 氧化还原反应-2022年高考真题模拟题分项汇编(已下线)微专题08 氧化性和还原性强弱的实验探究及应用-备战2023年高考化学一轮复习考点微专题(已下线)【2023】【高一下】【其他】【余高2】【高中化学】【刘尼尼收集】
名校
4 . 实验室用浓硫酸、铜与NaOH溶液为原料制取少量 并探究其性质。
并探究其性质。
I.制备 (装置如图所示)。
(装置如图所示)。
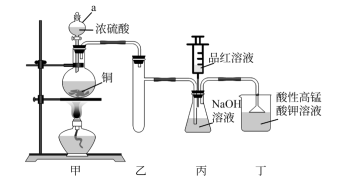
(1)仪器a的名称是___________ 。
(2)装置丁的作用有①吸收尾气,防止环境污染;②___________ ;③___________ 。
(3)证明丙中NaOH已完全转化为 的操作和现象是
的操作和现象是___________ 。
II.探究 与
与 的反应,设计实验如下:向2mL1mol/L
的反应,设计实验如下:向2mL1mol/L 溶液中加入2mL1mol/L
溶液中加入2mL1mol/L 溶液,得到绿色溶液,3min内无明显变化。将所得混合液分为两等份,进行实验Ⅰ和Ⅱ。
溶液,得到绿色溶液,3min内无明显变化。将所得混合液分为两等份,进行实验Ⅰ和Ⅱ。
(4)推测实验Ⅱ产生的无色气体为 ,实验证实推测正确:用滴有碘水的淀粉试纸接近试管口,观察到
,实验证实推测正确:用滴有碘水的淀粉试纸接近试管口,观察到___________ ,反应的离子方程式为___________ 。
(5)对实验Ⅱ产生 的原因进行分析,提出两种假设:
的原因进行分析,提出两种假设:
假设1: 水解使溶液中
水解使溶液中 增大。
增大。
假设2: 存在时,
存在时, 与
与 反应生成CuCl白色沉淀,溶液中
反应生成CuCl白色沉淀,溶液中 增大。
增大。
①假设1不合理,实验证据是___________ 。
②实验证实假设2合理,实验Ⅱ中发生反应的离子方程式有______ ,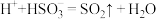 。
。
(6)通过上述分析可知, 增强了
增强了 的氧化性。某同学设计原电池实验证明该实验结果。
的氧化性。某同学设计原电池实验证明该实验结果。
①补全乙实验的现象___________ 。
②已知E为电池电动势[电池电动势即电池的理论电压,是两个电极电位之差,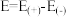 ],
], 为电池反应的自由能变,则甲电池与乙电池相比较,
为电池反应的自由能变,则甲电池与乙电池相比较,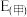
___________ 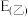 ,
,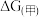
___________ 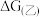 (填“>”或“<”)。
(填“>”或“<”)。
 并探究其性质。
并探究其性质。I.制备
 (装置如图所示)。
(装置如图所示)。
(1)仪器a的名称是
(2)装置丁的作用有①吸收尾气,防止环境污染;②
(3)证明丙中NaOH已完全转化为
 的操作和现象是
的操作和现象是II.探究
 与
与 的反应,设计实验如下:向2mL1mol/L
的反应,设计实验如下:向2mL1mol/L 溶液中加入2mL1mol/L
溶液中加入2mL1mol/L 溶液,得到绿色溶液,3min内无明显变化。将所得混合液分为两等份,进行实验Ⅰ和Ⅱ。
溶液,得到绿色溶液,3min内无明显变化。将所得混合液分为两等份,进行实验Ⅰ和Ⅱ。| 实验 | 操作及现象 |
| Ⅰ | 加入适量 固体,瞬间无明显变化,30s时也无明显变化。 固体,瞬间无明显变化,30s时也无明显变化。 |
| Ⅱ | 加入适量NaCl固体,瞬间无明显变化,30s时有无色气体和白色沉淀,上层溶液颜色变浅。 |
 ,实验证实推测正确:用滴有碘水的淀粉试纸接近试管口,观察到
,实验证实推测正确:用滴有碘水的淀粉试纸接近试管口,观察到(5)对实验Ⅱ产生
 的原因进行分析,提出两种假设:
的原因进行分析,提出两种假设:假设1:
 水解使溶液中
水解使溶液中 增大。
增大。假设2:
 存在时,
存在时, 与
与 反应生成CuCl白色沉淀,溶液中
反应生成CuCl白色沉淀,溶液中 增大。
增大。①假设1不合理,实验证据是
②实验证实假设2合理,实验Ⅱ中发生反应的离子方程式有
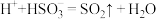 。
。(6)通过上述分析可知,
 增强了
增强了 的氧化性。某同学设计原电池实验证明该实验结果。
的氧化性。某同学设计原电池实验证明该实验结果。①补全乙实验的现象
| 编号 | 甲 | 乙 |
| 实验 | 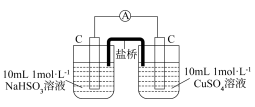 | 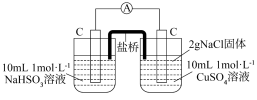 |
| 现象 | 电流计指针发生微小偏转 |
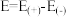 ],
], 为电池反应的自由能变,则甲电池与乙电池相比较,
为电池反应的自由能变,则甲电池与乙电池相比较,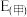
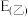 ,
,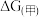
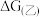 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解题方法
5 . 某小组拟探究双氧水和铁离子的氧化性强弱,设计如下实验装置。
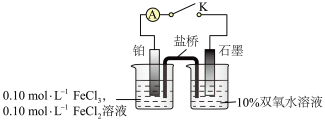
注明:盐桥为饱和KCl溶液和琼脂,烧杯中溶液均为100mL.
(1)用30%双氧水配制10%的双氧水需要使用的玻璃仪器有__________________ (填名称)。已知:30%双氧水的密度约为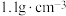 ,该双氧水溶液的物质的量浓度约为
,该双氧水溶液的物质的量浓度约为________ (保留1位小数)。
(2)关闭K,电流计显示电子由石墨极流出经外电路流入铂极。盐桥中阳离子向________ (填“石墨”或“铂”)极迁移。负极反应式为_____________________ 。若忽略体积变化和盐类水解,电路上转移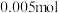 电子,则
电子,则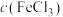
_________ (填“净增”或“净减”)_______  。
。
(3)一段时间后,向石墨极烧杯中加入适量30%双氧水和硫酸,电流计显示:电子由铂极流入石墨极。此时,铂极是___________ (填“正极”或“负极”)。
(4)结合上述(2)、(3)实验现象,可以得出的结论是__________ 。

注明:盐桥为饱和KCl溶液和琼脂,烧杯中溶液均为100mL.
(1)用30%双氧水配制10%的双氧水需要使用的玻璃仪器有
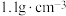 ,该双氧水溶液的物质的量浓度约为
,该双氧水溶液的物质的量浓度约为(2)关闭K,电流计显示电子由石墨极流出经外电路流入铂极。盐桥中阳离子向
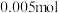 电子,则
电子,则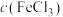
 。
。(3)一段时间后,向石墨极烧杯中加入适量30%双氧水和硫酸,电流计显示:电子由铂极流入石墨极。此时,铂极是
(4)结合上述(2)、(3)实验现象,可以得出的结论是
您最近一年使用:0次
名校
解题方法
6 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 酸性: | 电负性: |
B | 碳酸氢钠用作面团膨松剂 | 碳酸氢钠可以与碱反应 |
C | 马口铁(镀锡铁)出现刮痕后浸泡在饱和食盐水中,一段时间后,滴入几滴 | 锡做原电池的负极 |
D | 将在空气中灼烧呈黑色的铜丝趁热插入盛有乙醇的试管中,铜丝会变红色 | 乙醇具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-24更新
|
331次组卷
|
4卷引用:广东省东莞中学、广州二中、惠州一中等六校联考2023-2024学年高三下学期(第六次)开学化学试题
名校
7 . 下列说法正确的是
| A.用含有少量硫酸铜的稀硫酸跟锌粒反应,能加快产生氢气,说明Cu2+具有催化能力 |
| B.增大浓度会加快化学反应速率,是因为增加了反应物单位体积内活化分子的百分数 |
| C.等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA<HB |
| D.碱性锌锰电池是一种常见的二次电池 |
您最近一年使用:0次
2021-09-23更新
|
141次组卷
|
2卷引用:广东省东莞市东莞中学松山湖学校2023-2024学年高二上学期期中考试化学试题
解题方法
8 . 物质有从浓度大的区域向浓度小的区域扩散的趋势,利用该趋势可设计浓差电池。如图所示装置可测定氧气的含量,参比侧通入纯氧,测量侧气压调节到与参比测相同,接通电路,通过电势差大小可测出测量侧气体的含氧量。下列说法不正确的是


| A.参比侧为正极 |
| B.负极的电极反应式为2O2——4e—=O2↑ |
| C.测量侧处于封闭环境时,初期的读数比较准确 |
| D.相同压强下,电势差越大,测量侧气体中含氧量越高 |
您最近一年使用:0次



 溶液,出现蓝色沉淀
溶液,出现蓝色沉淀

