名校
解题方法
1 . 为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
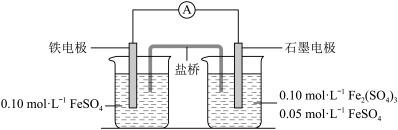
回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、________ (从下列图中选择,写出名称)。
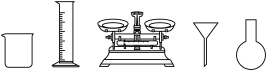
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________ 作为电解质。
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________ 电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________ 。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为________ ,铁电极的电极反应式为______________ 。因此,验证了Fe2+氧化性小于Fe3+还原性小于Fe。

回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、

(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择
| 阳离子 | u∞×108/(m2·s-1·V-1) | 阴离子 | u∞×108/(m2·s-1·V-1) |
| Li+ | 4.07 |  | 4.61 |
| Na+ | 5.19 |  | 7.40 |
| Ca2+ | 6.59 | Cl- | 7.91 |
| K+ | 7.62 |  | 8.27 |
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为
您最近一年使用:0次
2021-01-12更新
|
135次组卷
|
2卷引用:新疆伊犁奎屯市第一高级中学2020-2021学年高二上学期期末考试化学试题
2 . 按要求回答问题
(1)一种电解法制备高纯铬和硫酸的简单装置如图所示,请回答下列问题。
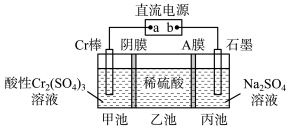
a为直流电源的_______ (填“正”或“负”)极;阳极反应式为_______ 工作时乙池中溶液的
_______ (填“增大”、“减小”或“不变”);若有 离子通过A膜,理论上阳极生成
离子通过A膜,理论上阳极生成_______  气体。
气体。
(2)为了验证 与
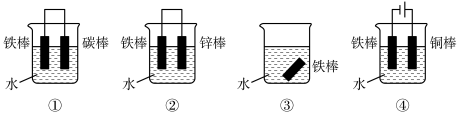
与 氧化性强弱,图中装置能达到实验目的是
氧化性强弱,图中装置能达到实验目的是_______ (填序号)。

(3)图中各个装置中铁棒被腐蚀由易到难的顺序是_______ 。
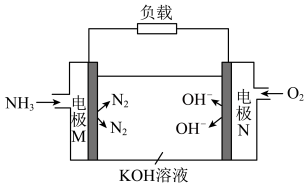
(4)甲醇( )燃料电池,两电极均为铂网,电解质溶液为
)燃料电池,两电极均为铂网,电解质溶液为 ,写出该原电池负极的电极反应式为
,写出该原电池负极的电极反应式为_______ 。
(1)一种电解法制备高纯铬和硫酸的简单装置如图所示,请回答下列问题。

a为直流电源的

 离子通过A膜,理论上阳极生成
离子通过A膜,理论上阳极生成 气体。
气体。(2)为了验证
 与
与 氧化性强弱,图中装置能达到实验目的是
氧化性强弱,图中装置能达到实验目的是
(3)图中各个装置中铁棒被腐蚀由易到难的顺序是

(4)甲醇(
 )燃料电池,两电极均为铂网,电解质溶液为
)燃料电池,两电极均为铂网,电解质溶液为 ,写出该原电池负极的电极反应式为
,写出该原电池负极的电极反应式为
您最近一年使用:0次
2022-03-20更新
|
151次组卷
|
3卷引用:新疆维吾尔自治区和田地区于田县2022-2023学年高二上学期11月期中化学试题
名校
解题方法
3 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
(1)下列化学反应过程中的能量变化符合图示的是___________ (填序号)。
①酸碱中和反应 ②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧 ⑤灼热的碳与二氧化碳反应 ⑥ 与
与 反应
反应 的反应过程如图所示:
的反应过程如图所示: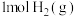 和
和 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收___________ kJ能量,生成物中新键形成共放出___________ kJ能量,该反应为___________ (填“吸热”或“放热”)反应。
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(3)现有如下两个反应:A ;B.
;B.  ,判断上述两个反应中能设计成原电池的是
,判断上述两个反应中能设计成原电池的是___________ (填“A”或“B”)。
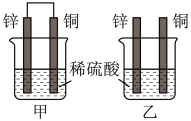
(4)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:___________ 。
A 甲、乙均为化学能转变为电能的装置 B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少 D. 两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:___________ 。
(5)若利用反应 设计一个原电池,请完善实验装置,负极材料:
设计一个原电池,请完善实验装置,负极材料:___________ ;正极材料:___________ ;电解质溶液:___________ 。
__________________ ___________ 。
(1)下列化学反应过程中的能量变化符合图示的是
①酸碱中和反应 ②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧 ⑤灼热的碳与二氧化碳反应 ⑥
 与
与 反应
反应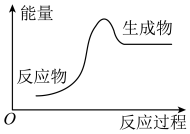
 的反应过程如图所示:
的反应过程如图所示: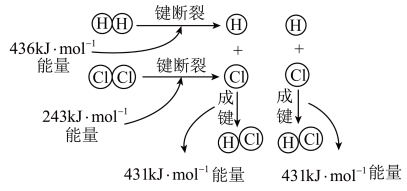
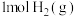 和
和 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(3)现有如下两个反应:A
 ;B.
;B.  ,判断上述两个反应中能设计成原电池的是
,判断上述两个反应中能设计成原电池的是(4)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
A 甲、乙均为化学能转变为电能的装置 B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少 D. 两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式:
(5)若利用反应
 设计一个原电池,请完善实验装置,负极材料:
设计一个原电池,请完善实验装置,负极材料: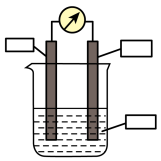
您最近一年使用:0次
4 . 用下列装置进行相应实验,能达到实验目的的是


| A.用装置甲验证浓硫酸的脱水性和强氧化性 |
| B.用装置乙验证浓硝酸的强氧化性 |
| C.用装置丙验证牺牲阳极的阴极保护法 |
| D.用装置丁验证镁片与稀盐酸反应放热 |
您最近一年使用:0次



