名校
解题方法
1 . 叠氮化钠( )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
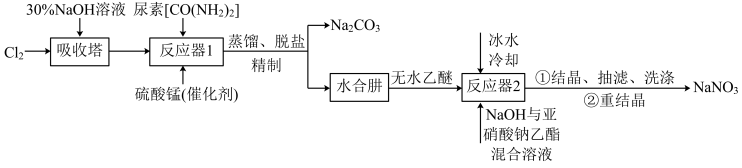
已知:① 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 ;
;
②一定条件下,碱性NaClO溶液与尿素溶液反应生成 。
。
回答下列问题:
(1)吸收塔内发生反应的离子方程式为_______ 。
(2)写出反应器1中生成水合肼反应的化学方程式:_______ 。
(3)反应器2中加入无水乙醚的作用是_______ 。
(4)已知亚硝酸乙酯的结构简式为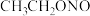 ,反应器2中生成
,反应器2中生成 和
和 。若生成39g
。若生成39g  ,则该反应中转移电子的物质的量为
,则该反应中转移电子的物质的量为_______ 。
(5)反应器1要控制NaClO溶液的用量,其主要目的是_______ 。
(6)某实验室设计了如图所示装置制备 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
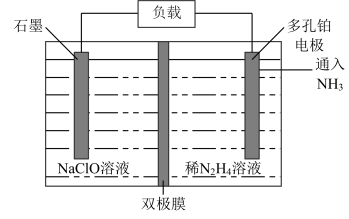
①双极膜中产生的_______ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②石墨电极反应式为_______ 。
 )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
已知:①
 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 ;
;②一定条件下,碱性NaClO溶液与尿素溶液反应生成
 。
。回答下列问题:
(1)吸收塔内发生反应的离子方程式为
(2)写出反应器1中生成水合肼反应的化学方程式:
(3)反应器2中加入无水乙醚的作用是
(4)已知亚硝酸乙酯的结构简式为
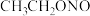 ,反应器2中生成
,反应器2中生成 和
和 。若生成39g
。若生成39g  ,则该反应中转移电子的物质的量为
,则该反应中转移电子的物质的量为(5)反应器1要控制NaClO溶液的用量,其主要目的是
(6)某实验室设计了如图所示装置制备
 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②石墨电极反应式为
您最近一年使用:0次
名校
2 . 下列装置或操作一定能达到实验目的的是
| A | B | C | D |
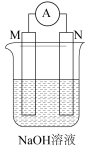 | 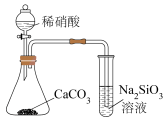 | 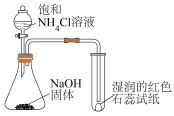 |  |
| 比较金属M和N的活动性 | 验证酸性: | 验证碱性:NaOH> | 验证氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-12更新
|
196次组卷
|
2卷引用:湖北省2023届高三5月联考化学试题
名校
解题方法
3 . 现有M、N、P、E四种金属,已知:①氧化性强弱顺序为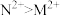 ;②E、P用导线连接放入稀硫酸中,P表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为
;②E、P用导线连接放入稀硫酸中,P表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为 ,
, 。则这四种金属的还原性由强到弱的顺序是
。则这四种金属的还原性由强到弱的顺序是
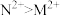 ;②E、P用导线连接放入稀硫酸中,P表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为
;②E、P用导线连接放入稀硫酸中,P表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为 ,
, 。则这四种金属的还原性由强到弱的顺序是
。则这四种金属的还原性由强到弱的顺序是A.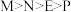 | B. |
C. | D.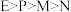 |
您最近一年使用:0次
2022-09-11更新
|
173次组卷
|
2卷引用:湖北省襄阳市第一中学2022-2023学年高二上学期12月线上考试化学试题
名校
解题方法
4 . 某同学研究FeSO4溶液和AgNO3溶液的反应,设计如下对比实验。
下列说法正确的是
| 实验 |  Ⅰ |  Ⅱ |
| 现象 | 连通电路后,电流表指针向右偏转,分别取反应前和反应一段时间后甲烧杯中的溶液,滴加KSCN溶液,前者几乎无色,后者显红色 | 连通电路后,电流表指针向左发生微小的偏转,丙、丁烧杯中均无明显现象 |
下列说法正确的是
| A.仅由Ⅰ中的现象可推知Ag+的氧化性强于Fe3+ |
| B.Ⅱ中电流表指针向左偏转的原因是Fe2+氧化了银电极 |
| C.Ⅱ中若将银电极换成石墨电极,电流表指针可能不再向左偏转 |
| D.对比Ⅰ、Ⅱ可知,Ⅰ中NO3-氧化了Fe2+ |
您最近一年使用:0次
2020-06-11更新
|
3817次组卷
|
8卷引用:湖北省沙市中学2021-2022学年高二上学期期末考试化学试题
解题方法
5 . 某实验小组在做 与
与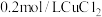 溶液反应的实验时,发现产生了白色沉淀。常温下,该实验小组对白色沉淀进行如下探究,操作与现象如下表所示:
溶液反应的实验时,发现产生了白色沉淀。常温下,该实验小组对白色沉淀进行如下探究,操作与现象如下表所示:
资料显示; 是一种白色、难溶于水的固体,可溶于氨水形成无色的
是一种白色、难溶于水的固体,可溶于氨水形成无色的 。
。 可 溶于氨水,
可 溶于氨水,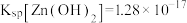 。
。
回答下列问题:
(1)步骤ⅰ中测量溶液 最适宜的方法是
最适宜的方法是_______ (填标号)。
a.广泛 试纸 b.精密
试纸 b.精密 试纸 c.
试纸 c. 计
计
(2)步骤ⅰ产生的气体是_______ 。
(3)步骤ⅲ中加少量植物油的目的是_______ 。
(4)测得“白色悬浊液A”的 ,判断“白色悬浊液A”中是否含有
,判断“白色悬浊液A”中是否含有
_______ (请写出计算过程)。
(5)步骤ⅳ中无色溶液变为深蓝色溶液的原因是_______ (用离子方程式表示)。
(6)由上述实验可知A为 悬浊液。为探究其产生的原因,设计如下实验:
悬浊液。为探究其产生的原因,设计如下实验:
v)将紫红色固体B加入到a mol/L的 溶液中,出现白色悬浊液;
溶液中,出现白色悬浊液;
vi)在隔绝空气条件下设计如图所示的原电池,30min后,观察到右侧烧杯中出现白色悬浊液,石墨棒上未见红色固体。

①步骤v中a_______ 0.2(填“>“<”或“=”)。
②该原电池的总离子反应方程式为_______ 。
(7)综合上述实验,下列说法正确的是_______ (填标号)。
a.置换反应都能设计成双液原电池,以加快反应速率
b.原电池反应中,阴离子可能对阳离子放电产生影响
c. 与
与 溶液反应得到
溶液反应得到 的途径可能不止一种
的途径可能不止一种
d. 与
与 溶液反应过程中,氢气生成速率持续减慢
溶液反应过程中,氢气生成速率持续减慢
 与
与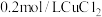 溶液反应的实验时,发现产生了白色沉淀。常温下,该实验小组对白色沉淀进行如下探究,操作与现象如下表所示:
溶液反应的实验时,发现产生了白色沉淀。常温下,该实验小组对白色沉淀进行如下探究,操作与现象如下表所示:| 实验步骤 | 实验现象 |
ⅰ)将锌片置于盛有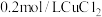 溶液( 溶液( )的烧杯中 )的烧杯中 | 锌片表面产生暗红色疏松圆体物,30min后有大量气泡产生 |
| ⅱ)取出锌片,疏松固体物脱落,搅拌并静置 | 烧杯中出现白色悬浊液A和颗粒状紫红色固体B |
| ⅲ)用注射器吸取部分上层白色悬浊液A于试管中,立即加入少量植物油覆盖 | |
| ⅳ)用长胶头滴管伸入A中,加入适量氨水;再向其中通入空气 | 加入氨水后沉淀溶解,得到无色溶液,通入空气后溶液变为深蓝色 |
 是一种白色、难溶于水的固体,可溶于氨水形成无色的
是一种白色、难溶于水的固体,可溶于氨水形成无色的 。
。 可 溶于氨水,
可 溶于氨水,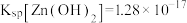 。
。回答下列问题:
(1)步骤ⅰ中测量溶液
 最适宜的方法是
最适宜的方法是a.广泛
 试纸 b.精密
试纸 b.精密 试纸 c.
试纸 c. 计
计(2)步骤ⅰ产生的气体是
(3)步骤ⅲ中加少量植物油的目的是
(4)测得“白色悬浊液A”的
 ,判断“白色悬浊液A”中是否含有
,判断“白色悬浊液A”中是否含有
(5)步骤ⅳ中无色溶液变为深蓝色溶液的原因是
(6)由上述实验可知A为
 悬浊液。为探究其产生的原因,设计如下实验:
悬浊液。为探究其产生的原因,设计如下实验:v)将紫红色固体B加入到a mol/L的
 溶液中,出现白色悬浊液;
溶液中,出现白色悬浊液;vi)在隔绝空气条件下设计如图所示的原电池,30min后,观察到右侧烧杯中出现白色悬浊液,石墨棒上未见红色固体。

①步骤v中a
②该原电池的总离子反应方程式为
(7)综合上述实验,下列说法正确的是
a.置换反应都能设计成双液原电池,以加快反应速率
b.原电池反应中,阴离子可能对阳离子放电产生影响
c.
 与
与 溶液反应得到
溶液反应得到 的途径可能不止一种
的途径可能不止一种d.
 与
与 溶液反应过程中,氢气生成速率持续减慢
溶液反应过程中,氢气生成速率持续减慢
您最近一年使用:0次
名校
解题方法
6 . 室温下,探究 溶液(pH=1)的性质,下列实验方案不能达到探究目的的是
溶液(pH=1)的性质,下列实验方案不能达到探究目的的是
 溶液(pH=1)的性质,下列实验方案不能达到探究目的的是
溶液(pH=1)的性质,下列实验方案不能达到探究目的的是| 选项 | 探究目的 | 实验方案 |
| A |  和I-能否发生可逆反应 和I-能否发生可逆反应 | 向 溶液中加入 溶液中加入 的 的 溶液充分反应后,将溶液分为两份,一份滴加几滴淀粉溶液,另一份滴加几滴 溶液充分反应后,将溶液分为两份,一份滴加几滴淀粉溶液,另一份滴加几滴 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |
| B | 证明 的氧化性 的氧化性 | 将铁片和石墨棒用导线相连,并连上电流表,插入到 溶液中,形成闭合电路后,观察电流表的指针变化情况 溶液中,形成闭合电路后,观察电流表的指针变化情况 |
| C |  能否净水 能否净水 | 取两份浑浊的泥水于两只试管中,向其中一份泥水中加入 溶液,静置 溶液,静置 ,观察两只试管中泥水的变化情况 ,观察两只试管中泥水的变化情况 |
| D |  能否催化 能否催化 分解 分解 | 取两份 溶液于两只试管中,向其中一份 溶液于两只试管中,向其中一份 溶液中滴加几滴 溶液中滴加几滴 溶液,观察两只试管中气泡产生的快慢情况 溶液,观察两只试管中气泡产生的快慢情况 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9-10高一下·黑龙江鹤岗·期末
名校
解题方法
7 . X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有H2放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为( )
| A.X>Z>Y>M | B.X>Y>Z>M |
| C.M>Z>X>Y | D.X>Z>M>Y |
您最近一年使用:0次
2020-03-19更新
|
262次组卷
|
26卷引用:2015-2016学年湖北省黄石市有色一中高二上学期10月月考化学试卷
2015-2016学年湖北省黄石市有色一中高二上学期10月月考化学试卷(已下线)09~10年鹤岗一中高一下学期期末考试化学卷(已下线)2010年福建省厦门六中高二上学期期中考试化学试卷(已下线)2010—2011学年河北省保北十二县市高一下学期期中联考化学试卷(已下线)2011-2012学年福建省罗源县第一中学高二上学期期中考试化学(理)试卷(已下线)2012-2013学年山东东营一中高二上学期第一次模块考试化学试卷(已下线)2012-2013学年内蒙古巴市中学高二12月月考化学试卷(已下线)2012-2013学年四川省雅安中学高二下学期期中考试化学试卷(已下线)2012-2013学年浙江省杭州市西湖高级中学高二5月月考化学试卷(已下线)2013-2014学年江苏省响水中学高二上学期期中考试化学试卷(选修)(已下线)2013-2014吉林省吉林一中高二下学期期末考试化学试卷(已下线)2014-2015学年浙江省杭州市西湖高级中学高二10月月考化学试卷2015届上海理工大学附中高三上学期月考化学试卷2014-2015陕西省西安市一中高二上学期期末化学试卷2014-2015学年四川省雅安中学高二下期末模拟化学试卷2014-2015学年重庆市主城区六校高二上期末联考化学试卷2016届辽宁省五校协作体高三上学期期初考试化学试卷2015-2016学年福建省龙海市程溪中学高二上学期期中测试化学试卷2015-2016学年辽宁庄河高中高二下期末化学试卷2017届北京市中央民族大学附中高三上9.12周练化学卷福建省三明市第一中学2017-2018学年高二上学期第一次月考化学试题甘肃省武威市第六中学2018-2019学年高一下学期第二次学段考试化学试题山西省太原市太原师范学院附属中学2019-2020学年高二上学期12月月考理科化学试题课时3 电能转化为化学能——A学习区 夯实基础(苏教版必修2)云南省云天化中学2019-2020学年高二下学期开学考试化学试题河北省衡水市武强中学2021-2022学年高二下学期期中考试化学试题
9-10高二下·江西·期中
名校
解题方法
8 . 根据下列事实,判断离子的氧化性顺序为①A+B2+=A2++B;②D+2H2O=D(OH)2+H2↑;③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-=E,B-2e-=B2+ ( )
| A.D2+>A2+>B2+>E2+ | B.D2+>E2+>A2+>B2+ |
| C.E2+>B2+>A2+>D2+ | D.A2+>B2+>D2+>E2+ |
您最近一年使用:0次
2019-12-25更新
|
399次组卷
|
20卷引用:湖北省武汉市钢城第四中学2019-2020高一下学期期中考试化学试题
湖北省武汉市钢城第四中学2019-2020高一下学期期中考试化学试题(已下线)09~10年江西四校高二下学期期中联考化学卷(已下线)2010年江西省吉安市高一下学期期末考试化学试题(已下线)2010年海南省嘉积中学高二上学期教学质量检测(三)化学试卷(已下线)2010年长春外国语学校高二第一学期期末考试化学试卷(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2011-2012学年陕西省宝鸡中学高二下学期期末考试化学试卷(已下线)2014年高一下学期化学必修2 2-2-1 化学能转化为电能练习卷2014-2015辽宁省实验中学分校高一下学期期中考试化学试卷2015-2016学年河北省石家庄市辛集中学高一下期中理科化学试卷云南省曲靖市第一中学2016-2017学年高一下学期期中考试化学试题甘肃省陇东中学2016-2017学年高一下学期期末考试化学试题黑龙江省鸡西市第十九中学2019届高三上学期期中考试化学试题(已下线)山东省济南市2019-2020年高三10月月考化学试题西藏自治区拉萨市那曲第二高级中学2018-2019学年高二下学期第一次月考化学试题北京市海淀区首都师范大学附属中学2019-2020学年高一下学期第二次月考化学试题第二章 化学反应与能量学 综合拓展——B 拓展区 夯实基础(人教版必修2)四川省达州市大竹中学2020-2021学年高一下学期期中考试化学试题(苏教版2019)必修第二册专题6 化学反应与能量变化 B 素养拓展区河北省保定市唐县第一中学2022-2023学年高一下学期5月月考化学试题
名校
解题方法
9 . 某课题组利用盐度梯度和氧化还原工艺,成功的设计了下图所示的电池装置,将酸性废水中存在的高毒性 转化为低毒性Cr3+。下 列说法正确的是
转化为低毒性Cr3+。下 列说法正确的是

 转化为低毒性Cr3+。下 列说法正确的是
转化为低毒性Cr3+。下 列说法正确的是 
| A.该装置为电解池,能量由电能转化为化学能 |
| B.左边电极反应式为: Cr(Ⅵ) +3e- =Cr(Ⅲ) |
| C.电池利用溶液盐度梯度产生电动势,C2表示低浓度盐溶液 |
D.若产生6.72L氧气,则理论上转化0.2 mol  |
您最近一年使用:0次
解题方法
10 . 如图所示,是原电池的装置图。请回答:
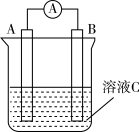
(1)若溶液C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为_______ ;反应进行一段时间后溶液C的酸性_______ (填“升高”“降低”或“基本不变”)
(2)若需将反应Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A极(负极)材料为_______ , B极电极反应式为_______ 。
(3)若C为CuCl2溶液,Zn是_______ 极,Cu极发生_______ 反应,电极反应为_______ 。反应过程溶液中c(Cu2+)_______ (填“变大”“变小”或“不变”)。
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:
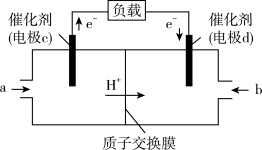
电池总反应为2CH3OH+3O2=2CO2+4H2O,则电极c是_______ (填“正极”或“负极”),若线路中转移2 mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为_______ L。

(1)若溶液C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若需将反应Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A极(负极)材料为
(3)若C为CuCl2溶液,Zn是
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则电极c是
您最近一年使用:0次



