解题方法
1 . 研究大气中含硫化合物(主要是SO2和H2S)的转化具有重要意义。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离H2,发生的反应为2H2S(g) 2H2(g)+S2(g) △H。
2H2(g)+S2(g) △H。
已知:①H2S(g) H2(g)+S(g) △H1;
H2(g)+S(g) △H1;
②2S(g) S2(g) △H2。
S2(g) △H2。
则△H=______ (用含△H1、△H2的式子表示)。
(2)土壤中的微生物可将大气中的H2S经两步反应氧化成SO ,两步反应的能量变化示意图如图:
,两步反应的能量变化示意图如图: (aq)的热化学方程式为
(aq)的热化学方程式为_______ 。
(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。______ 。
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有_______ 。
(4)二氧化硫—空气质子交换膜燃料电池可以利用大气中所含SO2快速启动,其装置示意图如图所示:______ (填“从A到B”或“从B到A”)。
②负极的电极反应为________ 。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离H2,发生的反应为2H2S(g)
 2H2(g)+S2(g) △H。
2H2(g)+S2(g) △H。已知:①H2S(g)
 H2(g)+S(g) △H1;
H2(g)+S(g) △H1;②2S(g)
 S2(g) △H2。
S2(g) △H2。则△H=
(2)土壤中的微生物可将大气中的H2S经两步反应氧化成SO
 ,两步反应的能量变化示意图如图:
,两步反应的能量变化示意图如图: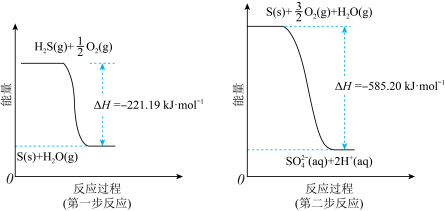
 (aq)的热化学方程式为
(aq)的热化学方程式为(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
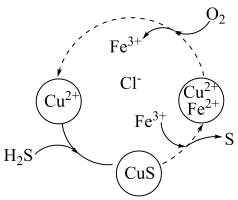
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有
(4)二氧化硫—空气质子交换膜燃料电池可以利用大气中所含SO2快速启动,其装置示意图如图所示:
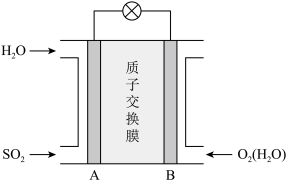
②负极的电极反应为
您最近一年使用:0次
解题方法
2 . 氨是一种重要的化工原料,电化学合成氨在工业上起着相当重要的作用。
(1)电解法合成氨反应装置如图所示:______ (填“阴”或“阳”)极。
②电解装置中质子交换膜的作用为_________ 。
(2)科学家研究通过一种生物燃料电池实现室温下合成氨,其工作原理如图所示:______ (填“a”或“b”)电极,正极的电极反应为________ ;对比传统的工业合成氨,生物燃料电池合成氨的优点是________ (任写一条)。
(3)以悬浮的纳米Fe2O3作催化剂,H2O和N2为原料直接常压电化学合成氨技术取得了突破性进展,其工作原理如图所示:_______ 。
②蒙乃尔筛网处发生的电极反应为_______ 。
(1)电解法合成氨反应装置如图所示:

②电解装置中质子交换膜的作用为
(2)科学家研究通过一种生物燃料电池实现室温下合成氨,其工作原理如图所示:
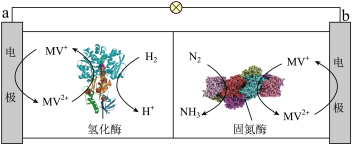
(3)以悬浮的纳米Fe2O3作催化剂,H2O和N2为原料直接常压电化学合成氨技术取得了突破性进展,其工作原理如图所示:
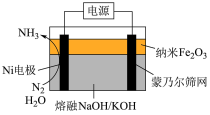
②蒙乃尔筛网处发生的电极反应为
您最近一年使用:0次



