解题方法
1 . 试运用所学的电化学知识回答下列问题:
(1)①请设计一个原电池,可自发进行反应: ,该电池的两电极分别为铜棒、银棒,请画出该实验的装置示意图:
,该电池的两电极分别为铜棒、银棒,请画出该实验的装置示意图:_______ 。该电池中,电子的流向为_______ 。
②该电化学装置的能量变化形式为_______ 。若开始时两电极质量相等,当电路中转移0.2mol电子时,理论上两电极的质量差为_______ g。
(2)科学家用氮化镓材料与铜组装成如图所示的人工光合系统实现 的再利用。电池的总反应为
的再利用。电池的总反应为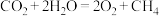 (已知:质子交换膜仅允许
(已知:质子交换膜仅允许 通过)。
通过)。_______ (填“GaN”或“Cu”)。
②该电池的Cu电极上发生的电极反应为_______ 。
③生成 ,消耗
,消耗 的物质的量为
的物质的量为_______ mol。
(1)①请设计一个原电池,可自发进行反应:
 ,该电池的两电极分别为铜棒、银棒,请画出该实验的装置示意图:
,该电池的两电极分别为铜棒、银棒,请画出该实验的装置示意图:②该电化学装置的能量变化形式为
(2)科学家用氮化镓材料与铜组装成如图所示的人工光合系统实现
 的再利用。电池的总反应为
的再利用。电池的总反应为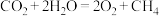 (已知:质子交换膜仅允许
(已知:质子交换膜仅允许 通过)。
通过)。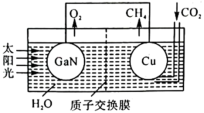
②该电池的Cu电极上发生的电极反应为
③生成
 ,消耗
,消耗 的物质的量为
的物质的量为
您最近一年使用:0次
解题方法
2 . NH3(含6个H-N)是一种重要的化工原料,在生产、生活中用途广泛。
(1)已知:
注:拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能
可逆反应N2(g)+3H2(g) 2NH(g) ∆H=
2NH(g) ∆H=___________ kJ•mol-1。
(2)在一定条件下,体积固定的体系中,建立如图所示的N2+3H2 2NH3平衡体系。
2NH3平衡体系。___________ (填“曲线A”、“曲线B”或“曲线C”)。
②0~tomin时,用H2表示化学反应速率是___________ mol•L•min-1。
③下列能说明该反应达到平衡的是___________ 。
A.混合气体的压强不再变化 B.c(H2)=c(NH3)
C.混合气体的质量不再变化 D.NH3的体积分数不再变化
(3)潜艇的液氨-液氧燃料电池示意图如图所示:___________ ,其中电极b是该电池的___________ 。
②电解质溶液中OH-离子向___________ 移动(填“电极a”或“电极b”)。
(4)火箭燃料N2H4具有强还原性,可用氨水与NaClO溶液反应制取,反应装置如图所示,其中分液漏斗中溶液是___________ 。
(1)已知:
| 共价键 | H-H | N≡N | N-H |
| 键能/kJ•mol-1 | 436 | 946 | 391 |
可逆反应N2(g)+3H2(g)
 2NH(g) ∆H=
2NH(g) ∆H=(2)在一定条件下,体积固定的体系中,建立如图所示的N2+3H2
 2NH3平衡体系。
2NH3平衡体系。
②0~tomin时,用H2表示化学反应速率是
③下列能说明该反应达到平衡的是
A.混合气体的压强不再变化 B.c(H2)=c(NH3)
C.混合气体的质量不再变化 D.NH3的体积分数不再变化
(3)潜艇的液氨-液氧燃料电池示意图如图所示:

②电解质溶液中OH-离子向
(4)火箭燃料N2H4具有强还原性,可用氨水与NaClO溶液反应制取,反应装置如图所示,其中分液漏斗中溶液是
您最近一年使用:0次
名校
解题方法
3 . 高分子有机物聚吡咯(PPy)是一种性能优异的光敏型半导体,其制成的纳米管在紫外光照射、关闭周期内会发生如下反应: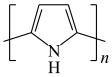 +H+
+H+
 。通过纳米管一端正电荷分布密度的变化,在电解质溶液中产生离子电流。某科研组使用PPy构建了一种浓差电池,用来提取天然水中的氢能,其构造如图所示。下列叙述正确的是
。通过纳米管一端正电荷分布密度的变化,在电解质溶液中产生离子电流。某科研组使用PPy构建了一种浓差电池,用来提取天然水中的氢能,其构造如图所示。下列叙述正确的是
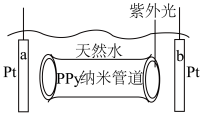
| A.a为负极,b为正极 |
B.b极电极方程式为 |
C.纳米管道中的离子电流由PPy阳离子、 、 、 、 、 的定向移动形成 的定向移动形成 |
| D.照射一段时间后关闭光源,纳米管道中仍能存在微弱电流 |
您最近一年使用:0次
2022-04-14更新
|
1872次组卷
|
6卷引用:化学-2022年高考押题预测卷02(江苏卷)
(已下线)化学-2022年高考押题预测卷02(江苏卷)浙江省台州市2022届高三下学期4月教学质量评估(二模)化学试题(已下线)卷05 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)易混易错4 电化学应用中的易错点河南省南阳市第八中学校2022-2023学年高三下学期第七次调研考试理科综合试卷-高中化学浙江省杭州市西湖高级中学2024届高三下学期5月模拟预测化学试题
21-22高三上·江苏·期中
名校
解题方法
4 . 纳米零价铁除去酸性废水中的三氯乙烯、五价砷的原理如图所示,下列说法正确的是
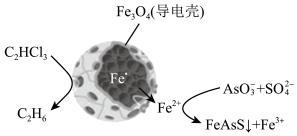

| A.该处理过程中将电能转化为化学能 |
| B.该处理过程中纳米零价铁中的Fe为正极 |
| C.每生成11.2L乙烷,转移电子0.4mol |
| D.酸性废水中的五价砷除去过程中As和S都被Fe2+还原了 |
您最近一年使用:0次
2021-11-28更新
|
990次组卷
|
4卷引用:【苏州新东方】2022新高考基地学校期中大联考化学
(已下线)【苏州新东方】2022新高考基地学校期中大联考化学江苏省盐城市五校2023届高三上学期期末联考化学试题江苏省常州市第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题07 化学能与热能、电能-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(江苏专用)
名校
5 . I.中学化学常见物质A、B、C、D、X、Y,存在如下图转化关系(部分物质和条件略去)。
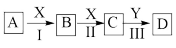
①若A为NaOH溶液,X为CO2,D是沉淀,则Y可为___________ 。(填序号)。
A.SO3B.Ba(OH)2C.H2SO4D.CaO
②若A为碱性气体,X为O2,A与D反应生成一种化肥,则反应Ⅲ的化学方程式为___________ 。
II.氨氮废水的处理流程如图所示:

①过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。请用离子方程式表示加NaOH溶液时所发生的反应:___________ 。
②过程Ⅱ:在微生物的作用、碱性条件下NH 被氧化成NO
被氧化成NO 的离子方程式为:
的离子方程式为:___________ 。
III.金属可用于还原废水中的Cr(Ⅵ)。
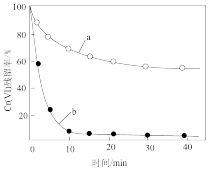
(1)其他条件相同时,用相同物质的量的Zn粉、Zn-Cu粉分别处理pH=2.5的含Cr(Ⅵ)废水,废水中Cr(Ⅵ)残留率随时间的变化如图所示。图中b对应的实验方法处理含Cr(Ⅵ)废水的效果更好,其原因是___________ (用文字说明)。
(2)用氧化铁包裹的纳米铁粉(用Fe/Fe2O3表示)能有效还原水溶液中的Cr(Ⅵ)。Fe/Fe2O3还原近中性废水中Cr(Ⅵ)的可能反应机理如图所示。Fe/Fe2O3中Fe还原CrO 的过程为:
的过程为:
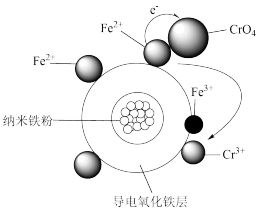
①单质铁发生吸氧腐蚀,铁的电极反应式为___________
②CrO 被还原的离子方程式
被还原的离子方程式___________
①若A为NaOH溶液,X为CO2,D是沉淀,则Y可为
A.SO3B.Ba(OH)2C.H2SO4D.CaO
②若A为碱性气体,X为O2,A与D反应生成一种化肥,则反应Ⅲ的化学方程式为
II.氨氮废水的处理流程如图所示:

①过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。请用离子方程式表示加NaOH溶液时所发生的反应:
②过程Ⅱ:在微生物的作用、碱性条件下NH
 被氧化成NO
被氧化成NO 的离子方程式为:
的离子方程式为:III.金属可用于还原废水中的Cr(Ⅵ)。
(1)其他条件相同时,用相同物质的量的Zn粉、Zn-Cu粉分别处理pH=2.5的含Cr(Ⅵ)废水,废水中Cr(Ⅵ)残留率随时间的变化如图所示。图中b对应的实验方法处理含Cr(Ⅵ)废水的效果更好,其原因是

(2)用氧化铁包裹的纳米铁粉(用Fe/Fe2O3表示)能有效还原水溶液中的Cr(Ⅵ)。Fe/Fe2O3还原近中性废水中Cr(Ⅵ)的可能反应机理如图所示。Fe/Fe2O3中Fe还原CrO
 的过程为:
的过程为:
①单质铁发生吸氧腐蚀,铁的电极反应式为
②CrO
 被还原的离子方程式
被还原的离子方程式
您最近一年使用:0次
2021-07-21更新
|
913次组卷
|
2卷引用:江苏省前黄高级中学 2020—2021学年高一下学期3月学情检测化学试题
名校
解题方法
6 . 氨浸菱锌矿制备活性氧化锌,成本低,选择性好,其工艺流程如下:
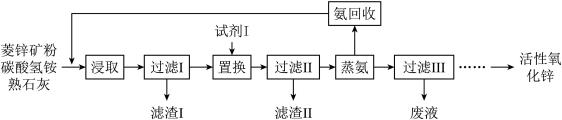
(1)滤渣Ⅰ主要成分的化学式为__________ 。
(2)浸取液中含少量Pb2+、Cu2+等重金属离子,可加入试剂Ⅰ除去,试剂Ⅰ为______________ ,但在实际操作过程中实际加入量远高于理论量,可能的原因是____________________________ 。
(3)过滤Ⅱ 后得到Zn(NH3)4CO3 溶液,经直接蒸汽加热可析出碱式碳酸锌[ZnCO3·2Zn(OH)2·H2O]沉淀,其反应化学方程式为____________________________ 。
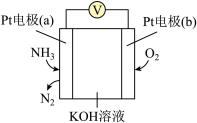
(4)蒸氨过程中会有部分氨气逸出,可用电化学气敏传感器监测环境中NH3 的含量,原理如图所示。负极的电极反应为________________________________ ,假设蒸氨过程中逸出氨气16.8L (标准状况) 进入传感器,另一极需要通入标准状况下O2的体积为____________________ 。
(5)蒸氨完成时,废液中残余氨含量需小于0.2mol/L,如果残余氨浓度过低,蒸汽用量增大,回收氨水中氨浓度降低,不利于循环使用;如果残余氨浓度过高,会导致____________________________ 。

(1)滤渣Ⅰ主要成分的化学式为
(2)浸取液中含少量Pb2+、Cu2+等重金属离子,可加入试剂Ⅰ除去,试剂Ⅰ为
(3)过滤Ⅱ 后得到Zn(NH3)4CO3 溶液,经直接蒸汽加热可析出碱式碳酸锌[ZnCO3·2Zn(OH)2·H2O]沉淀,其反应化学方程式为
(4)蒸氨过程中会有部分氨气逸出,可用电化学气敏传感器监测环境中NH3 的含量,原理如图所示。负极的电极反应为

(5)蒸氨完成时,废液中残余氨含量需小于0.2mol/L,如果残余氨浓度过低,蒸汽用量增大,回收氨水中氨浓度降低,不利于循环使用;如果残余氨浓度过高,会导致
您最近一年使用:0次



