解题方法
1 .  是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。
【 的制备】
的制备】
(1)用下图装置制备 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是___________ 。 ;
;___________ 。
【 的性质探究】
的性质探究】
资料:i. 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。
ii.单质硫可溶于 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。
某小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是___________ 。
②同学讨论后,设计了如下实验,证实该条件下 的确可以将
的确可以将 氧化成
氧化成 。
。___________ 。
b.连通后电流计指针偏转,一段时间后,___________ (填操作和现象)。
(4)实验I的现象与资料i不相符,其原因是新生成的产物( )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是___________ 。
(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是___________ ,请设计验证此猜想的实验方案___________ 。
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与___________ 等因素有关。
 是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。【
 的制备】
的制备】(1)用下图装置制备
 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是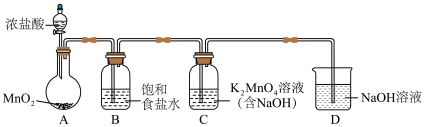
 ;
;【
 的性质探究】
的性质探究】资料:i.
 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。ii.单质硫可溶于
 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。某小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | 实验过程 | 实验现象 |
| Ⅰ |
| 紫色变浅( ),生成棕褐色沉淀( ),生成棕褐色沉淀( ) ) |
| Ⅱ |
| 溶液呈淡黄色( ),生成浅粉色沉淀(MnS) ),生成浅粉色沉淀(MnS) |
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有
 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是②同学讨论后,设计了如下实验,证实该条件下
 的确可以将
的确可以将 氧化成
氧化成 。
。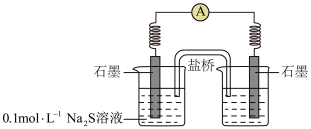
b.连通后电流计指针偏转,一段时间后,
(4)实验I的现象与资料i不相符,其原因是新生成的产物(
 )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与
您最近一年使用:0次
名校
解题方法
2 . 我国科学家最近开发出锌硒电池,工作原理如图所示。放电时,电池总反应为Se+2CuSO4+2Zn=Cu2Se+2ZnSO4。下列说法错误的是
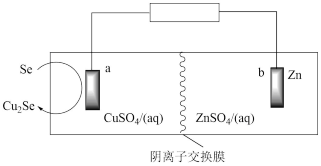

| A.放电时化学能转化成电能 |
B.b极的电极反应式为 |
C.放电时,溶液中 向a极迁移 向a极迁移 |
| D.79gSe完全反应时外电路中转移2mol电子 |
您最近一年使用:0次
2022-11-12更新
|
501次组卷
|
5卷引用:专题05 化学能与电能的转化(测)-2023年高考化学二轮复习讲练测(新高考专用)
(已下线)专题05 化学能与电能的转化(测)-2023年高考化学二轮复习讲练测(新高考专用)河北省高碑店市崇德实验中学2022-2023学年高三上学期期中考试化学试题湖南省株洲市攸县第二中学2022-2023学年高三上学期第三次月考化学试题(已下线)2019年高考海南卷化学试题变式题(不定项选择题)江西省宜春市宜丰中学2022-2023学年高一上学期12月月考化学试题
名校
解题方法
3 . 当氧化剂电对的电极电势大于还原剂电对的电极电势时,氧化还原反应才能进行。用如图所示装置探究原电池的工作原理,其中 、
、 均为碳棒,此时电流表的指针不发生偏转。已知:①反应
均为碳棒,此时电流表的指针不发生偏转。已知:①反应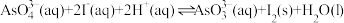 中的两个电对的标准电极电势
中的两个电对的标准电极电势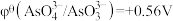 ,
, 。②标准电动势
。②标准电动势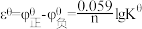 ,n为转移的电子数。下列说法错误的是
,n为转移的电子数。下列说法错误的是

 、
、 均为碳棒,此时电流表的指针不发生偏转。已知:①反应
均为碳棒,此时电流表的指针不发生偏转。已知:①反应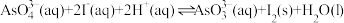 中的两个电对的标准电极电势
中的两个电对的标准电极电势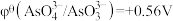 ,
, 。②标准电动势
。②标准电动势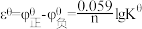 ,n为转移的电子数。下列说法错误的是
,n为转移的电子数。下列说法错误的是
| A.若向右侧烧杯中滴加浓盐酸,电流计指针会发生偏转 |
B.若向右侧烧杯中滴加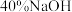 溶液,此时 溶液,此时 电极的电极反应式为 电极的电极反应式为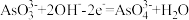 |
C.向右侧烧杯中加入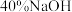 溶液时,盐桥中的阳离子向左侧烧杯移动 溶液时,盐桥中的阳离子向左侧烧杯移动 |
D.反应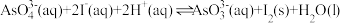 的 的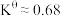 |
您最近一年使用:0次
2022-05-31更新
|
1229次组卷
|
4卷引用:山东省日照市2022届高三校际联考(三模)化学试题
山东省日照市2022届高三校际联考(三模)化学试题(已下线)第18讲 原电池 化学电源(练)-2023年高考化学一轮复习讲练测(全国通用)安徽省六安第一中学2022-2023学年高三上学期第四次月考化学试题(已下线)专题8 新概念应用
解题方法
4 . 纳米零价铁电化学法除去酸性废水(含有NO )中的三氯乙烯的原理如图所示。下列有关说法不正确的是
)中的三氯乙烯的原理如图所示。下列有关说法不正确的是

 )中的三氯乙烯的原理如图所示。下列有关说法不正确的是
)中的三氯乙烯的原理如图所示。下列有关说法不正确的是
| A.该处理过程中化学能转化为电能 |
B.②对应的电极反应式为:NO +10H++8e-=NH +10H++8e-=NH +3H2O +3H2O |
| C.若消耗amol零价铁,则可除去0.25amol三氯乙烯 |
| D.增大单位体积内的纳米零价铁投入量,可提高三氯乙烯的去除效率 |
您最近一年使用:0次
名校
解题方法
5 . 高分子有机物聚吡咯(PPy)是一种性能优异的光敏型半导体,其制成的纳米管在紫外光照射、关闭周期内会发生如下反应: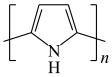 +H+
+H+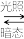
 。通过纳米管一端正电荷分布密度的变化,在电解质溶液中产生离子电流。某科研组使用PPy构建了一种浓差电池,用来提取天然水中的氢能,其构造如图所示。下列叙述正确的是
。通过纳米管一端正电荷分布密度的变化,在电解质溶液中产生离子电流。某科研组使用PPy构建了一种浓差电池,用来提取天然水中的氢能,其构造如图所示。下列叙述正确的是
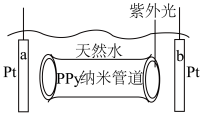
| A.a为负极,b为正极 |
B.b极电极方程式为 |
C.纳米管道中的离子电流由PPy阳离子、 、 、 、 、 的定向移动形成 的定向移动形成 |
| D.照射一段时间后关闭光源,纳米管道中仍能存在微弱电流 |
您最近一年使用:0次
2022-04-14更新
|
1872次组卷
|
6卷引用:浙江省台州市2022届高三下学期4月教学质量评估(二模)化学试题
浙江省台州市2022届高三下学期4月教学质量评估(二模)化学试题(已下线)卷05 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)易混易错4 电化学应用中的易错点河南省南阳市第八中学校2022-2023学年高三下学期第七次调研考试理科综合试卷-高中化学浙江省杭州市西湖高级中学2024届高三下学期5月模拟预测化学试题(已下线)化学-2022年高考押题预测卷02(江苏卷)
解题方法
6 . 电极电势的测定常用甘汞电极作为参比电极(部分数据如下)。
测定过程中,待测电极与甘汞电极组成原电池其工作原理如图。下列说法正确的是
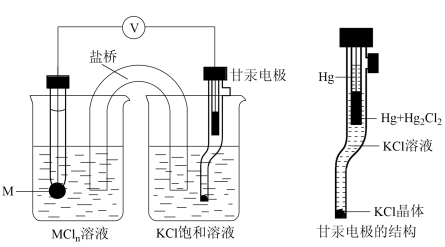
| 电极种类 | Na+/Na | Zn2+/Zn | H+/H2 | 甘汞电极 | Cu2+/Cu |
| 电极电势/V | -2.71 | -0.76 | 0.00 | 0.24 | 0.34 |

| A.盐桥中Cl-向甘汞电极移动 |
| B.若M为Cu,则电极反应式是:Cu-2e-=Cu2+ |
| C.甘汞电极电极反应式是:2Hg+2C1--2e-=Hg2Cl2 |
| D.测定过程中,甘汞电极内部KCl晶体可能增多 |
您最近一年使用:0次
2022-04-01更新
|
953次组卷
|
3卷引用:回归教材重难点03 电化学-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)
(已下线)回归教材重难点03 电化学-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)河北省承德市部分高中2023-2024学年高三上学期12月期中考试化学试题山东省潍坊市2021-2022学年高三下学期高中学科核心素养测评化学试题
名校
解题方法
7 . 全钒氧化还原液流电池是一种新型绿色的二次电池,具有容量和功率可调、大电流无损深度放电、使用寿命长、易操作和维护等优点,其放电时的工作原理如图所示,下列叙述正确的是


| A.B为该原电池的正极 |
| B.该电池放电时H+向B极室迁移,起到了导电作用 |
C.A极的电极反应式为:VO +2H++e—=VO2++H2O +2H++e—=VO2++H2O |
| D.反应过程中,每转移1mol电子,正极区n(H+)的变化量为2mol |
您最近一年使用:0次
2021-08-02更新
|
540次组卷
|
5卷引用:重庆市第八中学2020-2021学年高一下学期期中考试化学试题
重庆市第八中学2020-2021学年高一下学期期中考试化学试题(已下线)4.1 原电池-2021-2022学年高二化学课后培优练(人教版选修4)重庆市渝高中学校2021-2022学年高一下学期期中考试化学试题重庆市渝高中学2022-2023学年高一下学期期中考试化学试题福建省泉州现代中学2021-2022学年高二上学期9月月考化学试题
解题方法
8 . 中科院 HiNa公司研发的可充电的“钠离子电池”被欧盟评价为“锂电的性能、铅酸的价格”。若放电的总反应为: (Me为某元素符号),六氟磷酸钠充当电解液,其放电原理如图所示。该电池放电时,下列说法正确的是
(Me为某元素符号),六氟磷酸钠充当电解液,其放电原理如图所示。该电池放电时,下列说法正确的是
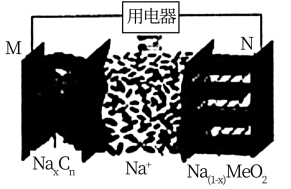
 (Me为某元素符号),六氟磷酸钠充当电解液,其放电原理如图所示。该电池放电时,下列说法正确的是
(Me为某元素符号),六氟磷酸钠充当电解液,其放电原理如图所示。该电池放电时,下列说法正确的是
| A.电流方向为N→用电器→M→电解液→N |
| B.Na+移向M电极 |
| C.正极反应为:NaMeO2- xe-=Na(1-x)MeO2 +xNa+ |
| D.转移1 mol电子时,有1mol NaxCn被还原 |
您最近一年使用:0次
9 . “低碳经济”已成为全世界科学家研究的重要课题。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)已知:①CO(g)+H2O(g) H2(g)+CO2(g) ΔH=-41 kJ·mol-1
H2(g)+CO2(g) ΔH=-41 kJ·mol-1
②C(s)+2H2(g) CH4(g) ΔH=-73 kJ·mol-1
CH4(g) ΔH=-73 kJ·mol-1
③2CO(g) C(s)+CO2(g) ΔH=-171 kJ·mol-1
C(s)+CO2(g) ΔH=-171 kJ·mol-1
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:____
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2 L密闭容器中,充入1 mol CO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:
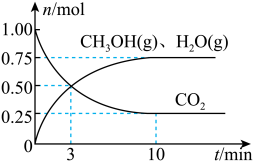
①从反应开始到平衡,氢气的平均反应速率v(H2)=________ 。
②下列措施一定不能使CO2的平衡转化率增大的是________ 。
A 在原容器中再充入1 mol CO2
B 在原容器中再充入1 mol H2
C 在原容器中充入1 mol氦气
D 使用更有效的催化剂
E 缩小容器的容积
F 将水蒸气从体系中分离
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g) H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:
H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:
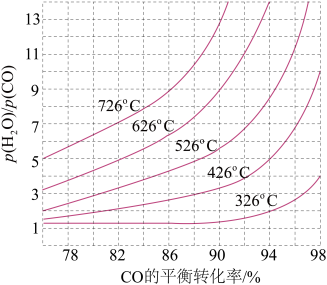
①上述反应的正反应方向是________ 反应(填“吸热”或“放热”);
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=_____ (填表达式,不必代数计算);如果提高p(H2O)/p(CO),则Kp_______ (填“变大”“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、p(H2O)/p(CO)=3~5,采用此条件的原因可能是_______
(4)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置实现了用CO2和H2O合成CH4。下列关于该电池的叙述错误的是________ 。
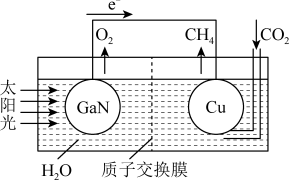
A.该装置能量转化形式仅存在将太阳能转化为电能
B.铜电极为正极,电极反应式为CO2+8e-+8H+===CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
(1)已知:①CO(g)+H2O(g)
 H2(g)+CO2(g) ΔH=-41 kJ·mol-1
H2(g)+CO2(g) ΔH=-41 kJ·mol-1②C(s)+2H2(g)
 CH4(g) ΔH=-73 kJ·mol-1
CH4(g) ΔH=-73 kJ·mol-1③2CO(g)
 C(s)+CO2(g) ΔH=-171 kJ·mol-1
C(s)+CO2(g) ΔH=-171 kJ·mol-1写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2 L密闭容器中,充入1 mol CO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:

①从反应开始到平衡,氢气的平均反应速率v(H2)=
②下列措施一定不能使CO2的平衡转化率增大的是
A 在原容器中再充入1 mol CO2
B 在原容器中再充入1 mol H2
C 在原容器中充入1 mol氦气
D 使用更有效的催化剂
E 缩小容器的容积
F 将水蒸气从体系中分离
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g)
 H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:
H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:
①上述反应的正反应方向是
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=
(4)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置实现了用CO2和H2O合成CH4。下列关于该电池的叙述错误的是

A.该装置能量转化形式仅存在将太阳能转化为电能
B.铜电极为正极,电极反应式为CO2+8e-+8H+===CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
您最近一年使用:0次
2019-06-18更新
|
1201次组卷
|
4卷引用:【市级联考】辽宁省兴城市2019届高三第九次模拟考试理科综合化学试题
【市级联考】辽宁省兴城市2019届高三第九次模拟考试理科综合化学试题四川省泸州市泸县第二中学2020届高三上学期期中考试理综化学试题(已下线)专题15 化学反应原理大题不丢分-2021年高考化学必做热点专题山东省济南二中2020届高三线上检测化学试题





