9-10高二下·北京·期末
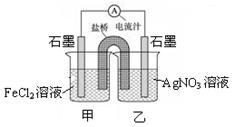
1 . 控制适合的条件,将反应Fe2++Ag+ Ag + Fe3+设计成如下图所示的原电池。下列判断错误的是
Ag + Fe3+设计成如下图所示的原电池。下列判断错误的是
 Ag + Fe3+设计成如下图所示的原电池。下列判断错误的是
Ag + Fe3+设计成如下图所示的原电池。下列判断错误的是
| A.反应开始时,电子从甲中石墨经导线流向乙中石墨 |
| B.电流计指针为零时,上述反应的正反应速率等于逆反应速率 |
| C.电流计读数为零后,在甲中加入FeCl3固体,乙中石墨电极反应为Ag - e- =Ag+ |
| D.电流计读数为零后,在乙中加入硫化钠固体,电流计指针读数仍为零 |
您最近半年使用:0次
2 . 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH + HCl = NaCl+ H2O,B.2FeCl3+ Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A._________ B.___________ 。(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是________ (填“锌”或“铜”),发生_________ 反应(填“氧化”或“还原”);
②正极的电极反应式为________________ ;
③产生这些气体共需转移电子_______________ mol。
(1)现有如下两个反应:A.NaOH + HCl = NaCl+ H2O,B.2FeCl3+ Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A.
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是
②正极的电极反应式为
③产生这些气体共需转移电子
您最近半年使用:0次
名校
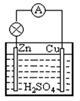
3 . 在下图所示的原电池中,正极发生的反应是( )


| A.H2-2e-=2H+ | B.Cu-2e-= Cu2+ |
| C.2H+ + 2e-= H2↑ | D.Zn-2e-=Zn2+ |
您最近半年使用:0次
9-10高一下·河北唐山·期中
解题方法
4 . 银锌电池是广泛用做各种电子仪器的电源,其放电过程可表示为Ag2O+Zn==ZnO+2Ag,此电池放电时,负极上发生反应的物质是( )
| A.Ag | B.ZnO | C.Ag2O | D.Zn |
您最近半年使用:0次
10-11高一下·吉林延边·期中
5 . 由铜、锌和稀硫酸组成的原电池中,正极是_______ ,发生_______ ,电极反应是_______ ;负极是_______ ,发生_______ ,电极反应是_______ ,电子的流动方向是从_______ 极到_______ 极;电流方向是从_______ 极到_______ 极。
您最近半年使用:0次
10-11高二上·北京·期末
6 . 原电池是把__________ 转化成__________ 的装置,其反应的实质是_____________ 。在铜锌原电池(稀硫酸为介质)中:
正极材料是____ ,其电极反应式:___________ ;
负极材料是____ ,其电极反应式:___________ 。
正极材料是
负极材料是

您最近半年使用:0次



