1 . 将如图所示的原电池分别进行如下变动,会导致电子向相反方向流动的是
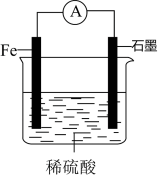
| A.将石墨更换为Zn片 | B.将稀硫酸更换为乙醇 |
C.向烧杯中加入 溶液 溶液 | D.将稀硫酸更换为NaCl溶液 |
您最近一年使用:0次
名校
解题方法
2 . 有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
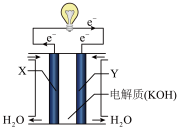
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
您最近一年使用:0次
3 . 一种在室温下可循环充放电的新型纤维 电池有望应用于可穿戴设备的储能,其工作原理为:
电池有望应用于可穿戴设备的储能,其工作原理为: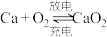 ,放电时
,放电时
 电池有望应用于可穿戴设备的储能,其工作原理为:
电池有望应用于可穿戴设备的储能,其工作原理为: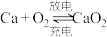 ,放电时
,放电时A. 发生还原反应 发生还原反应 | B. 在正极失电子 在正极失电子 |
| C.阳离子由正极移向负极 | D.每消耗 ,转移 ,转移 电子 电子 |
您最近一年使用:0次
4 . 某小组进行了如下两组对比实验,下列说法正确的是
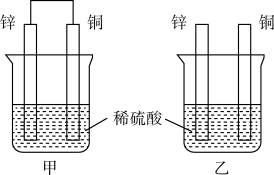

| A.甲烧杯中外电路的电子由铜流向锌 |
B.两烧杯中溶液的 均增大 均增大 |
| C.乙中产生气泡的速率比甲快 |
| D.都能够观察到锌片溶解,铜片表面产生气泡 |
您最近一年使用:0次
22-23高一下·广东深圳·期中
名校
5 . 电池是人类生产和生活中的重要能量来源。人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。
(1)知识源于实践。学习原电池知识后,某学习小组以 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
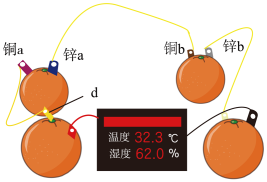
(2)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是_______(填字母)。
(3)将 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
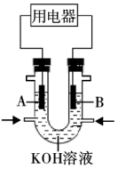
实验测得电子定向移向 电极,则
电极,则_______ (填“ ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为_______ 。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为: ,请回答下列问题:
,请回答下列问题:
①放电时,正极反应式为_______ 。
②放电时,负极附近溶液的碱性_______ 。(填“增强”或“减弱”)
(5) 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
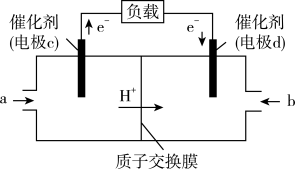
电池总反应为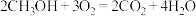 ,则
,则 电极反应式为
电极反应式为_______ ,若线路中转移 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为_______  。
。
(1)知识源于实践。学习原电池知识后,某学习小组以
 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
A.每个水果果汁中的 移向正极 移向正极 |
B.锌 、 、 发生的电极反应式为 发生的电极反应式为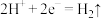 |
C.四个水果电池串联,则电极 为铜片 为铜片 |
D.铜 为电池正极,发生氧化反应 为电池正极,发生氧化反应 |
| A.锌锰电池工作一段时间后碳棒会变细 |
| B.氢氧燃料电池具有高效的特点,能量转化率可达100% |
| C.太阳能电池的主要材料是高纯度的二氧化硅 |
D.铅蓄电池负极是 ,正极是 ,正极是 |
 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
实验测得电子定向移向
 电极,则
电极,则 ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:
 ,请回答下列问题:
,请回答下列问题:①放电时,正极反应式为
②放电时,负极附近溶液的碱性
(5)
 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
电池总反应为
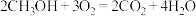 ,则
,则 电极反应式为
电极反应式为 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为 。
。
您最近一年使用:0次
名校
解题方法
6 . 为检验牺牲阳极法对钢铁防腐的效果,进行了如图所示实验,下列叙述正确的是
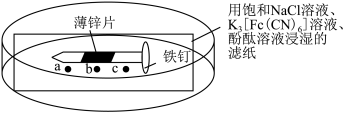

| A.一段时间后,铁钉底部a、c处滤纸上均能看到出现蓝色沉淀 |
| B.一段时间后,薄锌片底部b处能看到滤纸变红色 |
| C.薄锌片两端铁钉均为该原电池的正极 |
D.薄锌片发生的电极反应式为 |
您最近一年使用:0次
2023-04-27更新
|
875次组卷
|
5卷引用:广东省部分学校2023届高三下学期4月大联考化学试题
广东省部分学校2023届高三下学期4月大联考化学试题广东省普宁二中实验学校、普宁国贤学校2023届高三4月联考化学试题河北省石家庄市正定中学2022- 2023学年高二下学期期末考试化学试题(已下线)考点巩固卷07 化学反应与能量(3大考点45题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)考点3 电解池 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
7 . 某化学兴趣小组为了探索Zn电极在原电池中的作用,设计并进行了以下一系列实验。
已知:Zn与Al的化学性质基本相似, 。
。
回答下列问题:
(1)实验1:电极材料为Mg和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Zn。
①正极的电极反应式为___________ 。
②每转移0.1 mol电子,此时负极材料减少的质量为___________ g。
(2)实验2:电极材料为Cu和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Cu。
由实验1和实验2可知,Mg、Zn、Cu三种金属活动性由强到弱的顺序为___________ 。
(3)实验3:电极材料为石墨和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
①电池工作一段时间后,电解质溶液的pH将___________ (填“变大”、“变小”或“不变”)。
②石墨电极上发生___________ (填“氧化”或“还原”)反应。
(4)实验4:电极材料为Mg和Zn,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向Mg。
①负极的电极反应式为___________ 。
②外电路中电子的流动方向为___________ 。
(5)根据实验1、实验2、实验3、实验4,可总结出影响Zn电极在原电池中得到或失去电子的因素为___________ 。
已知:Zn与Al的化学性质基本相似,
 。
。回答下列问题:
(1)实验1:电极材料为Mg和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Zn。
①正极的电极反应式为
②每转移0.1 mol电子,此时负极材料减少的质量为
(2)实验2:电极材料为Cu和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Cu。
由实验1和实验2可知,Mg、Zn、Cu三种金属活动性由强到弱的顺序为
(3)实验3:电极材料为石墨和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
①电池工作一段时间后,电解质溶液的pH将
②石墨电极上发生
(4)实验4:电极材料为Mg和Zn,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向Mg。
①负极的电极反应式为
②外电路中电子的流动方向为
(5)根据实验1、实验2、实验3、实验4,可总结出影响Zn电极在原电池中得到或失去电子的因素为
您最近一年使用:0次
2023-04-18更新
|
350次组卷
|
7卷引用:广东省汕头市2022-2023学年高一下学期4月期中考试化学试题
名校
8 . 科学家利用水凝胶固态电解质建构了一种微型燃料电池,电池结构示意图如图。下列说法正确的是
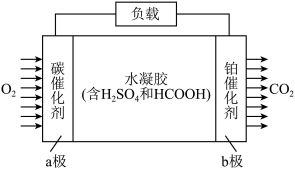

| A.a极为负极,发生还原反应 |
| B.外电路中,电子由a极流向b极 |
| C.内电路中,水凝胶中的H+向b极移动 |
| D.b极反应方程式为2HCOOH-4e-=2CO2↑+4H+ |
您最近一年使用:0次
2023-02-22更新
|
408次组卷
|
4卷引用:广东省大湾区2022-2023学年高二上学期期末联考化学试题
解题方法
9 . 无论是在环境保护领域还是在工农业生产领域,氮及其化合物一直是我国科研重点。回答下列问题:
(1)下列过程属于氮的固定过程的是_______(填选项字母)。
(2)消除汽车尾气中的氮氧化合物的原理之一为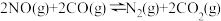 。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
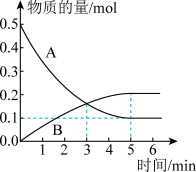
①其中B表示_______ (填“ ”或“
”或“ ”)物质的量的变化曲线。
”)物质的量的变化曲线。
②该温度下,反应开始至5min时该反应的平均反应速率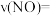
_______ 。
③3min时,反应_______ (填“达到”或“未达到”)化学平衡,6min时,正反应速率_______ (填“>”“<”或“=”)逆反应速率。
④下列情况能说明该反应达到平衡状态的是_______ (填选项字母)。
A.化学反应速率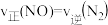
B.CO与 的物质的量之和不再发生变化
的物质的量之和不再发生变化
C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将 转化为
转化为 和
和 。该吸收过程中发生反应的离子方程式为
。该吸收过程中发生反应的离子方程式为_______ 。
(4)某固体氧化物为电解质的新型燃料电池是以液态肼(N2H4)为燃料,氧气为氧化剂构成,其原理示意图如图所示。
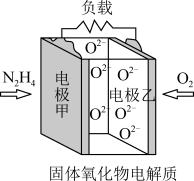
该电池的正极为_______ (填“电极甲”或“电极乙”,下同);电池工作时, 向
向_______ 移动。
(1)下列过程属于氮的固定过程的是_______(填选项字母)。
| A.工业合成氨 |
| B.工业利用氨气合成硝酸 |
| C.雷雨天中氮气与氧气生成氮氧化合物 |
| D.通过碱性试剂将气态的氮氧化合物转化为固态含氮化合物 |
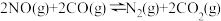 。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
①其中B表示
 ”或“
”或“ ”)物质的量的变化曲线。
”)物质的量的变化曲线。②该温度下,反应开始至5min时该反应的平均反应速率
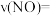
③3min时,反应
④下列情况能说明该反应达到平衡状态的是
A.化学反应速率
B.CO与
 的物质的量之和不再发生变化
的物质的量之和不再发生变化C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将
 转化为
转化为 和
和 。该吸收过程中发生反应的离子方程式为
。该吸收过程中发生反应的离子方程式为(4)某固体氧化物为电解质的新型燃料电池是以液态肼(N2H4)为燃料,氧气为氧化剂构成,其原理示意图如图所示。

该电池的正极为
 向
向
您最近一年使用:0次
名校
10 . 甲烷和乙烯是常见的两种有机化合物,在生产生活中有广泛的应用。
Ⅰ.以甲烷等碳氢化合物为燃料的新型燃料电池,成本大大低于以氢气为燃料的传统燃料电池。一种以甲烷为燃料的电池装置示意图如图。
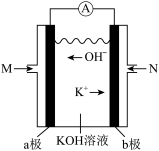
(1)N口通入的气体是_______ (填化学式)。
(2)外电路中电流的方向是由_______ 极到_______ 极(填“a”或“b”)。
(3)a极为_______ 极(填“正”或“负”),其电极方程式为_______ 。
(4)电路中每转移0.8mol电子,标准状况下消耗O2的体积是_______ L。
Ⅱ.石油裂解可得到重要的化工原料乙烯(CH2=CH2),有关乙烯的部分转化关系如图:
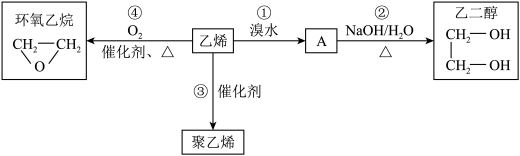
回答下列问题:
(5)写出A的结构简式:_______ 。
(6)②的反应类型为_______ 。
(7)反应③的化学方程式为_______ 。
(8)已知反应④的原子利用率为100%,其化学方程式为_______ 。
Ⅰ.以甲烷等碳氢化合物为燃料的新型燃料电池,成本大大低于以氢气为燃料的传统燃料电池。一种以甲烷为燃料的电池装置示意图如图。

(1)N口通入的气体是
(2)外电路中电流的方向是由
(3)a极为
(4)电路中每转移0.8mol电子,标准状况下消耗O2的体积是
Ⅱ.石油裂解可得到重要的化工原料乙烯(CH2=CH2),有关乙烯的部分转化关系如图:

回答下列问题:
(5)写出A的结构简式:
(6)②的反应类型为
(7)反应③的化学方程式为
(8)已知反应④的原子利用率为100%,其化学方程式为
您最近一年使用:0次



