名校
解题方法
1 . 化学能在一定条件下可转化为电能。
(1)如图所示为“锌-铜-稀硫酸”原电池,请写出锌与稀硫酸反应的离子方程式是___________ 。
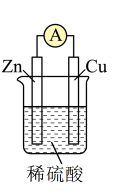
(2)装置中锌片上发生___________ (“氧化”或“还原”)反应,电极反应式是___________ ,铜片上发生反应的电极反应式是________ ,能证明化学能转化为电能的实验现象为_________ 。
(3)按照电化学装置的四个构成要素来看,Cu的作用是________ ,稀硫酸的作用是___________ 。
a.电极反应物 b.电极材料 c.离子导体 d.电子导体
(1)如图所示为“锌-铜-稀硫酸”原电池,请写出锌与稀硫酸反应的离子方程式是

(2)装置中锌片上发生
(3)按照电化学装置的四个构成要素来看,Cu的作用是
a.电极反应物 b.电极材料 c.离子导体 d.电子导体
您最近一年使用:0次
名校
解题方法
2 . 由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是
| 实验装置 | 甲 | 乙 | 丙 |
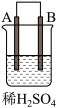 | 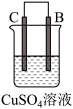 | 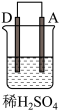 | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A.装置甲中的B金属是原电池的负极 | B.装置乙中电流的流向为B→C |
C.装置丙中溶液里的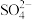 移向A 移向A | D.四种金属的活泼性顺序是D>A>B>C |
您最近一年使用:0次
3 . 回答下列问题
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,能正确表示该反应中能量变化的是图_______ (填“a”或“b”)。
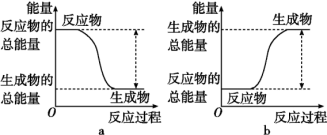
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示:
则生成1 mol H2O(g)可以放出热量_______ kJ。
(2)下列反应中,属于放热反应的是_______(填字母,下同) 。
(3)A、B、C、D 四种金属按表中装置进行实验。
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向_______ (填“A”或“B”)极。
②装置乙中正极的电极反应式为_______ 。
③四种金属活动性由强到弱的顺序是_______ 。
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,能正确表示该反应中能量变化的是图

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示:
| 化学键 | H-H | O=O | H-O |
| 键能/(kJ·mol-1) | 436 | 496 | 463 |
则生成1 mol H2O(g)可以放出热量
(2)下列反应中,属于放热反应的是_______(填字母,下同) 。
| A.盐酸与烧碱溶液反应 |
| B.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑ |
| C.氢气在氧气中燃烧生成水 |
| D.高温煅烧石灰石使其分解 |
| 装置 | 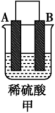 |  | 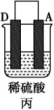 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
您最近一年使用:0次
解题方法
4 . Ⅰ.某实验小组同学进行如图1实验,以检验化学反应中的能量变化。请回答下列问题:
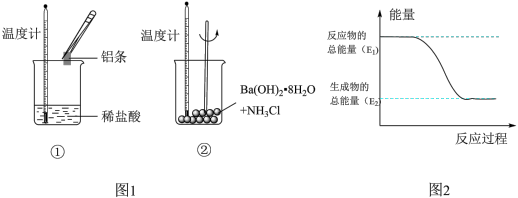
(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是________ 热反应。反应过程________ (填“①”或“②”)的能量变化可用图2表示。
Ⅱ.A、B、C、D四种金属按下表中装置进行实验。
(2)根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向________ 极(填“A”或“B”)。
②装置乙中正极的电极反应式为________ 。
③装置丙中溶液的pH________ (填“变大”“变小”或“不变”)。
④四种金属活动性由强到弱的顺序是________ 。
⑤实验后同学们经过充分讨论,观察原电池反应特点,认真符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是________ 。
A. B.
B.
C. D.
D.

(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是
Ⅱ.A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 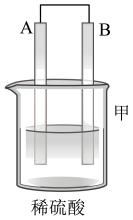 | 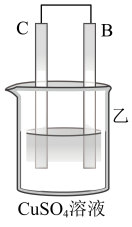 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属活动性由强到弱的顺序是
⑤实验后同学们经过充分讨论,观察原电池反应特点,认真符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
名校
解题方法
5 . 某同学以柠檬为材料自制水果电池,装置如图,下列叙述正确的是
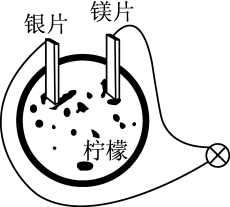

A. 由镁极区移向银极区 由镁极区移向银极区 | B.镁片上有无色气体放出 |
| C.铜片替代镁片,现象相同 | D.银片为负极 |
您最近一年使用:0次
2022-04-04更新
|
366次组卷
|
3卷引用:安徽省合肥市第八中学2021-2022学年高二上学期期末考试化学试题
6 . 下列实验操作、对应的现象及结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向苯酚浊液中滴加Na2CO3溶液,浊液变澄清 | 酸性:苯酚>碳酸 |
| B |  溶液中加入少量 溶液中加入少量 溶液,有砖红色沉淀( 溶液,有砖红色沉淀( )生成 )生成 | 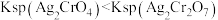 |
| C | 将镁片和铝片用导线连接后插入NaOH溶液中,镁片表面产生气泡 | 该装置构成了原电池,铝片做负极 |
| D | 向某溶液中加入稀NaOH溶液,用湿润的红色石蕊试纸检验,无明显现象 | 溶液中一定无 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 将锌片和铜片用导线连接后插入稀硫酸中,并在中间串联一个电流表,装置如图所示。
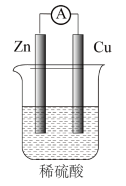
(1)该装置可以将_______ 能转化为_______ 能。
(2)装置中的负极材料是_______ 。
(3)铜片上的电极反应式是_______ ,该电极上发生了_______ (填“氧化”或“还原”)反应。
(4)稀硫酸中的SO 向
向_______ 片移动。导线中电子流向_______ 片。
(5)若将电解质溶液换成CuSO4溶液,则正极上的实验现象为_______ 。

(1)该装置可以将
(2)装置中的负极材料是
(3)铜片上的电极反应式是
(4)稀硫酸中的SO
 向
向(5)若将电解质溶液换成CuSO4溶液,则正极上的实验现象为
您最近一年使用:0次
8 . 回答下列问题
I:
(1) 的燃烧热为
的燃烧热为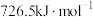 ,则表示液态甲醇燃烧热的热化学方程式为
,则表示液态甲醇燃烧热的热化学方程式为___________ 。
II.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
(2)利用反应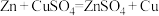 设计成原电池,该原电池的电解质溶液为
设计成原电池,该原电池的电解质溶液为___________ ,若开始时两电极质量相等,当电路中转移0.2mol电子后,两电极的质量差___________ g。
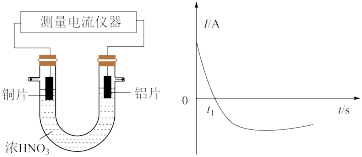
(3)某同学探究原电池原理时,认为“构成原电池的负极总是较活泼的金属材料”。该同学利用打磨过的铜片和铝片设计了下图所示的原电池装置(硝酸过量),并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转)。图中 时刻之前,正极反应式为
时刻之前,正极反应式为___________ , 时刻之后,Cu电极是
时刻之后,Cu电极是___________ (填“正极”或“负极”)。据以上现象,最终得出结论:在原电池中,构成原电池的负极不一定是较活泼的金属材料。
III.现在容积为2L的恒温密闭容器中,充入 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。
(4)下列说法正确的是___________ 。
A.使用催化剂可以增大反应速率,提高生产效率
B.反应达到平衡后,反应不再进行
C.通过改变反应条件,能改变该反应进行的限度,使 全部转化为
全部转化为
(5)达平衡时, 的转化率为
的转化率为___________ 。
I:
(1)
 的燃烧热为
的燃烧热为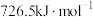 ,则表示液态甲醇燃烧热的热化学方程式为
,则表示液态甲醇燃烧热的热化学方程式为II.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:

(2)利用反应
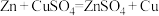 设计成原电池,该原电池的电解质溶液为
设计成原电池,该原电池的电解质溶液为(3)某同学探究原电池原理时,认为“构成原电池的负极总是较活泼的金属材料”。该同学利用打磨过的铜片和铝片设计了下图所示的原电池装置(硝酸过量),并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转)。图中
 时刻之前,正极反应式为
时刻之前,正极反应式为 时刻之后,Cu电极是
时刻之后,Cu电极是III.现在容积为2L的恒温密闭容器中,充入
 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。| 时间 | 0min | 3min | 6min | 9min | 12min |
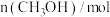 | 0 | 0.50 | 0.65 | 0.75 | 0.75 |
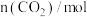 | 1 | 0.50 | 0.35 | A | 0.25 |
A.使用催化剂可以增大反应速率,提高生产效率
B.反应达到平衡后,反应不再进行
C.通过改变反应条件,能改变该反应进行的限度,使
 全部转化为
全部转化为
(5)达平衡时,
 的转化率为
的转化率为
您最近一年使用:0次
名校
解题方法
9 . 实验小组探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
【实验1】
(1)实验1中,电解质溶液为盐酸,铝条做原电池的___________ 极
【实验2】
将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为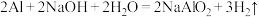 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为___________
实验2实际获得的现象如下:
(3)ⅰ中铝条表面放电的物质足溶解在溶液中的 ,则该电极反应式为
,则该电极反应式为___________
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是___________
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
(5)根据实验3和实验4可获得的正确推论是___________(填字母序号)
(6)由实验1~实验4可推知,铝片做电极材料时的原电池反应与___________ 等因素有关
【实验1】
| 装置 | 实验现象 |
 | 左侧装置电流计指针向右偏转,灯泡亮 右侧装置电流计指针向右偏转,镁条、铝条表面产生无色气泡 |
【实验2】
将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为
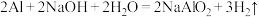 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为实验2实际获得的现象如下:
| 装置 | 实验现象 |
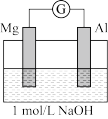 | ⅰ.电流计指针迅速向右偏转,镁条表面无气泡,铝条表面有气泡 ⅱ.电流计指针逐渐向零刻度恢复,经零刻度后继续向左偏转。镁条表面开始时无明显现象,一段时间后有少量气泡逸出,铝条表面持续有气泡逸出 |
 ,则该电极反应式为
,则该电极反应式为(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
| 编号 | 装置 | 实验现象 |
| 实验3 | 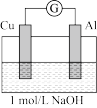 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约10分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| 实验4 | 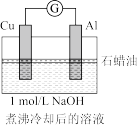 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约3分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
A.上述两装置中,开始时铜片表面得电子的物质是 |
| B.铜片表面开始产生气泡的时间长短与溶液中溶解氧的多少有关 |
C.铜片表面产生的气泡为 |
D.由“铝条表面气泡略有减少”能推测 在铜片表面得电子 在铜片表面得电子 |
您最近一年使用:0次
名校
解题方法
10 . I.由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________ 。
(2)装置乙中正极的电极反应式是________________________________________ 。
(3)四种金属活泼性由强到弱的顺序是______________________ 。
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。
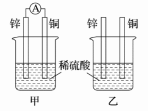
(1)下列叙述正确的是________ 。
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是________________________________________________________________________ 。
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应________________________ 。
| 装置 |  | 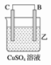 | 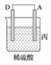 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是
(2)装置乙中正极的电极反应式是
(3)四种金属活泼性由强到弱的顺序是
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。

(1)下列叙述正确的是
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应
您最近一年使用:0次
2018-07-17更新
|
612次组卷
|
4卷引用:课后-6.1.2 化学反应与电能-人教2019必修第二册



