1 . 某科学探究小组为探究电化学原理, 设计了如图所示的装置进行探究实验。下列对实验中观察到的现象或相关结论的叙述错误的是
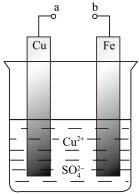

| A.a和b不连接时,铁片上有红色的铜析出 |
| B.a和b用导线连接时, 铜片为负极 |
| C.无论a和b是否连接,反应的本质相同,铁片均会被氧化,溶液中均有Fe2+生成 |
| D.a和b用导线连接时,溶液中的Cu2+应向铜电极移动且能更快地在铜电极上析出铜 |
您最近一年使用:0次
2 . 能源是现代文明的原动力,电池与我们的生活和生产密切相关。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的_____(填字母)。
(2)下图为原电池装置示意图:
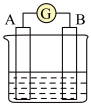
①若A为 片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:
片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:_____ ,反应过程中溶液的酸性_____ (填“增强”、“减弱”或“不变”)。一段时间后,当电池中放出2.24L(标准状况)气体时,电路中有_____ 个电子通过了导线(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
②若A为镁片,B为铝片,电解质为 溶液,则铝片为
溶液,则铝片为_____ (填“正极”或“负极”);写出该电极的电极反应式:_____ 。
(3)燃料电池是一种具有应用前景的绿色电源, 和
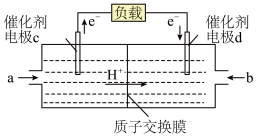
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是_____ (填“正极”或“负极”),则该燃料电池如下:
(4)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的_____(填字母)。
A. |
B.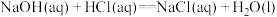 |
C.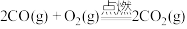 |
D.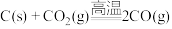 |

①若A为
 片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:
片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式: 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②若A为镁片,B为铝片,电解质为
 溶液,则铝片为
溶液,则铝片为(3)燃料电池是一种具有应用前景的绿色电源,
 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是
(4)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
A.将铁片置于 溶液中 溶液中 | 铁片上有亮红色物质析出 |
| B.将铁丝和铜丝分别在氯气燃烧 | 产物分别为 和 和 |
| C.将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| D.将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连 | 铁片溶解,铜片上有气泡产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组欲探究a,b,c,d四种金属的活动性大小顺序,利用实验室现有材料和试剂进行实验,组装了如图所示的装置(电流表指针偏向正极,电解质溶液足量)。请回答下列问题:
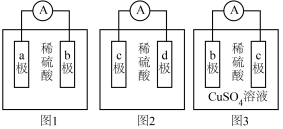
(1)观察到图1装置中的电流表指针偏向b极,说明a极为______ (填“正极”或“负极”),b极上发生的电极反应为______ 。
(2)观察到图2装置中的c极上有气泡生成,可观察到d极上的现象为______ 。
(3)图3装置中的电流表指针偏向c极,若b极为Fe电极,则b极上发生的电极反应为______ ,当该电路中转移0.4mole-时,______ (填“b”或“c”)极质量增重______ g。
(4)通过以上实验装置______ (填“能”或“不能”)比较出四种金属的活动性大小顺序,理由是______ 。

(1)观察到图1装置中的电流表指针偏向b极,说明a极为
(2)观察到图2装置中的c极上有气泡生成,可观察到d极上的现象为
(3)图3装置中的电流表指针偏向c极,若b极为Fe电极,则b极上发生的电极反应为
(4)通过以上实验装置
您最近一年使用:0次
解题方法
4 . 为了探究原电池的工作原理,某研究性学习小组进行了如下实验。
(1)分别按图1中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。
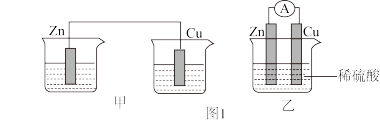
①以下叙述中正确的是___________ (填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向Cu→Zn
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是___________ 。
③在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极___________ (填实验现象),其对应的电极反应式为___________ 。
(2)某氢氧燃料电池装置如图2所示,a、b均为惰性电极。
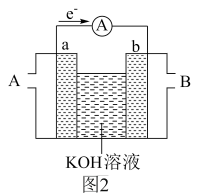
①电池工作时,空气从___________ (填“A”或“B”)口通入。
②正极上的电极反应式为___________
(3)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是________。
(1)分别按图1中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。

①以下叙述中正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向Cu→Zn
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
③在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极
(2)某氢氧燃料电池装置如图2所示,a、b均为惰性电极。

①电池工作时,空气从
②正极上的电极反应式为
(3)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是________。
| A.KOH+HCl=KCl+H2O | B.Cu+2Fe3+=2Fe2++Cu2+ |
| C.Na2CO3+2HCl=2NaCl+H2O+CO2↑ | D.Mg3N2+6H2O=3Mg(OH)2+2NH3↑ |
您最近一年使用:0次
名校
解题方法
5 . 化学反应与能量变化对人类生产、生活有重要的意义。回答下列问题:
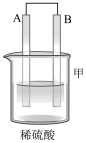
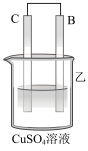
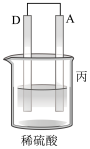
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
①装置甲中负极为___________ (填“A”或“B”)。
②装置乙中正极的电极反应式为___________ 。
③装置丙中溶液的pH___________ (填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是___________ 。
(2)北京冬奥会基本实现100%绿电供应和碳中和,利用CO2和H2在光催化酶作用下可以高效合成甲醇(CH3OH)。
①写出甲醇燃烧的化学方程式:___________ 。
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:
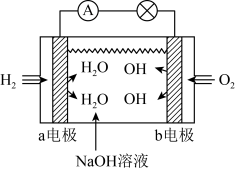
a电极是___________ 极,此时b电极发生反应的电极反应式是___________ , 向
向___________ (填“a”或“b”)电极移动。
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
| 装置 | 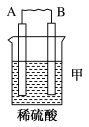 | 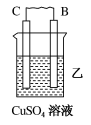 | 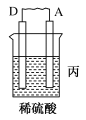 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(2)北京冬奥会基本实现100%绿电供应和碳中和,利用CO2和H2在光催化酶作用下可以高效合成甲醇(CH3OH)。
①写出甲醇燃烧的化学方程式:
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:

a电极是
 向
向
您最近一年使用:0次
名校
解题方法
6 . 化学能在一定条件下可转化为电能。
(1)如图所示为“锌-铜-稀硫酸”原电池,请写出锌与稀硫酸反应的离子方程式是___________ 。
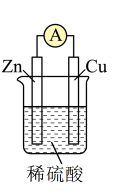
(2)装置中锌片上发生___________ (“氧化”或“还原”)反应,电极反应式是___________ ,铜片上发生反应的电极反应式是________ ,能证明化学能转化为电能的实验现象为_________ 。
(3)按照电化学装置的四个构成要素来看,Cu的作用是________ ,稀硫酸的作用是___________ 。
a.电极反应物 b.电极材料 c.离子导体 d.电子导体
(1)如图所示为“锌-铜-稀硫酸”原电池,请写出锌与稀硫酸反应的离子方程式是

(2)装置中锌片上发生
(3)按照电化学装置的四个构成要素来看,Cu的作用是
a.电极反应物 b.电极材料 c.离子导体 d.电子导体
您最近一年使用:0次
名校
解题方法
7 . 某科学探究小组为探究电化学原理,设计了如图所示的装置进行探究实验。下列对实验中观察到的现象或相关结论的叙述不正确的是
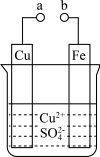
| A.a和b不连接时,铁片上有红色的铜析出,该装置不能形成原电池 |
| B.a和b用导线连接时,铜片为正极 |
C.无论a和b是否连接,反应的本质相同,铁片均会被氧化,溶液中均有 生成 生成 |
D.a和b用导线连接时,溶液中的 应向铁电极移动且能更快地析出铜 应向铁电极移动且能更快地析出铜 |
您最近一年使用:0次
2023-04-18更新
|
255次组卷
|
2卷引用:湖北省武汉市重点中学5G联合体2022-2023学年高一下学期期中考试化学试题
名校
解题方法
8 . 由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
| 装置 | 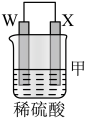 | 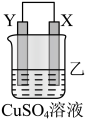 | 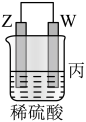 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A.装置甲中W作原电池负极 |
| B.装置乙中Y电极上的反应式为Cu2++2e-=Cu |
| C.装置丙溶液中电子由Z流向W |
| D.四种金属的活动性强弱顺序为Z>W>X>Y |
您最近一年使用:0次
2023-04-11更新
|
749次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题
名校
解题方法
9 . 某同学设计如图所示装置研究原电池原理。
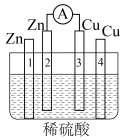
(1)正极发生的电极反应式为____________________ 。
(2)Cu(3)与Cu (4)上现象有何不同?_________ 。
(3)若保持正负极发生的反应不变,正极材料还可以是_________ (填序号)。
①碳棒②铝片③银棒
(4)溶液中 的移动方向是
的移动方向是_________ (填序号)(①从左往右②从右往左③不动)
(5)若将稀硫酸换为稀硝酸,Cu (4)上反应的离子方程式为____________________ 。

(1)正极发生的电极反应式为
(2)Cu(3)与Cu (4)上现象有何不同?
(3)若保持正负极发生的反应不变,正极材料还可以是
①碳棒②铝片③银棒
(4)溶液中
 的移动方向是
的移动方向是(5)若将稀硫酸换为稀硝酸,Cu (4)上反应的离子方程式为
您最近一年使用:0次
名校
解题方法
10 . 化学反应与能量变化对人类生产、生活有重要的意义。回答下列问题:
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
①装置甲中负极为_______ (填“A”或“B”)。
②装置乙中正极的电极反应式为_______ 。
③装置丙中溶液的pH_______ (填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是_______ 。
(2)北京冬奥会基本实现100%绿电供应和碳中和,利用 和
和 在光催化酶作用下可以高效合成甲醇(
在光催化酶作用下可以高效合成甲醇( )。
)。
①写出甲醇燃烧的化学方程式:_______ ,
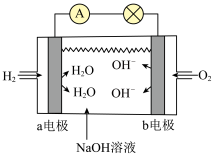
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:
a电极是_______ 极,此时b电极发生反应的电极反应式是_______ 。
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(2)北京冬奥会基本实现100%绿电供应和碳中和,利用
 和
和 在光催化酶作用下可以高效合成甲醇(
在光催化酶作用下可以高效合成甲醇( )。
)。①写出甲醇燃烧的化学方程式:
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:
a电极是

您最近一年使用:0次
2023-04-16更新
|
246次组卷
|
3卷引用:湖北省宜昌市协作体2022-2023学年高一下学期期中考试化学试题