2020高三·全国·专题练习
名校
解题方法
1 . 普通锌锰干电池的简图如图所示,它是用锌皮制成的锌筒作为电极,中央插一根石墨棒,石墨棒顶端加一铜帽。在石墨棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液。该电池工作时的总反应为Zn+2NH +2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
+2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
 +2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
+2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是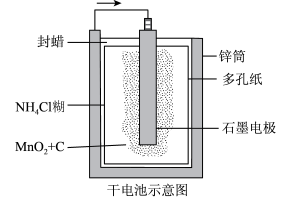
| A.当该电池电压逐渐下降后,利用电解原理能重新充电复原 |
B.电池负极反应为2MnO2+2NH +2e-=Mn2O3+2NH3+H2O +2e-=Mn2O3+2NH3+H2O |
| C.原电池工作时,电子从负极通过外电路流向正极 |
| D.外电路中每通过0.1 mol 电子,锌的质量理论上减少6.5 g |
您最近一年使用:0次
2023-05-13更新
|
272次组卷
|
10卷引用:专题6.2 原电池 化学电源(讲)——2020年高考化学一轮复习讲练测
(已下线)专题6.2 原电池 化学电源(讲)——2020年高考化学一轮复习讲练测(已下线)第四章 化学反应与电能(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)河南省洛阳市宜阳县第一高级中学2022-2023学年高二上学期第五次能力达标测试化学试题第一节 原电池 第2课时 化学电源辽宁省辽阳市第二高级中学2022-2023学年高二上学期12月月考化学试题四川省眉山市仁寿县2022-2023学年高一下学期5月期中联考化学试题新疆塔城地区塔城市2022-2023学年高二上学期11月期中考试化学试题陕西省渭南市白水中学2022-2023学年高二上学期12月月考化学试题河南省焦作市第十一中学2023-2024学年高二上学期12月份月考 化学试卷6.1.2 化学反应与电能 随堂练习
名校
解题方法
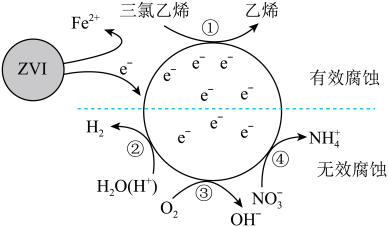
2 . 利用小粒径零价铁(ZVI)的电化学腐蚀处理三氯乙烯,进行水体修复的过程如图。H+、O2、NO 等共存物的存在会影响水体修复效果,定义单位时间内ZVI释放电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量ne。下列说法错误的是( )
等共存物的存在会影响水体修复效果,定义单位时间内ZVI释放电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量ne。下列说法错误的是( )
 等共存物的存在会影响水体修复效果,定义单位时间内ZVI释放电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量ne。下列说法错误的是( )
等共存物的存在会影响水体修复效果,定义单位时间内ZVI释放电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量ne。下列说法错误的是( )
| A.反应①②③④均在正极发生 |
| B.单位时间内,三氯乙烯脱去amolCl时ne=amol |
C.④的电极反应式为NO +10H++8e-=NH +10H++8e-=NH +3H2O +3H2O |
| D.增大单位体积水体中小微粒ZVI的投入量,可使nt增大 |
您最近一年使用:0次
2020-12-08更新
|
2221次组卷
|
34卷引用:河南省洛阳市2020届高三上学期期末模拟考试化学试题
河南省洛阳市2020届高三上学期期末模拟考试化学试题山东省2020年普通高中学业水平等级考试模拟试题【省级联考】山东省2020届新高考模拟统考化学试题山东省菏泽市菏泽第一中学2020届高三下学期在线考试化学试题陕西省西安市周至县第五中学2020届高三第二次模拟考试化学试题湖南省怀化市中方一中2020届高三下学期第一次模拟测试理综化学试题黑龙江省哈尔滨市第三中学2020届高三下学期5月第一次模拟考试(全国II卷)理综化学试题北京市海淀区育英学校2020届高三三模化学试题北京市海淀区中央民族大学附属中学2020届高三考前热身化学试题北京市清华大学附属中学2020届高三三模试卷化学试题(已下线)第八单元 化学反应与能量测试题-2021年高考化学一轮复习名师精讲练鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1章 综合检测鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 章末综合检测卷人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 章末综合检测卷(已下线)第21讲 电解池 金属的电化学腐蚀与防护 (精练)-2021年高考化学一轮复习讲练测(已下线)【南昌新东方】9.2020年11月江西南昌三中高三上学期期中化学湖北省武汉市蔡甸区汉阳一中2020-2021学年高二上学期9月联考化学试题吉林省白城市洮南一中2021届高三上学期第三次月考化学试题福建省安溪一中、养正中学、惠安一中、泉州实验中学2020-2021学年高二上学期期中联考化学试题江苏省徐州一中、兴化中学2021届高三上学期第二次适应性考试化学试题安徽省淮北市树人高级中学2020-2021学年高二上学期第四阶段考试化学试题福建省三明市2021届高三上学期期末质量检测化学试题江苏省盐城市阜宁中学2020-2021学年高二上学期期末考试化学试题广东省广州市三校联考2020-2021学年高二上学期期末考试化学试题广东省汕头市金山中学2021届高三下学期学科素养测试化学试题(已下线)2021年高考化学押题预测卷(湖北卷)03(含考试版、答题卡、参考答案、全解全析)(已下线)第17讲 电解池 金属的腐蚀与防护(练)— 2022年高考化学一轮复习讲练测(新教材新高考)山东省德州市2022届高三12月联合质量测评化学试题重庆市西南大学附中2021-2022学年高一下学期期中考试化学试题江苏省无锡市天一中学2021-2022学年高二下学期期中考试化学(强化班)试题第四章化学反应与电能甘肃省天水市清水县2022-2023学年高二上学期12月期中考试化学试题河南省南阳市2023-2024学年高二上学期期中考试化学试题 福建省厦门市集美中学2023-2024学年高二上学期10月第一次月考化学试题
3 . 原电池是将化学能转化为电能的装置,某兴趣小组利用数据采集器和传感器等仪器对原电池进行实验探究。
I.能量变化探究
将上表的现象和结论补充完整
(1)_____________
(2)__________ 、__________
II.原电池电压影响因素的测定
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。
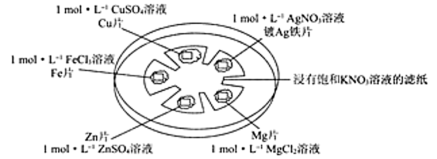
(3)准确配制一定物质的量浓度的溶液时,操作X应在__________ (填字母)之间。
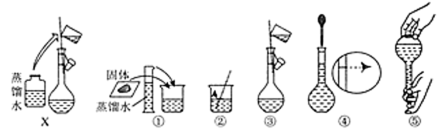
A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为_________________ 。
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表__________ (填“正”或“负”)极,预测表中Ag和Zn相连接时,测得电压的数值a可能的范围为____________ ;Fe和Mg相连接时,Z极的电极反应式为__________ ,Y极的电极反应式为____________ 。
I.能量变化探究
| 实验操作 | 数据及图象 | 现象与结论 |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,向其中加入1g镁粉 | 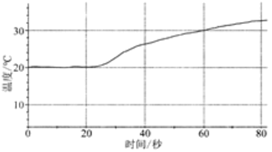 | (1)反应过程中,化学能直接转化为 能; |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,平行插入铜片和镁片,与电流传感器形成闭合回路 | 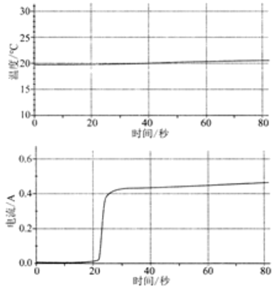 | (2)体系温度变化很小,原因是 ;反应过程中,镁片和铜片的质量变化分别为: ; |
(1)
(2)
II.原电池电压影响因素的测定
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。

(3)准确配制一定物质的量浓度的溶液时,操作X应在

A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表
| Y极 | Z极 | 测得电压/V |
| Ag | Fe | 1.009 |
| Ag | Zn | a |
| Ag | Mg | 2.114 |
| Fe | Zn | 0.473 |
| Fe | Mg | 1.111 |
| Zn | Mg | 0.636 |
您最近一年使用:0次
解题方法
4 . 如图所示的装置中。M为活动性顺序表中位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,不正确的是( )
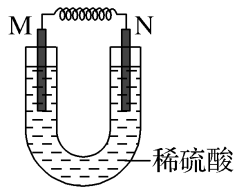

| A.是化学能转变为电能的装置 |
| B.N上有气体放出 |
| C.M为正极,N为负极 |
| D.导线中有电流通过,电流方向是经导线由N到M |
您最近一年使用:0次
2020-08-18更新
|
117次组卷
|
3卷引用:河南省洛阳市2019-2020学年高一下学期期中化学试卷
9-10高一下·河北衡水·期中
名校
解题方法
5 . 人造地球卫星上使用的一种高能电池(银锌蓄电池),其电池的电极反应式为:Zn+2OH--2e- =ZnO+H2O,Ag2O+H2O+2e- =2Ag+2OH-。据此判断氧化银是
| A.正极,被还原 | B.负极,被氧化 |
| C.正极,被氧化 | D.负极,被还原 |
您最近一年使用:0次
2020-06-18更新
|
777次组卷
|
81卷引用:2009—2010学年河北冀州中学高一下学期期中考试化学卷
(已下线)2009—2010学年河北冀州中学高一下学期期中考试化学卷(已下线)09-10年深圳高中高一下学期期末测试化学卷(已下线)2010年黑龙江省牡丹江一中高一下学期期末测试化学(已下线)2010年内蒙古通辽一中高一下学期期末考试化学试题(已下线)2010-2011学年广西北海市合浦县教研室高二上学期期末考试化学试卷(已下线)2010—2011学年辽宁省大连协作体高一4月月考化学试卷(已下线)2010—2011学年安徽蚌埠二中第二学期高一期中考试化学试卷(已下线)2010-2011学年甘肃省张掖中学高一下学期期中考试化学试卷(已下线)2010-2011学年河南省许昌市高一下学期四校期中联考化学试卷(已下线)2011-2012学年山东省济南外国语学校高二上学期期中考试化学(文)试卷(已下线)2011-2012学年山东临清三中高二上学期学分认定测试化学试卷(已下线)2011-2012学年贵州省湄潭中学高二上学期期末考试化学试卷(已下线)2011-2012学年浙江省衢州一中高一下学期期中检测化学试卷(已下线)2011-2012学年贵州省湄潭中学高一下学期期中考试化学试卷 (已下线)2011-2012年江苏南通小海中学高一下学期期中考试化学试卷(已下线)2011-2012年湖南湘潭等四县一中高一下学期期中联考化学试卷(已下线)2011-2012学年广东省罗定市高一下学期期中质检理综化学试卷(已下线)2011-2012学年陕西省岐山县高一下学期期中考试化学试卷(已下线)2011-2012学年陕西省西安一中高一下学期期末考试化学试卷(已下线)2012-2013学年吉林省实验中学高二上学期期末考试化学试卷(已下线)2013-2014湖南省衡南县高二下学期期末考试化学试卷2014-2015浙江省杭州地区七校高一下学期期中联考化学试卷2014-2015陕西省西安市一中高一下学期期中化学试卷2014-2015学年安徽省涡阳四中高一下第二次质检化学试卷2015-2016学年黑龙江大庆铁人中学高二上9月考化学试卷2015-2016学年山西省大同一中高二上期末考试化学试卷2015-2016学年陕西省黄陵中学高一下学期期中考试化学试卷2015-2016学年福建省清流一中高一实验班下第三段测化学试卷2015-2016学年河北省沧州市黄骅中学高一下期中化学试卷吉林省东北师范大学附属中学净月实验学校2016-2017学年高一下学期期中考试化学试题吉林省吉林油田实验中学2016-2017学年高一下学期期中考试化学试题湖南省2016-2017学年高二普通高中学业水平考试模拟二化学试题福建省长泰县第一中学2017-2018学年高二上学期期中考试(理)化学试题湖北省沙市中学2017-2018学年高一下学期期中考试化学试题【全国百强校】黑龙江省双鸭山市第一中学2017-2018学年高一下学期第二次6月月考化学试题宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题河北省黄骅中学2018-2019学年高二上学期第二次月考化学试题浙江省慈溪市三山高级中学2018-2019学年高一下学期第一次月考化学试题【校级联考】江苏省常州“教学研究合作联盟”2018-2019学年高二下学期期中考试化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高一下学期期中考试化学试题【校级联考】吉林省长春市九台区师范高中、实验高中2018-2019学年高一下学期期中考试化学试题广东省江门市第二中学2018-2019学年高一5月月考化学试题黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高一下学期期中考试化学试题(宾县用卷)新疆兵团八师一四三团一中2018-2019学年高一下学期期中考试化学试题黑龙江省龙东南联合体2018-2019学年高一下学期期末考试化学试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(学考)试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(选考)试题2020届高三化学化学二轮复习——新型电池基础练习【精编24题】河南省新乡市卫辉高中2019-2020学年高一下学期第一次调研考试化学试题甘肃省甘南藏族自治州合作第一中学2018-2019学年高一下学期期中考试化学试题湖南省常德市桃花源一中2019-2020学年高一下学期期中考试化学试题黑龙江省鸡西市鸡东县第二中学2019-2020学年高一下学期线上考试化学试题四川省乐山市第四中学2019-2020学年高一下学期期中考试化学试题辽宁省营口市第二高级中学2018-2019学年高一下学期第一次月考化学试题湖北省宜昌市长阳县第一高级中学2019-2020高一下学期期中考试化学试题浙江省金华市曙光学校2019-2020学年高一下学期第一次月考化学试题四川省遂宁市船山区第二中学校2019-2020学年高一下学期期中考试化学试题江苏省泰州中学2019-2020学年高一下学期期中考试化学试题安徽省桐城市第八中学2019-2020学年高一下学期期中考试化学试题(已下线)江苏省如皋市2019-2020学年高二下学期第二次月考化学试题贵州省兴仁市凤凰中学2019-2020学年高一下学期第一次月考化学试题广东省东莞市东华中学2019-2020学年高一下学期期末模拟化学试题安徽省安庆市第一中学2019-2020学年高一下学期月考化学试题甘肃省武威市第八中学2019-2020学年高一下学期期末考试化学试题湖南省衡阳市衡东县欧阳遇实验中学2019-2020学年高一上学期期末考试化学试题四川省雅安市2019-2020学年高二下学期期末考试化学试题河南省漯河市临颍县南街高级中学2020-2021学年高一10月质量检测化学试题重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题吉林省吉林市江城中学2020-2021学年高二上学期期中考试化学(理)试题河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题北京市第四十三中学2020-2021学年高一下学期第一次月考化学试题北京市丰台第八中学2020-2021学年高一下学期期中考试化学试题广西钦州市第四中学2020-2021学年高一下学期4月月考化学试题2甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(文)试题甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(理)试题陕西省宝鸡市金台区2021-2022学年高一下学期期中考试化学试题黑龙江省伊春市伊美区第二中学2021-2022学年高一下学期期中考试(会考)化学试题云南昆明市昆明行知中学2021-2022学年高二上学期期中考试化学试题北京师范大学附属中学2022-2023学年高一下学期期中考试化学试题海南省海口市长流中学2022-2023学年高一下学期期中考试化学试题A卷四川省雅安市名山区第三中学2023-2024学年高二12月月考化学试题
名校
解题方法
6 . 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,适合进行现场酒精检测,下列说法不正确的是
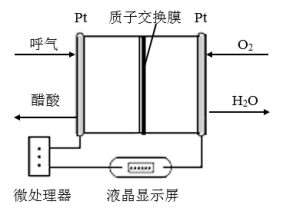

| A.电流由O2所在的铂电极经外电路流向另一电极 |
| B.该电池的正极反应式为:O2 + 4e- + 4H+=2H2O |
| C.该电池的负极反应式为:CH3CH2OH + 3H2O-12e-=2CO2↑ + 12H+ |
| D.微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
您最近一年使用:0次
2020-06-11更新
|
981次组卷
|
5卷引用:天津市红桥区2020届高三第二次模拟考试化学试题
名校
解题方法
7 . 关于下列装置说法正确的是( )
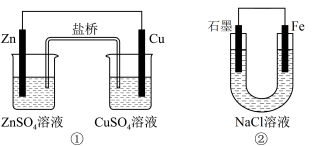

| A.装置②中电子由Fe流向石墨,然后再经溶液流向Fe |
| B.装置①中,Zn为负极,发生还原反应 |
| C.装置②中的Fe发生析氢腐蚀 |
| D.装置①中,盐桥中的K+移向CuSO4溶液 |
您最近一年使用:0次
2020-02-12更新
|
244次组卷
|
2卷引用:河南省洛阳市2019-2020学年高二上学期期末考试化学试题
8 . 我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。下列说法不正确 的是
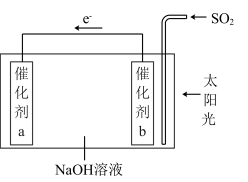

| A.该装置可将太阳能转化为化学能 |
| B.催化剂a表面发生还原反应,产生H2 |
| C.催化剂b附近的溶液pH增大 |
| D.吸收1 mol SO2,理论上能产生1 mol H2 |
您最近一年使用:0次
2019-04-04更新
|
1271次组卷
|
7卷引用:【区级联考】北京市朝阳区2019届高三下学期一模考试化学试题
解题方法
9 . Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是________ 。电池工作时,电子流向________ (填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是________ 。欲除去Cu2+,最好选用下列试剂中的________ (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是________ 。若电解电路中通过2 mol电子,MnO2的理论产量为________ 。
(4)用间接电化学法除去NO的过程,如下图所示:
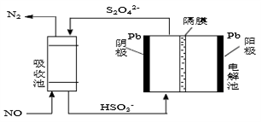
已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:_____________ 。用离子方程式表示吸收池中除去NO的原理:____________________________________ 。
(1)该电池的负极材料是
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是
(4)用间接电化学法除去NO的过程,如下图所示:

已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:
您最近一年使用:0次
2017-12-17更新
|
362次组卷
|
2卷引用:河南省洛阳名校2017-2018学年高二上学期第二次联考化学试题
名校
解题方法
10 . 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:___________ 。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置______ (填“能”或“不能”)
形成原电池,若不能,请说明理由;若能,请指出正、负极材料:__________ 。当反应中收集到标准状况下224mL气体时,消耗的电极质量为________ g。
(3)燃料电池工作原理是将燃料和氧化剂(如O2)反应产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入____ 极(填a或b,下同),电子从____ 极流出,电解质溶液中OH-向____ 极移动。
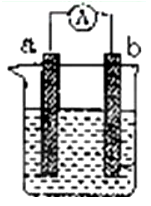
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置
形成原电池,若不能,请说明理由;若能,请指出正、负极材料:
(3)燃料电池工作原理是将燃料和氧化剂(如O2)反应产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入
您最近一年使用:0次



