名校
解题方法
1 . 由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
| 装置 | 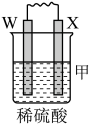 | 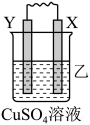 | 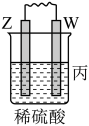 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A.装置甲中X作原电池正极 |
| B.装置乙中Y电极上的反应式为Cu2++2e−=Cu |
| C.装置丙中溶液的c(H+)不变 |
| D.四种金属的活动性强弱顺序为Z>W>X>Y |
您最近一年使用:0次
2020-06-16更新
|
470次组卷
|
2卷引用:辽宁省沈阳市郊联体2020-2021学年高一下学期期末考试化学试题
2 . (1)下列装置属于原电池的是___________ ;
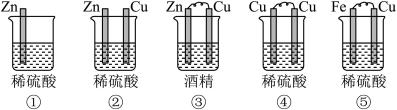
(2)在选出的原电池中,______ 是负极,发生______ (氧化、还原) 反应 ,______ 是正极 ,该极的现象___________________________ ;
(3)在该原电池的内电路中,硫酸根离子移向_________ (正、负)极。
(4)此原电池反应的化学方程式为___________________________ 。

(2)在选出的原电池中,
(3)在该原电池的内电路中,硫酸根离子移向
(4)此原电池反应的化学方程式为
您最近一年使用:0次
名校
解题方法
3 . 如下图设计的串联电池装置,R为变阻器,以调节电路电流。
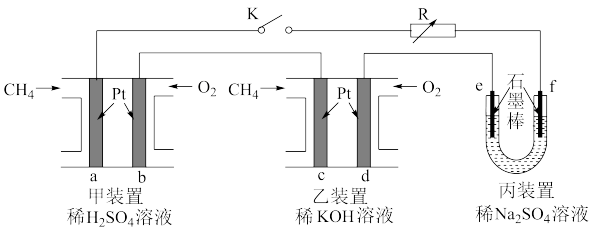
(1)写出b、c电极的电极反应式:b______________ ,c_______________ ;
(2)写出f电极的电极反应式____________________ ,向此电极区域滴入酚酞的现象为:_____________ ;该电极区域水的电离平衡被____________ (填“促进”、“抑制”或“无影响”)。
(3)闭合K一段时间后,丙装置的电解质溶液pH__________ (填“变大”、“变小”或“不变”),原因是______________ 。
(4)电解一段时间后丙装置析出芒硝(Na2SO4·10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入______ g H2O就可以将析出的沉淀溶解并恢复到原有浓度。

(1)写出b、c电极的电极反应式:b
(2)写出f电极的电极反应式
(3)闭合K一段时间后,丙装置的电解质溶液pH
(4)电解一段时间后丙装置析出芒硝(Na2SO4·10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入
您最近一年使用:0次
2018-10-19更新
|
487次组卷
|
5卷引用:选择性必修1专题1第二单元 突破2 电极反应式的书写
2014高三·全国·专题练习
名校
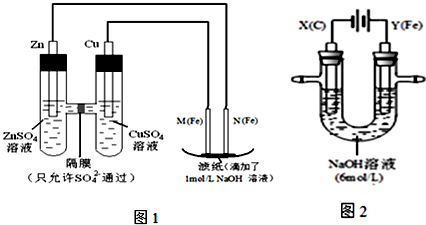
4 . 某课外小组分别用下图所示装置对原电池和电解原理进行实验探究.
请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是______ (填字母序号).
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为_____________ .
(3)实验过程中,SO42-______ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有______________ .
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH______ (填“增大”、“减小”或“不变”).
(5)电解过程中,Y极发生的电极反应为_____________ 和4OH- - 4e-= 2H2O + O2↑
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少______ g.
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为__________ .

请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为
(3)实验过程中,SO42-
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为
您最近一年使用:0次
2017-06-17更新
|
606次组卷
|
7卷引用:辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题
辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题(已下线)2014届高考化学二轮专题复习 电化学练习卷(已下线)2014高考名师推荐化学电解规律及电化学计算北京市2017届高三高考押题卷化学试题河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题河南省南阳市第一中学2016-2017学年高二下学期第三次月考化学试题2020届高考化学二轮复习大题精准训练 ——原电池、电解池填空题
名校
5 .  具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备
具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备 ,采用的装置如图B所示,以
,采用的装置如图B所示,以 辅助的
辅助的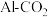 电池(如图A)为电源进行电解。
电池(如图A)为电源进行电解。
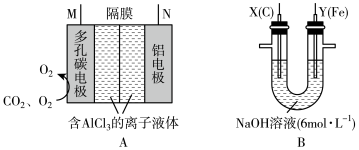
(1) 的电子式为
的电子式为___________ 。
(2)图A中正极反应式为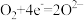 、
、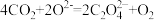 ,则该电池的总反应方程式为
,则该电池的总反应方程式为___________ 。
(3)图A中N极名称是___________ (填“正极”或“负极”),M极与图B___________ (填“X”或“Y”)极相连。
(4)电解过程中,图BX极区溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)图B中两极均有气体产生,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极质量减小___________ g。
 具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备
具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备 ,采用的装置如图B所示,以
,采用的装置如图B所示,以 辅助的
辅助的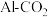 电池(如图A)为电源进行电解。
电池(如图A)为电源进行电解。
(1)
 的电子式为
的电子式为(2)图A中正极反应式为
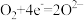 、
、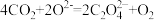 ,则该电池的总反应方程式为
,则该电池的总反应方程式为(3)图A中N极名称是
(4)电解过程中,图BX极区溶液的pH
(5)图B中两极均有气体产生,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极质量减小
您最近一年使用:0次
名校
解题方法
6 . 一种将燃料电池与电解池组合制备 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
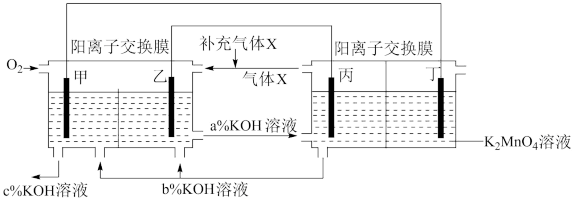
 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
| A.甲为正极,丙为阴极 |
B.丁极的电极反应式为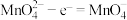 |
C.KOH溶液的质量分数: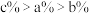 |
D.标准状况下,乙电极上每消耗 气体时,理论上有 气体时,理论上有 移入阴极区 移入阴极区 |
您最近一年使用:0次
2022-05-29更新
|
669次组卷
|
7卷引用:课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省株洲市第一中学2022届高三下学期第三次模拟考试化学试题四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题河南省南阳市第一中学校2022-2023学年高三上学期12月月考化学试题
7 . 合成氨对人类生存具有重大意义:
(1)传统工业合成法:反应为N2(g)+3H2(g) 2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
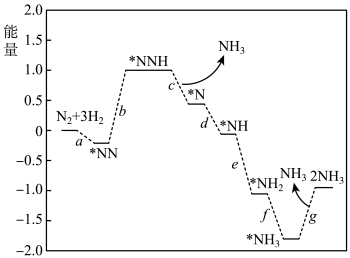
①N2的电子式是___ 。
②写出步骤b的化学方程式___ 。
③由图象可知合成氨反应的∆H__ 0(填“>”、“<”或“=”)。
④工业生产中,除了温度采用400℃—500℃外,促进该反应正向进行的措施是(至少两点)___ 。
(2)电化学制备方法:目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①氢化酶区域发生反应的离子方程式是___ 。
②溶液中H+的移动方向是___ (填“向左”或“向右”)。
③下列说法正确的是___ 。
A.该装置可以实现电能转化为化学能
B.电极a是燃料电池的负极
C.该方法相较于传统工业合成方法具有条件温和,对环境友好等优点
(1)传统工业合成法:反应为N2(g)+3H2(g)
 2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
①N2的电子式是
②写出步骤b的化学方程式
③由图象可知合成氨反应的∆H
④工业生产中,除了温度采用400℃—500℃外,促进该反应正向进行的措施是(至少两点)
(2)电化学制备方法:目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①氢化酶区域发生反应的离子方程式是
②溶液中H+的移动方向是
③下列说法正确的是
A.该装置可以实现电能转化为化学能
B.电极a是燃料电池的负极
C.该方法相较于传统工业合成方法具有条件温和,对环境友好等优点
您最近一年使用:0次
名校
8 . 回答下列问题:
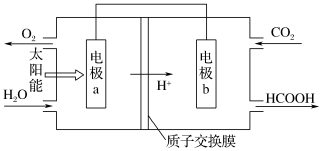
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作___________ 极,发生的电极反应式为___________ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为___________ 极,Y电极反应式为___________ 。
②Y极生成1 mol Cl2时,___________ mol Li+移向X极。
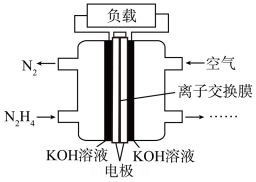
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH溶液作电解质溶液。负极反应式为___________ ,正极反应式为___________ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为
②Y极生成1 mol Cl2时,
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH溶液作电解质溶液。负极反应式为

您最近一年使用:0次
9 . (一)己二腈(NC(CH2)4CN)是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈(CH2=CHCN),再用丙烯腈电合成己二腈,总反应式为CH2=CHCN+2H2O=2NC(CH2)4CN+O2↑。(已知丙烯腈难溶于水,易溶于有机溶剂)。如图为模拟工业电合成己二腈装置图,回答下列问题:

(1)碳棒电极为__ 极(填“阴”或“阳”),其电极反应方程式为__ 。
(2)在甲室中加入异丙醇的作用是__ 。
(3)在甲室中得到产品己二腈54g时,乙室中质量减轻___ g。
(二)2019年诺贝尔化学奖颁给了三个人,其中一个是Goodenough(古迪纳夫),他因为发明可充电锂离子电池而闻名于世,他建造了锂离子电池的神经系统,被业界称为“锂电池之父”。其中一款是钴酸锂(LiCoO2)电池,它的工作原理如图所示,图中电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xCoO2 C6+LiCoO2。
C6+LiCoO2。
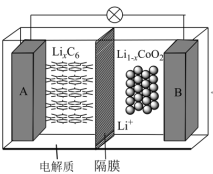
(4)放电时A电极为__ (填“正”或“负”)极,该电极的电极方程式为__ 。
(5)若该锂离子电池充电时,B电极的电极反应方程式为__ 。
(6)若用该锂离子电池给铁片上镀铜,铜片应连接该锂离子电池的极__ (填“A”或“B”),维持电流强度为1A,电池工作二十分钟,理论消耗Cu__ g(已知F=96500C•mol-1,保留两位有效数字)。

(1)碳棒电极为
(2)在甲室中加入异丙醇的作用是
(3)在甲室中得到产品己二腈54g时,乙室中质量减轻
(二)2019年诺贝尔化学奖颁给了三个人,其中一个是Goodenough(古迪纳夫),他因为发明可充电锂离子电池而闻名于世,他建造了锂离子电池的神经系统,被业界称为“锂电池之父”。其中一款是钴酸锂(LiCoO2)电池,它的工作原理如图所示,图中电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xCoO2
 C6+LiCoO2。
C6+LiCoO2。
(4)放电时A电极为
(5)若该锂离子电池充电时,B电极的电极反应方程式为
(6)若用该锂离子电池给铁片上镀铜,铜片应连接该锂离子电池的极
您最近一年使用:0次
名校
解题方法
10 . 一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。回答下列问题:
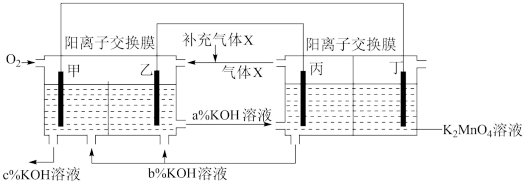
(1)甲为电源的___ 极。
(2)乙极的电极反应式为___ ,丁极的电极反应式为___ 。
(3)KOH溶液的质量分数,将a%、b%、c%由大到小排序___ 。
(4)标准状况下,甲电极上每消耗22.4L气体时,理论上阳极区减轻质量__ g,阴极区产生___ molOH-。

(1)甲为电源的
(2)乙极的电极反应式为
(3)KOH溶液的质量分数,将a%、b%、c%由大到小排序
(4)标准状况下,甲电极上每消耗22.4L气体时,理论上阳极区减轻质量
您最近一年使用:0次



