1 . 根据如图所示的装置,完成下列各空。
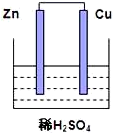
(1)该装置中的总反应式为___________ 。
(2)溶液中的H+移向___________ (填“Cu片”或“Zn片”)
(3)Zn电极的反应式为___________ ,发生 ___________ 反应,(填“氧化”或“还原”)
(4)Cu片为原电池的___________ 极(填“正”或“负”),现象为___________ 。

(1)该装置中的总反应式为
(2)溶液中的H+移向
(3)Zn电极的反应式为
(4)Cu片为原电池的
您最近一年使用:0次
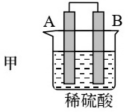
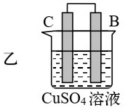
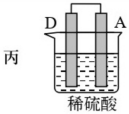
2 . 由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)装置乙溶液中C电极反应:_______ ;外电路中电子由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)装置乙溶液中C电极反应:
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次
3 . 原电池是直接把化学能转化为电能的装置。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)____ ;稀硫酸的作用是________ 。
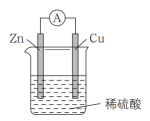
a.负极反应物 b.负极材料 c.正极反应物
d.正极材料 e.离子导体 f.电子导体
(2) ①在Cu-Zn原电池中,Zn片上发生________ 反应(填“氧化”或“还原”)。Cu片上发生的电极反应为________ 。
②外电路中电子流向_____ 极;内电路溶液中SO 移向
移向___ 极。
③能证明化学能转化为电能的实验现象为________ 。
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是__ 。

(4)从化学的角度分析,原电池装置产生电流的原因是:原电池可将________ ,并通过能导电的物质形成闭合回路,产生电流。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)

a.负极反应物 b.负极材料 c.正极反应物
d.正极材料 e.离子导体 f.电子导体
(2) ①在Cu-Zn原电池中,Zn片上发生
②外电路中电子流向
 移向
移向③能证明化学能转化为电能的实验现象为
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是

(4)从化学的角度分析,原电池装置产生电流的原因是:原电池可将
您最近一年使用:0次
名校
解题方法
4 . 电化学原理在探究物质性质和实际生产中应用广泛,据此回答下列问题。
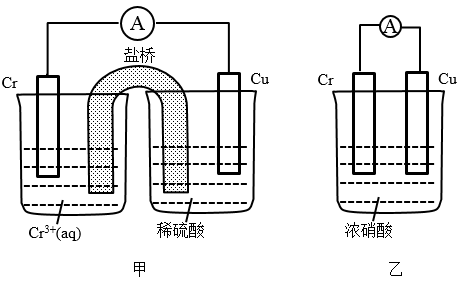
(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜__ (填“强”或“弱”);由装置乙知常温下铬在浓硝酸中出现__ 现象。
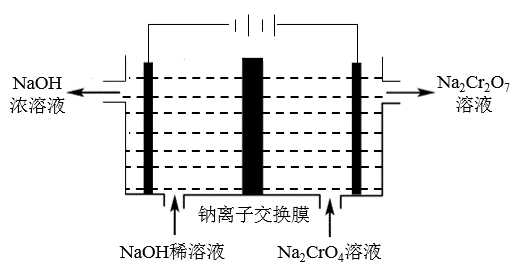
(2)工业上使用如图装置,以石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为__ 。
(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为__ 。阴极上Cr2O 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为__ ;若H+放电,则阴极区形成Fe(OH)3和Cr(OH)3沉淀。
②铁氧磁体法:在含Cr(Ⅵ)的废水中加入绿矾,在pH<4时发生反应使Cr(Ⅵ)转化为Cr(Ⅲ),调节溶液pH为6~8,使溶液中的Fe(Ⅱ)、Fe(Ⅲ)、Cr(Ⅲ)析出组成相当于Fe(Ⅱ)[Fe(Ⅲ)x•Cr(Ⅲ)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=___ 。
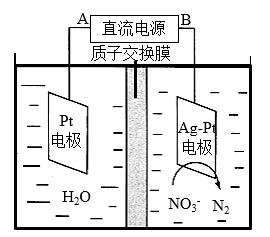
(4)电解法还可用于处理酸性硝酸盐污水,设计如图电解池。若电解过程中转移了0.1mol电子,则质子交换膜两侧电解液的质量变化差(△m左−△m右)为___ g。

(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜
(2)工业上使用如图装置,以石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为

(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O
 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为②铁氧磁体法:在含Cr(Ⅵ)的废水中加入绿矾,在pH<4时发生反应使Cr(Ⅵ)转化为Cr(Ⅲ),调节溶液pH为6~8,使溶液中的Fe(Ⅱ)、Fe(Ⅲ)、Cr(Ⅲ)析出组成相当于Fe(Ⅱ)[Fe(Ⅲ)x•Cr(Ⅲ)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=
(4)电解法还可用于处理酸性硝酸盐污水,设计如图电解池。若电解过程中转移了0.1mol电子,则质子交换膜两侧电解液的质量变化差(△m左−△m右)为

您最近一年使用:0次
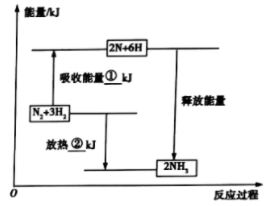
5 . (1)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1mol氮气中的化学键需要吸收946kJ能量;破坏0.5mol氢气中的 键需要吸收218kJ能量;形成氨分子中1mol
键需要吸收218kJ能量;形成氨分子中1mol 键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
①______ kJ,②_____ kJ。
(2)由A、B、C、D四种金属按如表所示装置进行实验。
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为_______________ 。
②装置乙中正极的电极反应式为_______________ 。
③装置丙中溶液的pH_________ (填“变大”“变小”或“不变”)
④四种金属的活动性由强到弱的顺序是____________ 。
(3)一定温度下,在体积为2L的恒容密闭容器中充入1mol 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: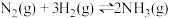 ,测得其中
,测得其中 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
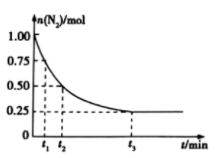
从开始反应到 min,氮气的平均反应速率为
min,氮气的平均反应速率为_________ 。
 键需要吸收218kJ能量;形成氨分子中1mol
键需要吸收218kJ能量;形成氨分子中1mol 键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。①

(2)由A、B、C、D四种金属按如表所示装置进行实验。
| 装置 | 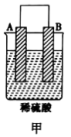 | 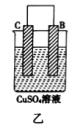 | 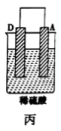 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中负极的电极反应式为
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(3)一定温度下,在体积为2L的恒容密闭容器中充入1mol
 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: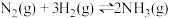 ,测得其中
,测得其中 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
从开始反应到
 min,氮气的平均反应速率为
min,氮气的平均反应速率为
您最近一年使用:0次
解题方法
6 . 原电池是将化学能转化为电能的装置。
(1)a为铜片,b为铁片,烧杯中是稀硫酸溶液。
①当开关K断开时产生的现象为___________ 。
A.a不断溶解
B.b不断溶解
C.a上产生气泡
D.b上产生气泡
E.溶液逐渐变蓝
②闭合开关K,反应一段时间后断开开关K,经过一段时间后,下列叙述不正确的是___________ 。
A.溶液中H+浓度减小 B.正极附近 浓度逐渐增大
浓度逐渐增大
C.溶液中含有FeSO4 D.溶液中 浓度基本不变
浓度基本不变
(2)FeCl3常用于腐蚀印刷电路铜板,若将此反应设计成原电池,请写出该原电池正极电极反应为___________ 。
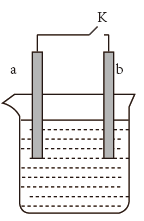
(3)下图为氢氧燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:
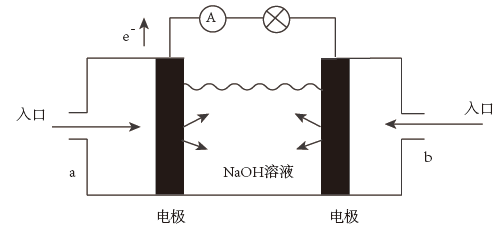
①a极通入的物质为___________ ,电解质溶液中的 移向
移向___________ 极(选填“负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:___________ 。
③当消耗氢气11.2L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子的物质的量为___________ mol。

(1)a为铜片,b为铁片,烧杯中是稀硫酸溶液。
①当开关K断开时产生的现象为
A.a不断溶解
B.b不断溶解
C.a上产生气泡
D.b上产生气泡
E.溶液逐渐变蓝
②闭合开关K,反应一段时间后断开开关K,经过一段时间后,下列叙述不正确的是
A.溶液中H+浓度减小 B.正极附近
 浓度逐渐增大
浓度逐渐增大C.溶液中含有FeSO4 D.溶液中
 浓度基本不变
浓度基本不变(2)FeCl3常用于腐蚀印刷电路铜板,若将此反应设计成原电池,请写出该原电池正极电极反应为
(3)下图为氢氧燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:

①a极通入的物质为
 移向
移向②写出此氢氧燃料电池工作时,负极的电极反应式:
③当消耗氢气11.2L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子的物质的量为
您最近一年使用:0次
名校
解题方法
7 . 把A、B、C、D四种金属按表中装置进行实验。
根据实验现象回答问题:
(1)装置乙中正极的电极反应式是___ 。
(2)装置丙中溶液的酸性___ (填“变大”“变小”或“不变”)。
(3)四种金属活泼性由强到弱的顺序是___ 。
| 装置 | 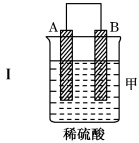 |  | 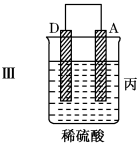 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置乙中正极的电极反应式是
(2)装置丙中溶液的酸性
(3)四种金属活泼性由强到弱的顺序是
您最近一年使用:0次
2021-04-14更新
|
223次组卷
|
3卷引用:湖南省长沙市南雅中学2020-2021学年高一下学期第一次月考化学试题
解题方法
8 . 由下列实验操作和现象得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Co2O3中滴加浓盐酸 | 产生黄绿色气体 | 氧化性:Cl2<Co2O3 |
| B | 在镁、铝为电极,氢氧化钠为电解质的原电池装置 | 镁表面有气泡 | 金属活动性:Al>Mg |
| C | 蘸有浓氨水的玻璃棒靠近溶液X | 有白烟 | X可能是浓盐酸 |
| D | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3的反应具有可逆性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-09-24更新
|
175次组卷
|
2卷引用:湖北省孝感市普通高中2021-2022学年高三上学期期中联考化学试题
9 . (1)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1molN2中的 键需要吸收
键需要吸收 能量;破坏
能量;破坏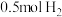 中的
中的 键需要吸收
键需要吸收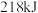 能量;形成
能量;形成 中的
中的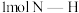 键能释放
键能释放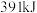 能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
①________________  ,②
,②____________________  。
。

(2)用A、B、C、D四种金属按如表所示的装置进行实验。
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为__________________ 。
②装置乙中正极的电极反应式为________________ 。
③装置丙中溶液的pH________ (填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是________ 。
(3)一定温度下,在体积为 的恒容密闭容器中充入
的恒容密闭容器中充入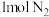 和
和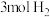 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
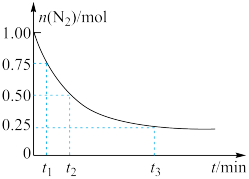
从开始反应到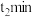 ,用
,用 表示的化学反应速率为
表示的化学反应速率为_________ 。
 键需要吸收
键需要吸收 能量;破坏
能量;破坏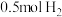 中的
中的 键需要吸收
键需要吸收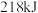 能量;形成
能量;形成 中的
中的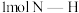 键能释放
键能释放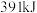 能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。①
 ,②
,② 。
。
(2)用A、B、C、D四种金属按如表所示的装置进行实验。
| 装置 |  甲 |  乙 |  丙 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(3)一定温度下,在体积为
 的恒容密闭容器中充入
的恒容密闭容器中充入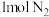 和
和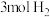 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
从开始反应到
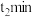 ,用
,用 表示的化学反应速率为
表示的化学反应速率为
您最近一年使用:0次
2020-09-24更新
|
650次组卷
|
3卷引用:陕西省咸阳市武功县普集高级中学2020-2021学年高一下学期第三次月考化学试题
解题方法
10 . 由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题(用符号A、B、C、D回答下列问题)
(1)装置甲中负极 为___ 。装置丙中负极 为__ 。
(2)装置乙中正极 的电极反应式是___ 。
(3)四种金属活泼性由强到弱 的顺序是___ 。
| 装置 |  甲 甲 |  乙 乙 |  丙 丙 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题(用符号A、B、C、D回答下列问题)
(1)装置甲中
(2)装置乙中
(3)四种金属活泼性
您最近一年使用:0次