名校
解题方法
1 . 微生物燃料电池(MFC)耦合人工湿地(CW)系统可用于生产生活废水处理并提供电能,系统内产电微生物由根沉积物和废水提供,其原理如图所示,下列有关MFC-CW系统叙述正确的是
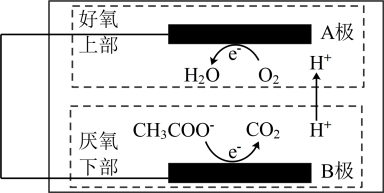

| A.电子由A极经外电路流向B极 |
| B.A极发生氧化反应 |
C.消耗2.24L 时,转移0.4NA电子 时,转移0.4NA电子 |
D.B极反应式为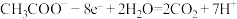 |
您最近一年使用:0次
2022-07-14更新
|
266次组卷
|
2卷引用:四川省广安市2021-2022学年高一下学期期末考试化学试题
解题方法
2 . 如图为原电池构造示意图,下列有关说法正确的是
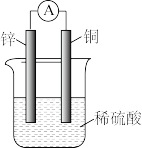

| A.铜片上有气泡产生 |
| B.锌是原电池正极 |
| C.铜片上发生反应Cu-2e- = Cu2+ |
| D.该装置电流计的指针不发生偏转 |
您最近一年使用:0次
2022-07-12更新
|
66次组卷
|
2卷引用:四川省内江市2021-2022学年高一下学期期末检测文科化学试题
解题方法
3 . 对化学反应原理的研究能让我们更加深刻地认识化学反应,也是化学中最有魅力和挑战性的领域,依据所学的化学反应原理知识和题干信息回答下列问题:
I.面对气候变化,我国承诺二氧化碳排放力争2030年前达到峰值,力争2060年前实现碳中和。“碳达峰、碳中和”目标下,必须加强对二氧化碳资源开发利用的研究。
(1)往容积为2L的恒容密闭容器中通入2mol 和6mol
和6mol ,一定温度下发生反应:
,一定温度下发生反应: ,20min时达到化学平衡状态,测得水蒸气的物质的量为2mol,前20min内,用
,20min时达到化学平衡状态,测得水蒸气的物质的量为2mol,前20min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为___________  ,
, 的平衡转化率
的平衡转化率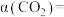
___________ %(保留一位小数)。[注:转化率等于反应物消耗的物质的量与反应物初始的物质的量之比。]
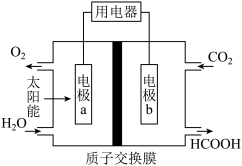
(2)一种 电化学制甲酸的装置如图所示,电极a为
电化学制甲酸的装置如图所示,电极a为___________ 极(填“正”或“负”),写出电极b的电极反应式___________ 。
II.催化剂的研究是化学反应原理中一个重要领域,催化剂往往是化学工业过程和技术改造更新的关键。化学反应中的活化能会显著影响化学反应速率,活化能越低,化学反应速率越快。催化剂能加快化学反应速率是因为它能改变反应的路径,降低反应的活化能。
(3) 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
由上表判断,催化剂X______ Y(填“优于”或“劣于”),理由是_____ 。
(4)催化剂的存在会显著地加快 的分解,某兴趣小组研究
的分解,某兴趣小组研究 催化分解
催化分解 历程如下:
历程如下:
第一步: (慢反应)
(慢反应)
第二步:______(快反应)
反应的活化能较大的为第___________ 步(填“一”或“二”),第二步反应的离子方程式为___________ 。
I.面对气候变化,我国承诺二氧化碳排放力争2030年前达到峰值,力争2060年前实现碳中和。“碳达峰、碳中和”目标下,必须加强对二氧化碳资源开发利用的研究。
(1)往容积为2L的恒容密闭容器中通入2mol
 和6mol
和6mol ,一定温度下发生反应:
,一定温度下发生反应: ,20min时达到化学平衡状态,测得水蒸气的物质的量为2mol,前20min内,用
,20min时达到化学平衡状态,测得水蒸气的物质的量为2mol,前20min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为 ,
, 的平衡转化率
的平衡转化率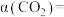
(2)一种
 电化学制甲酸的装置如图所示,电极a为
电化学制甲酸的装置如图所示,电极a为
II.催化剂的研究是化学反应原理中一个重要领域,催化剂往往是化学工业过程和技术改造更新的关键。化学反应中的活化能会显著影响化学反应速率,活化能越低,化学反应速率越快。催化剂能加快化学反应速率是因为它能改变反应的路径,降低反应的活化能。
(3)
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:积碳反应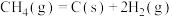 | 消碳反应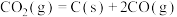 | ||
活性能/ | 催化剂X | 33 | 91 |
| 催化剂Y | 43 | 72 | |
(4)催化剂的存在会显著地加快
 的分解,某兴趣小组研究
的分解,某兴趣小组研究 催化分解
催化分解 历程如下:
历程如下:第一步:
 (慢反应)
(慢反应)第二步:______(快反应)
反应的活化能较大的为第
您最近一年使用:0次
2022-07-12更新
|
376次组卷
|
2卷引用:四川省雅安市2021-2022学年高一下学期期末检测化学试题
4 . I.化学反应的快慢和限度对人类生产、生活有重要的影响。800°C时,A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,回答下列问题:
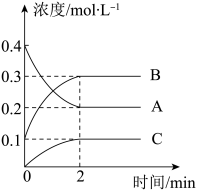
(1)该反应的生成物是_______ 。
(2)2min内,C的反应速率为________ 。
(3)该条件下,为加快反应速率,下列措施不可行的是_______(填选项)。
II.一种微生物电池处理含氮( )废水的装置如图所示:。
)废水的装置如图所示:。
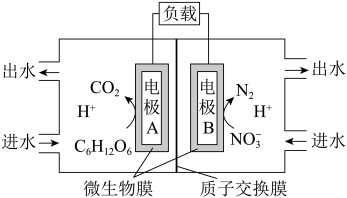
(4)电极A是_______ (填“正”或“负”)极,其电极反应式为_______ ;电极B上发生_______ 反应(填“氧化”或“还原”)。
(5)工作过程中,H+通过质子交换膜向电极_______ (填“A”或“B”)方向移动;电路中每转移2mol电时,产生氮气的体积在标准状况下是_______ L。

(1)该反应的生成物是
(2)2min内,C的反应速率为
(3)该条件下,为加快反应速率,下列措施不可行的是_______(填选项)。
| A.增大A的量 | B.通入稀有气体Ar |
| C.加入合适的催化剂 | D.压缩容器体积 |
II.一种微生物电池处理含氮(
 )废水的装置如图所示:。
)废水的装置如图所示:。
(4)电极A是
(5)工作过程中,H+通过质子交换膜向电极
您最近一年使用:0次
解题方法
5 . 镁和次氯酸盐燃料电池的工作原理为Mg+ClO-+H2O=Mg(OH)2+Cl-。下列说法错误的是
| A.镁作负极材料,发生氧化反应 |
| B.放电时,所有阴离子都向负极迁移 |
| C.负极反应式为Mg+2OH-—2e-=Mg(OH)2 |
| D.消耗12g镁时转移1mol电子 |
您最近一年使用:0次
2022-07-10更新
|
176次组卷
|
2卷引用:四川省南充市2021-2022学年高一下学期期末考试化学试题
名校
6 . 芬兰Enfucell公司造出了一种纸质碱性电池,电解质溶液为KOH,其电池总反应为Zn+2MnO2+H2O=2MnOOH+ZnO。下列说法正确的是
| A.该电池的正极材料为锌 |
| B.电池正极反应式为:MnO2+e-+H2O=MnOOH+OH- |
| C.当0.1molZn完全溶解时,流经电解质溶液的电子数目为1.204×1023 |
| D.该电池内部OH-移向正极 |
您最近一年使用:0次
2022-07-01更新
|
175次组卷
|
2卷引用:四川省绵阳市南山中学2021-2022学年高一下学期6月月考化学试题
名校
解题方法
7 . 某化学小组为了探究原电池的基本原理,设计装置如图。下列相关分析错误的是
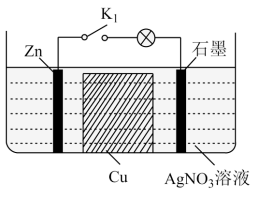

| A.电池工作时,石墨电极发生反应:Ag++e-=Ag |
| B.电池中Cu块取出前后灯泡亮度会发生变化 |
| C.一段时间后铜块无明显变化 |
| D.Zn为该电池的负极,发生氧化反应 |
您最近一年使用:0次
2022-05-17更新
|
92次组卷
|
2卷引用:四川省雅安市2021-2022学年高一下学期期末检测化学试题
解题方法
8 . CH4、CH3OH(甲醇)既是重要的化工原料,又是未来重要的能源物质。
(1)CH4可用作燃料,CH4的燃烧反应属于_______  填“放热,,或“吸热”
填“放热,,或“吸热” 反应,CH4和O2还可以构成燃料电池,通入CH4的一极是
反应,CH4和O2还可以构成燃料电池,通入CH4的一极是_______  填“正”或“负”
填“正”或“负” 极。
极。
(2)将1.0 molCH4和2.0 molH2O(g)通入容积为V L的恒容反应室,在一定条件下发生反应 。测得在5 min时达到平衡,CH4的物质的量为0.6 mol,CO的物质的量浓度为0.04 mol/L。
。测得在5 min时达到平衡,CH4的物质的量为0.6 mol,CO的物质的量浓度为0.04 mol/L。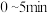 内,用H2表示该反应的平均反应速率v(H2)=
内,用H2表示该反应的平均反应速率v(H2)=_______ ,V=_______ 。
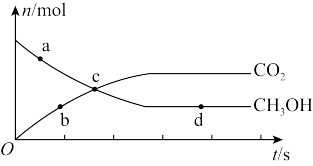
(3)在恒容条件下进行反应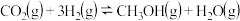 、CO2、CH3OH的物质的量随时间变化关系如图,该反应达到平衡的点是
、CO2、CH3OH的物质的量随时间变化关系如图,该反应达到平衡的点是_______ 。
(1)CH4可用作燃料,CH4的燃烧反应属于
 填“放热,,或“吸热”
填“放热,,或“吸热” 反应,CH4和O2还可以构成燃料电池,通入CH4的一极是
反应,CH4和O2还可以构成燃料电池,通入CH4的一极是 填“正”或“负”
填“正”或“负” 极。
极。(2)将1.0 molCH4和2.0 molH2O(g)通入容积为V L的恒容反应室,在一定条件下发生反应
 。测得在5 min时达到平衡,CH4的物质的量为0.6 mol,CO的物质的量浓度为0.04 mol/L。
。测得在5 min时达到平衡,CH4的物质的量为0.6 mol,CO的物质的量浓度为0.04 mol/L。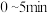 内,用H2表示该反应的平均反应速率v(H2)=
内,用H2表示该反应的平均反应速率v(H2)=(3)在恒容条件下进行反应
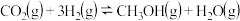 、CO2、CH3OH的物质的量随时间变化关系如图,该反应达到平衡的点是
、CO2、CH3OH的物质的量随时间变化关系如图,该反应达到平衡的点是
您最近一年使用:0次
2022-05-06更新
|
27次组卷
|
2卷引用:四川省广安市育才学校2022-2023学年高一上学期9月月考化学试题
名校
解题方法
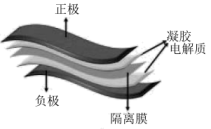
9 . 有一种可穿戴电池,其结构如图所示,该电池的总反应为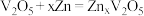 ,关于此电池,下列说法错误的是
,关于此电池,下列说法错误的是
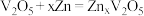 ,关于此电池,下列说法错误的是
,关于此电池,下列说法错误的是
A. 为负极,生成的 为负极,生成的 向正极移动 向正极移动 |
B.正极反应式为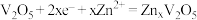 |
C.当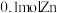 溶解时,有 溶解时,有 电子由负极经隔离膜流向正极 电子由负极经隔离膜流向正极 |
| D.凝胶电解质可提高电池的安全性和稳定性 |
您最近一年使用:0次
2022-05-03更新
|
251次组卷
|
4卷引用:四川省南充高级中学2021-2022学年高一下学期第二次月考化学试题
四川省南充高级中学2021-2022学年高一下学期第二次月考化学试题湖北省六校新高考联盟2021-2022学年高一下学期4月联考化学试题湖北省潜江市园林高级中学2021-2022学年高一下学期五月月考化学试题(已下线)第15练 化学反应与能量变化-2023年高考化学一轮复习小题多维练(全国通用)
名校
10 . 氨、硫酸都是重要的工业原料,根据题意完成下列各题。
(1)工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为_______ 。
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为_______ 。
(3)将硫酸工业尾气中的SO2转化成硫酸,同时获得电能。装置如图所示(电极均为惰性材料):
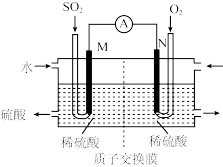
①原电池的负极为_______ 。(填“M”或“N”)
②M极发生的电极反应式为_______ 。
(1)工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为
(3)将硫酸工业尾气中的SO2转化成硫酸,同时获得电能。装置如图所示(电极均为惰性材料):

①原电池的负极为
②M极发生的电极反应式为
您最近一年使用:0次



