名校
解题方法
1 . 某研究性学习小组的同学对 、
、 、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
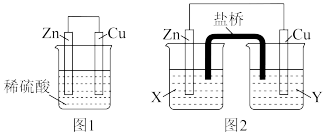
(1)实验表明,图1中铜电极上有气泡产生,说明反应中有一部分化学能转化为___________ 能。锌电极为___________ 极(填写“正”或“负”),电极反应为:___________
(2)图2中实验过程中只有Cu极上产生气泡,则X是_______ 溶液,正极上的电极反应式为_______ 。
(3)当图1装置中的溶液质量增加63g时,生成氢气_______ L(标准状况);当图2中锌电极的质量减少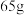 时,电路中转移的电子为
时,电路中转移的电子为_______  。
。
 、
、 、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
(1)实验表明,图1中铜电极上有气泡产生,说明反应中有一部分化学能转化为
(2)图2中实验过程中只有Cu极上产生气泡,则X是
(3)当图1装置中的溶液质量增加63g时,生成氢气
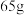 时,电路中转移的电子为
时,电路中转移的电子为 。
。
您最近一年使用:0次
解题方法
2 . 某实验小组为探究CuSO4与Na2SO3反应后的产物,做如下探究实验。
【查阅资料】
①Cu2O为砖红色固体,不溶于水;
②Cu2SO3为黄色固体,不溶于水;
③[Cu(SO3)2]3-为无色配合离子、[Cu(NH3)2]+为无色配合离子、[Cu(NH3)4]2+为深蓝色配合离子。
【实验探究】
实验1:①向2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,开始出现黄色沉淀,但无气体产生。
②继续加入Na2SO3溶液,最终沉淀消失。经检验,溶液中生成[Cu(SO3)2]3-离子。
实验2:向90℃ 2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,直接生成砖红色沉淀。
实验3:向2mL0.2mol∙L-1的Na2SO3溶液中滴加0.2mol∙L-1的CuSO4溶液,开始阶段有蓝色沉淀出现。
(1)S元素在元素周期表中的位置为_______ 。N、O、S三种元素原子的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)某同学认为实验1黄色沉淀中有少量Cu(OH)2,该同学认为是CuSO4、Na2SO3相互促进水解产生的,用离子方程式表示生成Cu(OH)2沉淀的过程:_______ 。
(3)经检验,实验2所得溶液中有大量 、
、 生成。该实验中Cu2+表现
生成。该实验中Cu2+表现_______ 性,写出该实验中反应的离子方程式:_______ 。
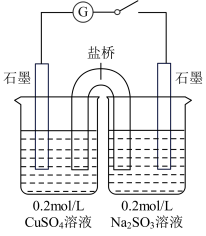
(4)某同学设计了如图所示的电化学装置,探究CuSO4与Na2SO3的反应。该装置中左侧烧杯中的石墨电极做_______ (填“正”或“负”)极,右侧烧杯中发生反应的电极反应式为_______ 。设计实验检验右侧烧杯中生成的阴离子,写出具体操作、现象和结论:_______ 。
【查阅资料】
①Cu2O为砖红色固体,不溶于水;
②Cu2SO3为黄色固体,不溶于水;
③[Cu(SO3)2]3-为无色配合离子、[Cu(NH3)2]+为无色配合离子、[Cu(NH3)4]2+为深蓝色配合离子。
【实验探究】
实验1:①向2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,开始出现黄色沉淀,但无气体产生。
②继续加入Na2SO3溶液,最终沉淀消失。经检验,溶液中生成[Cu(SO3)2]3-离子。
实验2:向90℃ 2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,直接生成砖红色沉淀。
实验3:向2mL0.2mol∙L-1的Na2SO3溶液中滴加0.2mol∙L-1的CuSO4溶液,开始阶段有蓝色沉淀出现。
(1)S元素在元素周期表中的位置为
(2)某同学认为实验1黄色沉淀中有少量Cu(OH)2,该同学认为是CuSO4、Na2SO3相互促进水解产生的,用离子方程式表示生成Cu(OH)2沉淀的过程:
(3)经检验,实验2所得溶液中有大量
 、
、 生成。该实验中Cu2+表现
生成。该实验中Cu2+表现(4)某同学设计了如图所示的电化学装置,探究CuSO4与Na2SO3的反应。该装置中左侧烧杯中的石墨电极做

您最近一年使用:0次
解题方法
3 . I.某研究性学习小组的同学对Zn、Cu、稀硫酸组成的原电池进行了探究,其中甲同学利用如图 所示装置进行探究,乙同学经过查阅资料后设计了图
所示装置进行探究,乙同学经过查阅资料后设计了图 装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。

(1)实验表明,图 中铜电极上有气泡产生,说明反应中有一部分化学能转化为
中铜电极上有气泡产生,说明反应中有一部分化学能转化为_______ 能。锌电极为_______ 极(填写“正”或“负”),电极反应为:_______ 。
(2)图 中实验过程中只有
中实验过程中只有 极上产生气泡,则
极上产生气泡,则 是
是_______ 溶液,正极上的电极反应式为_______ 。
(3)当图 装置中的溶液质量增加
装置中的溶液质量增加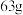 时,生成氢气
时,生成氢气_______ L(标准状况);当图 中锌电极的质量减少
中锌电极的质量减少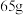 时,电路中转移的电子为
时,电路中转移的电子为_______ 
II.已知反应: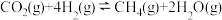
(4)已知下列数据:
若反应生成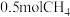
_______ (释放或者吸收)_______ 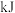 能量。
能量。
(5)在一定温度下,向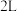 密闭容器中充入
密闭容器中充入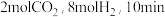 达到平衡,平衡时,测得
达到平衡,平衡时,测得 的体积分数为
的体积分数为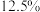 。
。 内,
内, 的平均反应速率为
的平均反应速率为_______ ,平衡时 的转化率为
的转化率为_______ 。
 所示装置进行探究,乙同学经过查阅资料后设计了图
所示装置进行探究,乙同学经过查阅资料后设计了图 装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
(1)实验表明,图
 中铜电极上有气泡产生,说明反应中有一部分化学能转化为
中铜电极上有气泡产生,说明反应中有一部分化学能转化为(2)图
 中实验过程中只有
中实验过程中只有 极上产生气泡,则
极上产生气泡,则 是
是(3)当图
 装置中的溶液质量增加
装置中的溶液质量增加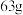 时,生成氢气
时,生成氢气 中锌电极的质量减少
中锌电极的质量减少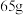 时,电路中转移的电子为
时,电路中转移的电子为
II.已知反应:
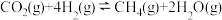
(4)已知下列数据:
| 化学键 |  |  | 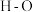 |  |
| 断裂化学键吸收的能量kJ/mol |  | 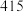 |  | 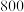 |
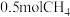
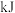 能量。
能量。(5)在一定温度下,向
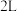 密闭容器中充入
密闭容器中充入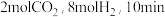 达到平衡,平衡时,测得
达到平衡,平衡时,测得 的体积分数为
的体积分数为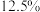 。
。 内,
内, 的平均反应速率为
的平均反应速率为 的转化率为
的转化率为
您最近一年使用:0次
名校
解题方法
4 . 人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息填空。
(1)铅蓄电池在放电时起原电池作用,铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。负极反应式为____ ;反应一段时间后负极的质量___ (填“增重”或“减少”或“不变”)
(2)燃料电池是一种高效、环境友好的供电装置,如甲烷燃料电池,在碱性条件下该电池的负电极反应式是:____ 。
(3)将铝片和铜片用导线相连,分别插入浓硝酸中(a组)和插入烧碱溶液中(b组),都形成了原电池,在a组原电池中,负极材料为____ ;写出b组插入烧碱溶液中形成原电池的负极反应式:___ 。
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为____ ,电解质溶液为____ ,反应中Cl-移向___ (填“负极”或“正极”),FeCl3溶液发生____ 反应(填“氧化”或“还原”)。
(5)碱性纽扣电池的总反应为Zn+Ag2O=2Ag+ZnO,其正极反应式为____ 。
(1)铅蓄电池在放电时起原电池作用,铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。负极反应式为
(2)燃料电池是一种高效、环境友好的供电装置,如甲烷燃料电池,在碱性条件下该电池的负电极反应式是:
(3)将铝片和铜片用导线相连,分别插入浓硝酸中(a组)和插入烧碱溶液中(b组),都形成了原电池,在a组原电池中,负极材料为
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(5)碱性纽扣电池的总反应为Zn+Ag2O=2Ag+ZnO,其正极反应式为
您最近一年使用:0次
2022-03-30更新
|
314次组卷
|
2卷引用:江西省宜春市上高二中2021-2022学年高一下学期第六次月考试题(3月)化学试题
名校
5 . 回答下列问题:
(1)根据氧化还原反应:Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移0.01mol电子时两电极的质量差为____ g。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
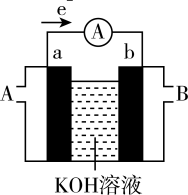
①假设使用的“燃料”是氢气(H2),则a极的电极反应式为____ 。若电池中氢气(H2)通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为____ C。(已知一个电子所带电量为1.6×10−19C,NA约为6.02×1023mol−1)。
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为____ ,如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为____ (用NA表示)。
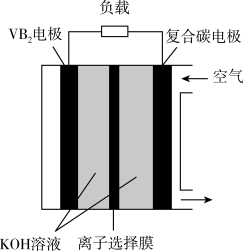
(3)一种高性能的碱性硼化钒(VB2)—空气电池如图所示,电池总反应为4VB2+11O2+20OH-+6H2O=8B(OH) +4VO
+4VO 。VB2电极发生的电极反应为
。VB2电极发生的电极反应为____ 。
(1)根据氧化还原反应:Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移0.01mol电子时两电极的质量差为
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①假设使用的“燃料”是氢气(H2),则a极的电极反应式为
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为
(3)一种高性能的碱性硼化钒(VB2)—空气电池如图所示,电池总反应为4VB2+11O2+20OH-+6H2O=8B(OH)
 +4VO
+4VO 。VB2电极发生的电极反应为
。VB2电极发生的电极反应为
您最近一年使用:0次
解题方法
6 . 根据化学能转化为电能的相关知识,回答下列问题:
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是____ ,发生____ (填“氧化”或”还原”)反应,电解质溶液是____ 。
(2)正极上出现的现象是____ 。
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:
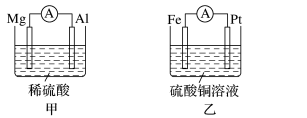
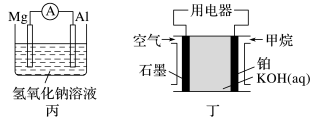
(3)丙装置中负极反应式为____ ,丁装置中负极反应式为____ 。
(4)电池的放电过程中,甲装置中溶液质量____ (填“增加”或“减少”);丁装置中溶液碱性____ (填“增强”或减弱”)。
(5)当甲装置导线中转移0.3mol电子时,正极生成气体____ L(标准状况下);假设开始时乙装置中两电极质量相等,导线中转移0.3mol电子时,两电极质量相差____ g。
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:


(3)丙装置中负极反应式为
(4)电池的放电过程中,甲装置中溶液质量
(5)当甲装置导线中转移0.3mol电子时,正极生成气体
您最近一年使用:0次
名校
7 . 从能量变化和反应快慢等角度研究化学反应具有重要意义。
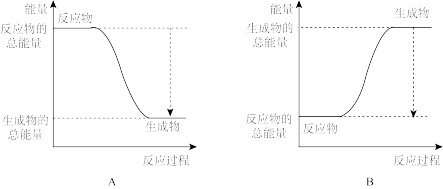
(1)已知一定条件下,反应N2+3H2 2NH3为放热反应,下图能正确表示该反应中能量变化的是
2NH3为放热反应,下图能正确表示该反应中能量变化的是___________ ;(填“A”或“B”)
(2)研究高效催化剂是解决汽车尾气中的NO和CO对大气污染的重要途径。
已知:C(s)+O2(g)=CO2(g) △H1= -393.5 kJ/mol
C(s)+ O2(g)= CO(g) △H2= -110.5 kJ/mol
O2(g)= CO(g) △H2= -110.5 kJ/mol
N2(g)+ O2(g)=2NO(g) △H3= +180.0 kJ/mol
则汽车尾气的催化转化反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的△H =___________ kJ/mol。
(3)某兴趣小组为研究原电池原理,设计下图装置。

①Cu为原电池___________ 极(填“正”或“负”),其电极反应式是___________ ;
②溶液中SO 移向
移向___________ (填“Cu”或“Zn”极)。当负极金属溶解13.0 g时,通过导线的电子数___________ 。
③甲烷(CH4)燃料电池在碱性介质(电解质为KOH溶液)中的电极反应方程式:
负极:___________ ,正极:___________ 。
(1)已知一定条件下,反应N2+3H2
 2NH3为放热反应,下图能正确表示该反应中能量变化的是
2NH3为放热反应,下图能正确表示该反应中能量变化的是
(2)研究高效催化剂是解决汽车尾气中的NO和CO对大气污染的重要途径。
已知:C(s)+O2(g)=CO2(g) △H1= -393.5 kJ/mol
C(s)+
 O2(g)= CO(g) △H2= -110.5 kJ/mol
O2(g)= CO(g) △H2= -110.5 kJ/molN2(g)+ O2(g)=2NO(g) △H3= +180.0 kJ/mol
则汽车尾气的催化转化反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的△H =
(3)某兴趣小组为研究原电池原理,设计下图装置。

①Cu为原电池
②溶液中SO
 移向
移向③甲烷(CH4)燃料电池在碱性介质(电解质为KOH溶液)中的电极反应方程式:
负极:
您最近一年使用:0次
名校
解题方法
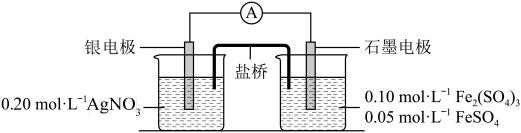
8 . 为验证反应 ,利用如图电池装置进行实验。
,利用如图电池装置进行实验。
(1)由 固体配制500mL
固体配制500mL
 溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、药匙、托盘天平、
溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、药匙、托盘天平、_______ (填写名称);在烧杯中溶解固体时,先加入一定体积的_______ 稀溶液,搅拌后再加入一定体积的水。
(2)电流表显示电流由银电极流向石墨电极。可知,盐桥中的阳离子进入_______ 电极溶液中。
(3)根据(2)实验结果,可知石墨电极的电极反应式为_______ ,银电极的电极反应式为_______ 。因此, 氧化性小于
氧化性小于_______ 。
(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为 ,反应一段时间后,可以观察到电流表指针反转,原因是
,反应一段时间后,可以观察到电流表指针反转,原因是_______ 。
 ,利用如图电池装置进行实验。
,利用如图电池装置进行实验。
(1)由
 固体配制500mL
固体配制500mL
 溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、药匙、托盘天平、
溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、药匙、托盘天平、(2)电流表显示电流由银电极流向石墨电极。可知,盐桥中的阳离子进入
(3)根据(2)实验结果,可知石墨电极的电极反应式为
 氧化性小于
氧化性小于(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为
 ,反应一段时间后,可以观察到电流表指针反转,原因是
,反应一段时间后,可以观察到电流表指针反转,原因是
您最近一年使用:0次
2022-12-07更新
|
162次组卷
|
2卷引用:河南郑州外国语学校2022-2023学年高三上学期调研考试2化学试题
名校
9 . 甲醇燃料电池在碱性条件下的电池反应为2CH3OH+3O2+4OH-=2CO +6H2O。则下列有关说法不正确的是
+6H2O。则下列有关说法不正确的是
 +6H2O。则下列有关说法不正确的是
+6H2O。则下列有关说法不正确的是| A.O2在正极参与反应 | B.每转移0.6 mol电子,则消耗氧气的体积为3.36L |
C.负极反应为:CH3OH-6e-+8OH-=CO +6H2O +6H2O | D.该电池使用一段时间后溶液pH变小 |
您最近一年使用:0次
2022-03-20更新
|
254次组卷
|
2卷引用:宁夏青铜峡市高级中学2021-2022学年高二上学期期末考试化学试题
解题方法
10 . 利用CO2的氧化性制成的新型固态电池有望成为火星探测器的供电设备。该电池正、负极分别为碳纳米管、金属钠,Na3Zr2Si2PO12固体为电解质,电池放电时
| A.将电能转化为化学能 | B.CO2能在正极上得到电子 |
| C.电子通过Na3Zr2Si2PO12移向正极 | D.负极上发生还原反应 |
您最近一年使用:0次



